Por la Dra. María José Martínez Albarracín es médica y cirujana, catedrática de procesos diagnósticos clínicos, ha sido profesora de Bioquímica, Inmunología, y Técnicas Analíticas Instrumentales en el Ciclo Superior de Formación Profesiónal del “Laboratorio Diagnóstico Clínico”.

Resumen de conclusiones:
1.- La covid-19 grave es un síndrome de inmunidad alterada
2.- Puede, en todo caso, estar desencadenada por una infección vírica en determinadas circunstancias.
3.- Para que se produzca covid-grave es necesario que concurran determinadas situaciones fisiopatológicas e inmunopatológicas previas que pueden haber sido propiciadas por vacunaciones anteriores, especialmente la vacunación antigripal.
4.- Igualmente, determinadas condiciones metabólicas como diabetes, obesidad, y deficiencias de vitamina D activa, son determinantes en la Covid-19.
4.- Síndrome Hemofagocitico o de Enfermedad Aumentada por la Vacuna antigripal.
5.- Otros factores coadyuvantes serían aquellos capaces de inducir inmunodepresión, especialmente linfopenia, como es el caso de la exposición a REM especialmente las de alta potencia como la 5G y la proximidad a antenas emisoras, los pesticidas y herbicidas, metales pesados y otros tóxicos ambientales.
6.- Muchos tratamientos son totalmente inadecuados.
Cuando empezamos a saber de la “nueva enfermedad” supuestamente producida por el nuevo virus chino Sars-CoV-2, apenas sabíamos que era una neumonía intersticial bilateral. Luego supimos que había enfermos que fallecían por un síndrome inflamatorio hiperagudo o “Tormenta de Citocinas” y finalmente, cuando desoyendo las recomendaciones de la OMS un grupo de patólogos italianos empezaron a hacer autopsias supimos que los endotelios de diversos vasos sanguíneos, incluidas arterias, estaban dañados, trombosados y en ellos se producía acúmulo de NETs (trampas o redes de cromatina de neutrófilos apoptóticos).
Durante el verano y otoño de 2020, aunque se ha estado repitiendo reiterativamente por el oficialismo y los mass media que estábamos inmersos en supuestos rebrotes y “segundas olas” de covid-19, la clínica y fisiopatología de la citada covid no tenía nada que ver con la epidemia primaveral que se produjo de forma cuasi sincrónica, en muchos países del viejo mundo. Apenas catarros y asintomáticos: casos PCR positivo y alguna neumonía.
Un virólogo de la universidad de Zürich, nos confirma en el otoño-invierno de 2020 que el SarsCov2, según el modelo elaborado en Wuhan con la supuesta intención de crear una vacuna contra el VIH, se había extinguido por sí mismo. Su amiga, la patóloga Dra. Schmied de la Universidad de Ulm, utilizando fotos con el electromicroscopio del lavado bronquial de pacientes con Covid y haciendo posteriormente un cultivo celular, encuentra sólo en pacientes inmunodeprimidos con sintomatologia pulmonar, algunas particulas virales, de las cuales las menos son coronavirus. Sobre todo encuentra estafilococos, estreptococos, adenovirus y sorprendentemente, muy frecuentemente, Borrelia, y las Borrelias sabemos que aparecen en inmunosupresión. Curiosamente en el Lyme crónico (en relación con Borrelia burgdorferi) se observa un aumento de la actividad de Nagalasa y parece ser que la nagalasa se comporta como antagonista de la vitamina D activa. (1-25-dihidroxi vitamina D).
También sabemos que la bacteria Prevotella spp. (germen oportunista en flora bucal) se ha asociado frecuentemente con covid-grave: (1)
Por otra parte, sabemos que los pesticidas y herbicidas contienen sustancias que se comportan como lipoxinas, es decir, como citocinas depresoras del sistema inmune, y que las personas con obesidad sufren una covid más grave. Como los pesticidas son liposolubles y se acumulan en el tejido adiposo, ésta puede ser una razón de dicha susceptibilidad.
COVID grave
Todo el problema de la covid-19 es con mucha probabilidad un problema de inmunodeficiencia que puede estar inducido por sucesivas vacunaciones debido a infección por gamma-retrovirus contaminantes de dichas vacunas, como ha dicho la viróloga norteamericana Judy Mikovits, o por desregulación de los gamma retrovirus endógenos como pensamos nosotros. Así, cuando la persona sufre un proceso gripal se puede producir un síndrome de ADE o similar (patología TH2) con inflamación sistémica, tormenta de citocinas y daño endotelial: trombosis y acúmulo de NETS, esto es la covid-19 grave.
Dra. María José Martínez Albarracín,
Asociación positiva entre las muertes por COVID-19 y la vacuna contra la influenza link al video , comparta por favor, https://www.bitchute.com/video/IJWLfHhSRHkh/
Según declaraciones a la prensa del inmunólogo Ignacio Melero (Univ. Navarra) la covid-19 grave es una reacción inflamatoria:
«Esta reacción inflamatoria se sabe que está detrás de la muerte de muchos pacientes… Lo que llamamos distrés respiratorio del adulto (SARS) lo precipitan muchos tipos de enfermedades, como la sepsis bacteriana o la pancreatitis aguda o estar en un incendio e inhalar humos tóxicos»,
Inmunólogo Ignacio Melero (Univ. Navarra)
«Empezamos a tener una foto muy precisa de los mecanismos que provocan la destrucción de tejido y perpetúan y aumentan esa reacción inflamatoria». «Otra cosa que sabemos es que algunas de las citocinas que liberan los macrófagos están entre los mejores inductores de NETs en las otras células».»Nosotros nos estamos centrando mucho en una citocina que se llama interleucina-8″.
«Desde que tenemos los datos preliminares de la netosis, hay una enzima llamada PAD4 que es absolutamente necesaria para que ocurra esta liberación de los NETs que, en principio, se produce para defendernos de bacterias y hongos». (Esta proteína PAD4 parece desempeñar un papel en el desarrollo de granulocitos y macrófagos que conduce a la inflamación y respuesta inmune).
Correlación entre la covid grave con la vacunación antigripal previa
Publicaciones científicas (2) y otros estudios: COVID-19 severity in Europe and the USA: Could the seasonal influenza vaccination play a role? EBMPHET Consortium1,* Hospital de Barbastro (Huesca): Hipótesis: Posible interferencia inmunológica entre el Polisorbato 80 de la vacuna antigripal adyuvada y el Sars-CoV-2 como causa de la pandemia por coronavirus, o los del biólogo Bartomeu Payeras, correlacionan significativamente la covid grave con la vacunación antigripal previa, por lo que hay fundadas sospechas de que las vacunas de la gripe han podido desencadenar un síndrome tipo ADE o ENFERMEDAD AUMENTADA POR VACUNA, porque contuvieran péptidos inmunosupresores como la nagalasa: Alfa-N-Acetilgalactosaminidasa, que también es una enzima que producen las células cancerosas.
Sobre la Nagalasa
En 1991, el bioquímico japonés Nobuto Yamamoto proclamó que había encontrado un activador de macrófagos con extensas propiedades inmunomoduladoras. Más tarde sus utilidades terapéuticas se extenderían supuestamente a numerosas patologías:
- autismo,
- infección por VIH o
- cáncer.
La Vitamin D-binding protein (DBP o proteína transportadora de vitamina D), también conocida como globulina Gc, es una proteína naturalmente promovida por los linfocitos T y B, perteneciente a la familia de las albúminas, que se asocia a la vitamina D y se encarga de llevarla a los tejidos.
Yamamoto proponía que una de estas globulinas gc podía transformarse, tras desglicosilación en las células, en una MAF, o proteína activadora de macrófagos, cambiando el perfil de dichos macrófagos de M2 a M1. La DBP se considera ya, hay bastantes estudios al respecto (3), como una proteína multifuncional de gran importancia clínica que, entre otras funciones, puede modular la respuesta inmune e inflamatoria.
La nagalasa desglicosila la proteína gc (DBP), que de esta forma ya no puede convertirse en un factor activador de macrófagos (MAF) e induce una potente inmunosupresión. De hecho Yamamoto publicó un trabajo que relacionaba la inefectividad del sistema inmune ante las infecciones con la enzima Nagalasa: (4)
Pathogenic significance of alpha-N-acetylgalactosaminidase activity found in the envelope glycoprotein gp160 of human immunodeficiency virus Type 1. Es un artículo demoledor cuyo resumen dice lo siguiente:
La proteína de unión a vitamina D3 (proteína Gc) sérica es la precursora del principal factor activador de macrófagos (MAF). La actividad precursora de la proteína Gc sérica se perdió o se redujo en pacientes infectados por VIH. Estos sueros de pacientes contenían alfa-N-acetilgalactosaminidasa (Nagalasa) que desglicosila la proteína Gc del suero. La proteína Gc desglicosilada no se puede convertir en MAF,y, por tanto, pierde la actividad precursora de MAF, lo que conduce a inmunosupresión.
La nagalasa en el torrente sanguíneo de los pacientes infectados por el VIH se unió complementariamente con IgG del paciente, lo que sugiere que esta enzima es inmunogénica, aparentemente un producto génico viral. De hecho, nagalasa fue inducible mediante el tratamiento de cultivos de células mononucleares de sangre periférica de pacientes infectados por VIH con un agente inductor de provirus. Esta enzima fue inmunoprecipitable con suero anti VIH policlonal pero no antienzima constitutiva celular ni antinagalasa tumoral. Los parámetros cinéticos (valor de km de 1,27 mM y pH óptimo de 6,1) de la nagalasa en suero del paciente eran distintos de los de la enzima constitutiva (valor de km de 4,83 y pH óptimo de 4,3).
Esta glicosilasa (nagalasa) debería residir en una proteína de la envoltura vírica capaz de interactuar con los O-glicanos de la membrana celular. Aunque la gp 160 clonada no mostró actividad de nagalasa, el tratamiento de gp160 con tripsina expresó actividad de nagalasa, lo que sugiere que se requiere la escisión proteolítica de gp160 para generar gp120 y gp41 para la actividad de nagalasa. La gp120 clonada mostró actividad de nagalasa mientras que la gp41 no mostró actividad nagalasa.
Dado que la escisión proteolítica de la proteína gp160 es necesaria para la expresión tanto de la capacidad de fusión como de la actividad nagalasa, nagalasa parece ser una base enzimática para la fusión en el proceso infeccioso. Por tanto, nagalasa parece desempeñar un papel doble en la infectividad viral y la inmunosupresión.
Adicionalmente, nagalasa parece estar involucrada en los procesos de degradación de la matriz extracelular que acompañan la invasión de las neoplasias malignas.
Es de destacar también que la DBP aumenta en el suero por los estrógenos (hormonas sexuales femeninas) pero no por andrógenos (hormonas sexuales masculinas) lo que explicaría que los varones suelen sufrir una covid más grave. También disminuye la expresión de DBP en los diabéticos. (5)
Es importante hacer un inciso respecto a inmunosupresión por nagalasa ya que las vacunas para covid-19 se basan todas ellas de una manera u otra en la Spike protein del Sars-CoV-2. Siendo además su dominio más antigénico la subunidad de fusión (S2) .
Dicha subunidad de fusión de la proteína espiga, según la secuencia que se ha difundido, contiene cuatro inserciones peptídicas que se corresponden con la proteína gp120 con actividad nagalasa, según demostraron los autores del estudio del Instituto de Tecnología de India (6) que fue retirado rápidamente por presiones políticas pero que fue confirmado por el Virólogo Luc Montaigner, premio Nobel por descubrir precisamente el VIH.
Finalmente resaltar que la actividad nagalasa también se ha comprobado en los sueros de los pacientes infectados con virus de la gripe (influenza) y que reside en la actividad hemaglutinante de dichos virus. Es decir que la nagalasa es un componente intrínseco de la hemaglutinina (HA) de los virus de la gripe, y es precisamente el antígeno HA uno de los que se utiliza para fabricar las vacunas antigripales (7).
Otro modo en que las vacunas antigripales pudieron haber ocasionado un síndrome de tipo ADE es porque sus antígenos sintéticos hayan producido anticuerpos aglutinantes pero no neutralizantes.
Cuando la persona enferma de gripe o catarro, sea por contagio o por reacción inflamatoria a su propia carga tóxica, elimina virus endógenos, entonces los anticuerpos no neutralizantes, por reacción cruzada, pueden desencadenar el síndrome de ADE.
María José Martinez Albarracín
Sars-CoV-2 no es la única causa
¿Qué fue lo que pasó en primavera en España y otros países? Si el síndrome Covid-19 hubiera estado provocado exclusivamente por un virus, sea el Sars-CoV-2 u otro, se habría manifestado de la misma manera en primavera, en verano y en otoño, ¿por qué no ocurrió así?. Evidentemente porque el Sars-CoV-2 no era la causa, o al menos no era la única causa.
Otros factores que se han relacionados con la covid-19, además de la vacunación antigripal previa, son las REM, especialmente de tipo 5G y otros tóxicos ambientales que se comportan como favorecedores o desencadenantes de inflamación y, por tanto, inmunoalteradores, especialmente como depresores de la inmunidad celular.
Se discute el papel de las microondas como factor que interfiere con el proceso de inmunidad celular (8)
Expliquemos el síndrome de ADE (Antibody dependent enhancement) (9) (10)
En el SINDROME de ADE, los anticuerpos facilitan la entrada de virus en las células inmunes de la serie mieloide (macrófagos, y células dendríticas), en vez de producirse la presentación normal del antígeno. Estos virus enteros en el macrófago inhiben la producción de interferón, a través de diversos mecanismos, con lo que disminuye la respuesta inmune innata contra los virus a la vez que éstos se multiplican dentro de la célula. Cuando los nuevos virus salen al exterior del macrófago, aumenta la infección. Los linfocitos activados producen una gran cantidad de citocinas y quimiocinas desencadenando lo que se conoce como “tormenta de citocinas”. Los neutrófilos acuden a las zonas inflamadas para realizar la fagocitosis pero al estar cubiertos de partículas víricas son atacados por linfocitos citotóxicos y células NK y mueren produciéndose en dichas zonas inflamadas acúmulo de NETS (redes de material nuclear de los neutrófilos apoptóticos).
Teóricamente, la mejora inmunológica de la enfermedad puede ocurrir de dos maneras:
- En primer lugar, los niveles de anticuerpos no neutralizantes o subneutralizantes pueden potenciar la infección por SARS-CoV-2, otros coronavirus, o virus influenza en las células diana.
- En segundo lugar, los anticuerpos podrían potenciar la inflamación y, por tanto, la gravedad de la enfermedad pulmonar (11). Una descripción general de estas infecciones dependientes de anticuerpos y los efectos de mejora de la inmunopatología se resumen en la siguiente figura:
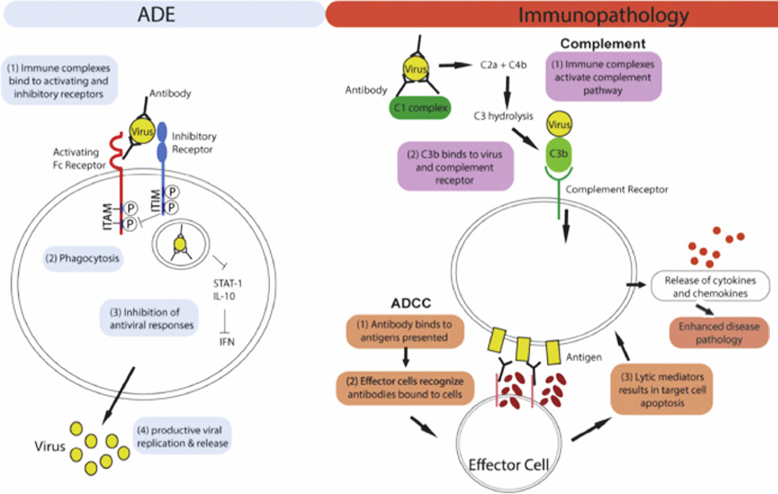
Un caso conocido de ADE se produce en el Dengue (12) (13)
Las células presentadoras (macrófagos, monocitos y dendríticas) se activan a través de receptor TLR2 /MyD 88 y activan respuesta TH2 (CD4) con aumento de IL 4,5,6,10 y 13 contribuyendo así a una actividad inflamatoria e inmunodepresora (supresión perfil Th1 y activación perfil Th2) contraria a la eliminación del virus y propicia al daño endotelial, mientras que la elevación de interferón-gamma e interleucina 2 (PERFIL Th1) es beneficiosa.
En el ADE INTRÍNSECO se produce un apagamiento de la inmunidad innata proporcional al aumento de partículas virales y la disminución de la expresión de receptores TOLL (TLRs). De esta manera, la unión de los complejos inmunes a células dendríticas y monociticas disminuye la transcripción de TLRs y aumenta la de SARM y TANK (proteínas que inhiben la expresión de TLRs) en células monocíticas generando un círculo vicioso de replicación viral y estimulación inmune (citocinas).
La supresión de los TLRs conlleva la disminución de la expresión de interferón de tipo I lo cual es crucial para favorecer la replicación viral y el daño endotelial por supresión de la producción de óxido nítrico (potente vasodilatador y antivírico).
En la covid-19 grave hemos visto, gracias a las autopsias, que los endotelios vasculares están dañados y en ellos se han encontrados estos NETs. ¿Son acaso las células endoteliales susceptibles a un determinado virus? ¿Tienen los receptores necesarios para facilitar la entrada en dichas células endoteliales de un determinado virus como el Sars-CoV-2? ¿Por qué los endotelios pulmonares han sido los inicialmente atacados produciéndose la característica neumonía intersticial bilateral?
En primer lugar el receptor ACE2 no se expresa (o apenas lo hace) en células pulmonares y de vías respiratorias, según el artículo revisado por pares (14):
El perfil de expresión de la proteína ACE2 en los tejidos humanos (The protein expression profile of ACE2 in human tissues)
Por esta razón, el supuesto virus Sars-CoV-2, si tiene como receptor a ACE2, no podría dañar directamente el aparato respiratorio, aunque el receptor sí parece expresarse en los pericitos microvasculares de algunos órganos como el corazón.
En la covid-19 grave se ha visto, además del acúmulo de NETs en vasos sanguíneos, alta expresión de Interleuquina 8, citoquina producida por macrófagos y células endoteliales. Su acción principal es proinflamatoria y angiogénica. Es un potente factor quimiotáctico de neutrófilos, en los que induce la expresión de integrinas, favoreciendo su adhesión a células endoteliales.
Otra cuestión que favorecería el daño endotelial es la circulación de tóxicos liposolubles por vía sanguínea, ya que estos atacan las membranas celulares. Pues bien, científicos del hospital de Barbastro respondieron esta cuestión:
Emulsionantes de tipo detergente contenidos en las vacunas de la gripe
Emulsionantes de tipo detergente contenidos en las vacunas de la gripe estacional como Chiromas, cuyo adyuvante MF59C.1 contiene polisorbato-80 y sorbitol trioleato, en una cantidad considerablemente alta (1,175 mg) o Fluzone que contiene triton-100, resultan tóxicos para las células endoteliales al dañar sus membranas y desactivar las C-lectinas que suponen una defensa innata de dichas células contra la invasión de virus. Por tanto, la posible entrada de virus o simplemente ”virus like particles” (antígenos virales contenidos en las vacunas) en células endoteliales de aquellos órganos con mayor red vascular como el pulmón, pudieron ir facilitando un fenómeno inmune de tipo ADE que se desencadenó ante un contagio con virus similares, es decir, los virus de la gripe que circulan todas las temporadas invernales.
Este fenómeno de ADE pudo, a su vez, estar facilitado si las vacunas antigripales contenían algún tipo de péptido con capacidad inmunosupresora así como en aquellas personas que tuvieran en sus organismos cierto acúmulo de tóxicos con capacidad de inmunodepresión. A este respecto es de notar que la Covid-19 grave se produjo con mayor frecuencia en personas con obesidad, incluso jóvenes como ya hemos explicado y es bien sabido que los tejidos adiposos acumulan tóxicos provenientes, en su mayor parte, de los pesticidas y herbicidas que son liposolubles y se comportan como análogos de las Lipoxinas (citocinas con función inmunodepresora).
Por otra parte hay que destacar que ADE también puede ser producido o facilitado por el antígeno HA (hemaglutinina) de las vacunas antigripales:
En el estudio citado a continuación (15), el análisis de citometría de flujo mostró que el mecanismo de entrada del virus en macrófagos de ratones podría ser a través de HA a receptores de virus específicos, o HA más anticuerpo a través de receptores Fc. Estos resultados indican que el ADE de la infección por el virus NWS (influenza A murina) se produce realmente en macrófago murino primario portador del receptor Fc, dependiendo de la concentración de anticuerpo en presencia de la proteasa apropiada para la escisión de HA viral:
Aumento de la infección del virus influenza A NWS en macrófagos murinos primarios por anticuerpo monoclonal anti-hemaglutinina
El ADE comienza cuando el virus unido al anticuerpo se une a los receptores Fc activadores para iniciar la endocitosis o fagocitosis mediada por el receptor Fc. Este proceso facilita la entrada del virus en los monocitos, macrófagos y células dendríticas que expresan el receptor Fc. Sin embargo, la unión a los receptores Fc activadores sola es insuficiente para ADE. Esto se debe a que la activación de los receptores Fc desencadena la producción de moléculas de señalización que también inducen la expresión del gen estimulado por interferón (IFN) (ISG), independiente del IFN de tipo I .
Se han observado reinfecciones con CoV humanos y no hay ningún informe de que la infección secuencial sea más grave que la infección primaria. Del mismo modo, tampoco hay pruebas que sugieran que la gravedad del SARS o del MERS esté relacionada con los anticuerpos CoV con reactividad cruzada basal, por lo tanto es necesario que confluyan otros factores causales de inmunodepresión.
El apoyo clínico para la inmunopatología mediada por anticuerpos proviene de la observación de que el SARS grave se manifestó en la semana 3 de la enfermedad, en un momento en que la carga viral del tracto respiratorio estaba disminuyendo debido al aumento de los títulos de anticuerpos (16) .
Además, Ho y sus colegas observaron que los pacientes con SRAS que desarrollan respuestas de anticuerpos en la segunda semana de enfermedad tienen más probabilidades de desarrollar una enfermedad grave en comparación con los que desarrollan anticuerpos en la tercera semana de enfermedad o más tarde (17).
Se estableció un vínculo más directo entre los anticuerpos y la enfermedad en los macacos rhesus chinos, cuando los anticuerpos específicos del SARS-CoV después de la vacunación indujeron una patología pulmonar grave en comparación con los animales no vacunados tras la exposición viral (18)
El ADE o EAM de la infección puede producirse in vitro para muchos virus diferentes, incluido el virus de la inmunodeficiencia humana (19), la gripe o influenza (15) y los virus del Ébola (20). De manera similar, el ADE in vitro de virus de tipo salvaje y virus de pseudotipo, en células derivadas de mieloides que expresan el receptor Fc en presencia de concentraciones subneutralizantes de Ac. de sueros inmunes, también se ha descrito para SARS-CoV y MERS-CoV (21). En el caso de los CoV, se ha demostrado que los anticuerpos pueden unirse a la proteína del pico de superficie exponiendo el virus a la activación proteolítica y la entrada mediada por el receptor Fc (21).
Por otra parte sabemos que la vacunación también puede ocasionar ADE: la vacuna quimérica tetravalente contra el dengue (Dengvaxia) es un ejemplo de ello (22). Otros dos ejemplos notables de enfermedad amplificada inducida por vacuna son el virus respiratorio sincitial (VSR) (23) (24) (25) (26) y el sarampión atípico (27) (28) donde la enfermedad grave fue más prevalente después de la vacunación con viriones inactivados.
El mecanismo exacto de la inmunopatología potenciada por anticuerpos en los modelos de infección por CoV no se comprende bien. Sin embargo, las vacunas contra virus como el VSR mostraron una inmunopatología mejorada similar después de la vacunación. Se ha postulado que las vías efectoras mediadas por anticuerpos son la causa de la inmunopatología mejorada (24) . Además de unirse al antígeno y activar la endocitosis o fagocitosis mediada por el receptor de Fc, los anticuerpos también provocan una serie de respuestas mediadas por Fc, a saber, la activación del complemento y la citotoxicidad celular dependiente de anticuerpos (ADCC).
Sin embargo, una respuesta efectora mediada por Fc aberrante y sobreestimulada también puede conducir a una inmunopatología grave y daños (29) (30). Por ejemplo, un estudio observó que el anticuerpo IgG anti-proteína Spike de pacientes con SARS grave de macacos Rhesus, inmunizados con una vacuna CoV contra el SARS, vectorizada por vacuna de Ankara modificada, condujo a la producción de citocinas proinflamatorias y al reclutamiento de macrófagos inflamatorios en el parénquima pulmonar (18).
También se ha comprobado en ratones que los animales más viejos tienden a responder mal a la vacunación (31) (32).
Las enfermedades autoinmunes suponen una respuesta inflamatoria amplificada y desregulada.
Respecto a este punto es de notar que las vacunaciones excesivas y prematuras en la vida de un individuo predisponen al desarrollo de un perfil inmunitario Th2 (inmunidad humoral y adquirida) en detrimento del perfil Th1 que es el que prevalece en la inmunidad innata y celular. Es conveniente reflexionar sobre la importancia y función de dichos perfiles inmunológicos.
Cualquier infección vírica se desarrolla en el contexto de nuestro viroma, es decir que, aunque una persona pueda sufrir un contagio vírico por “resonancia” con el individuo enfermo (recordemos que toda persona expuesta a virus no sufre un contagio y que éste depende del estado inmune basal del posible receptor) el proceso infeccioso cursará con expresión o activación de sus propios virus endógenos. Cuando esto ocurre, la señalización vírica marca o “infecta” células dañadas o intoxicadas de manera que no están cumpliendo adecuadamente sus funciones. El perfil de inmunidad Th1 favorecerá la muerte de dichas células y la fagocitosis de los detritus orgánicos produciéndose, a continuación, la renovación celular y la reparación del tejido dañado por la infección.
En el caso de una vacunación, lo que ocurre es que la expresión incompleta de antígenos víricos, desencadena principalmente una respuesta humoral con producción de anticuerpos, es decir, expresión principal del perfil inmune Th2, este perfil es proinflamatorio, provocando una inflamación de bajo grado que puede ser atenuada pero que no es “resolutoria” de ninguna situación tóxica o alterada que hubiera podido desencadenar la infección viral.
Por otra parte, la producción mantenida de Ac contra Ag víricos que son compatibles con Ag expresados por retrovirus endógenos, puede dar lugar a fenómenos autoinmunes o al mantenimiento de un perfil inflamatorio crónico de bajo grado que favorezca la ADE o síndromes similares como el Síndrome hemofagocítico.
Covid-19 como un proceso autoinmune
Es absurdo decir que un mismo virus puede producir cuadros clínicos tan diversos como la ausencia de síntomas:
- el resfriado leve,
- la neumonía intersticial bilateral y
- la vasculitis multiorgánica con tormenta de citoquinas aguda y mortal.
Si se producen estas enormes diferencias clínicas es debido al paciente, a su estado inmunológico, no al virus. Por lo tanto urge estudiar qué determina dicho estado inmune.
Por otra parte, se ha visto en las autopsias que lo que se encuentra en los vasos sanguíneos dañados (pues la covid grave es básicamente una vasculitis) es un gran acúmulo de NETs o trampas extracelulares de macrófagos y éstas son características del Lupus Eritematoso Diseminado, enfermedad autoinmune por excelencia y que además de no ser transmisible puede ser ocasionada por reacciones vacunales y diversos químicos tóxicos. Por cierto, el Lupus se trata también con hidroxicloroquina. Otros factores que apoyan la autoinmunidad son el aumento de interleucina 8 y los anticuerpos antiinterferón encontrados en los enfermos de covid grave.
Según un artículo publicado en Science a finales de septiembre:
Bastard y col. identificaron individuos con títulos altos de autoanticuerpos neutralizantes contra IFN-α2 e IFN-ω tipo I en aproximadamente el 10% de los pacientes con neumonía grave por COVID-19. Estos autoanticuerpos no se encontraron ni en personas infectadas que eran asintomáticas, ni en individuos sanos.
La coautora Isabelle Meyts, inmunóloga pediátrica de los Hospitales Universitarios de Lovaina dice:
Nunca ha habido una enfermedad infecciosa explicada a este nivel por un factor en el cuerpo humano. Y no es una cohorte aislada de europeos. Los pacientes son de todo el mundo, de todas las etnias .
Isabelle Meyts, inmunóloga pediátrica de los Hospitales Universitarios de Lovaina
Otro hallazgo es que el 94% de los pacientes con anticuerpos que atacan al interferón eran hombres, lo que ayuda a explicar por qué los hombres tienen un mayor riesgo de enfermedad grave.
En un estudio, Jean-Laurent Casanova, genetista de enfermedades infecciosas de la Universidad Rockefeller, y su equipo concluyen que “Al menos el 10% del COVID-19 crítico es un ataque autoinmune.”
Los AC ANTIINTERFERÓN (33) suponen un trastorno de inmunodeficiencia adquirida poco frecuente, caracterizado por la aparición de susceptibilidad a infecciones oportunistas diseminadas (en particular, infección micobacteriana no tuberculosa diseminada, salmonelosis, peniciliosis e infección por el virus de la varicela zoster) en adultos previamente sanos (VIH negativos). Está asociada a la presencia de autoanticuerpos anti-interferón gamma adquiridos. Los hallazgos clínicos característicos incluyen linfadenopatía (cervical o generalizada), fiebre, pérdida de peso y/o lesiones cutáneas reactivas.
En relación con la deficiencia adquirida de interferón es importante destacar su relación con los HERVs (retrovirus endógenos humanos) (34).
Los retrovirus endógenos (ERV) son abundantes en los genomas de mamíferos y contienen secuencias que modulan la transcripción. El impacto de la propagación de ERV en la evolución de la regulación genética sigue siendo poco conocido. Los ERV han dado forma a la evolución de una red transcripcional subyacente a la respuesta de interferón (IFN), una rama importante de la inmunidad innata, y los ERV específicos de linaje han dispersado numerosos potenciadores inducibles por IFN de forma independiente en diversos genomas de mamíferos.
Aunque estas secuencias reguladoras probablemente surgieron de virus antiguos, ahora constituyen un depósito dinámico de potenciadores inducibles por IFN que alimentan la innovación genética en las defensas inmunitarias de los mamíferos.
La prevalencia de potenciadores inducibles por IFN en los LTR de estos antiguos retrovirus no es una coincidencia, sino que puede reflejar adaptaciones virales anteriores para explotar las vías de señalización inmunitaria que promueven la transcripción y replicación viral . De hecho, varios virus existentes, incluido el VIH, poseen elementos reguladores cis inducibles por IFN.
A este respecto recordar la secuencia peptídica del VIH encontrada en la spike protein del Sars-CoV-2 y estudiada en el artículo citado: Uncanny similarity of unique insert in the 2019-nCoV spike protein to HIV-1 Gp 120 and Gag (Pashant Pradham et alt.) De la que también se hizo eco el Premio Nobel Luc Montaigner.
Síndromes hemofagociticos
Otro tipo de fenómenos y síndromes clínicos relacionados con la covid-19 grave y que pueden guardar estrecha relación con la autoinmunidad son los llamados síndromes hemofagocíticos.
El síndrome hemofagocítico (SHF) o linfohistiocitosis hemofagocítica es una entidad clínica con elevada mortalidad, típicamente reconocida en la edad pediátrica, sin un correcto tratamiento puede ser fatal: el riesgo de una rápida progresión a fallo multiorgánico y de afectación del sistema nervioso central con secuelas a largo plazo son las consecuencia más graves de un retraso diagnóstico (35) (36).
Los síntomas iniciales suelen ser fiebre y afectación progresiva del estado general y el factor desencadenante puede ser infeccioso, oncológico, autoinmune o metabólico.
Los síndromes hemofagocíticos (SPH) son afecciones raras que ponen en peligro la vida y se caracterizan por una sobreestimulación del sistema inmunológico que conduce a inflamación sistémica, hipercitocinemia e insuficiencia multiorgánica. Se dividen a grandes rasgos en linfohistiocitosis hemofagocítica primaria (HLH) y síndromes hemofagocíticos secundarios..
La HLH primaria es causada por mutaciones genéticas que alteran la función citotóxica de los linfocitos T citotóxicos y asesinos naturales (NK) y , por lo general, están presentes en la infancia y la niñez. HLH primario incluye HLH familiar (fHLH), donde los pacientes tienen mutaciones autosómicas recesivas en diversos genes (Perforin(PRF1), MUNC 13-4 (UNC13D), MUNC 19-2 (STXBP2) y sintaxina 11 (STX11).
La HLH primaria también incluye otros síndromes de inmunodeficiencia hereditaria como el síndrome de Chédiak-Higashi , el síndrome de Griscelli y el síndrome de Hermansky-Pudlak tipo II.
Los síndromes hemofagocíticos secundarios generalmente afectan a adolescentes y adultos y no están asociados con defectos genéticos conocidos, aunque se han informado casos raros de fHLH después de los 70 años
Síndrome hemofagocitico secundario
En el SPH secundario o reactivo, a menudo hay una «condición predisponente» asociada que causa una desregulación inmunológica , como una neoplasia maligna (en particular linfoma), inmunodeficiencia o enfermedad autoinmune, y / o un «desencadenante», más comúnmente una infección como la del virus de Epstein-Barr. En algunos casos, no se identifica un proceso patológico asociado (37).
El SPH también puede denominarse síndrome de activación de macrófagos (MAS) cuando se presenta en pacientes con enfermedades autoinmunitarias como artritis idiopática juvenil , enfermedad de Still del adulto y lupus eritematoso sistémico (38). La activación inmunitaria patológica que caracteriza a HPS / HLH puede ser difícil de distinguir de la activación fisiológica de macrófagos. Por ejemplo, ni la presencia ni la cantidad de hemofagocitosis en las biopsias de médula ósea son específicas de HPS / HLH.
Conclusiones:
1.- La covid-19 grave como síndrome de inmunidad alterada.
2.- Puede, en todo caso, estar desencadenada por una infección vírica en determinadas circunstancias.
3.- En casos de covid-grave pueden que ocurran determinadas situaciones fisiopatológicas e inmunopatológicas previas que pueden haber sido propiciadas por vacunaciones anteriores, especialmente la vacunación antigripal.
4.- Igualmente, determinadas condiciones metabólicas como diabetes, obesidad, y deficiencias de vitamina D activa, son determinantes en la Covid-19.
4.- Síndrome Hemofagocitico o de Enfermedad Aumentada por la Vacuna antigripal.
5.- Otros factores coadyuvantes serían aquellos capaces de inducir inmunodepresión, especialmente linfopenia, como es el caso de la exposición a REM especialmente las de alta potencia como la 5G y la proximidad a antenas emisoras, los pesticidas y herbicidas, metales pesados y otros tóxicos ambientales.
ver más:
Referencias:
1.-Las proteínas Prevotella sobreexpresadas asociadas a COVID-2019 mediadas por interacciones huésped-patógeno y su papel en el brote de coronavirus.
Abdul Arif Khan, Zakir Khan (Bioinformatics 2020)
2.- Asociación positiva entre las muertes por COVID-19 y las tasas de vacunación contra la influenza en las personas mayores en todo el mundo
Christian Wehenkel (Peer journal, 2020)
3.- Vitamin D binding protein: a multifunctional protein of clinical importance. Marijn M Speeckaert et alt.( Epub 2005).
4.- Pathogenic significance of alpha-N-acetylgalactosaminidase activity found in the envelope glycoprotein gp160 of human immunodeficiency virus Type 1 Nobuto Yamamoto (Pub Med, 2006)
5.- Vitamin D Binding Protein: A Historic Overview Roger Bouillon (Front. Endocrinol. 2020)
6.- Uncanny similarity of unique inserts in the 2019-nCoV spike protein to HIV-1 gp120 and gag. Prashant Pradhan et alt. (BioRXiv, preprint. 2020)
7.- Pathogenic significance of alpha-N-acetylgalactosaminidase activity found in the hemagglutinin of influenza virus Nobuto Yamamoto , Masahiro Urade (Microbes and Infection, 2005)
8.-Microwaves and cellular immunity: I. Effect of whole body microwave irradiation on tumor necrosis factor production in mouse cells.
E.E Fesenko (Bioelectrochemistry and Bioenergetics, 1999)
9.- Molecular mechanism for antibody-dependent enhancement of coronavirus entry.
Wan Y.( J Virol. 2020)
10.- Antibody-dependent enhancement of SARS coronavirus infection and its role in the pathogenesis of SARS.
Yip M.S.(Hong Kong Med J. 2016)
11.-Is antibody-dependent enhancement playing a role in COVID-19 pathogenesis?
Negro Francesco( Swiss Med Wkly. 2020)
12.- Antibody- dependent enhancement in the inmunopathogenesis of severe dengue, implications for the development and use of vaccines.
B. Alejandro Cácers Munar et alt. (Acta Colombiana 2019)
13.- Dengue viruses and mononuclear phagocytes. I. Infection enhancement by non-neutralizing antibody. S B Halstead, E J O’Rourke (Pub Med 1977)
14.- The protein expression profile of ACE2 in human tissues. Feria Hikmet et alt. (Mol. Syst. Biol. 2020)
15.- Infection enhancement of influenza a NWS virus in primary murine macrophages by anti-hemagglutinin monoclonal antibody. Ochiai H. et alt. (J Med Virol. 1992)
16.- Clinical progression and viral load in a community outbreak of coronavirus-associated SARS pneumonia: a prospective study.
Peiris J.S. et alt Lancet. 2003
17.- Neutralizing antibody response and SARS severity.
Ho M.S. et alt. (Emerg Infect Dis. 2005)
18.- Anti-spike IgG causes severe acute lung injury by skewing macrophage responses during acute SARS-CoV infection.
Liu L. et alt (JCI Insight. 2019)
19.- Antibody-dependent enhancement of human immunodeficiency virus type 1 infection.
Robinson J.R. et alt. (Lancet. 1988)
20.- Infectivity-enhancing antibodies to Ebola virus glycoprotein.
Takada A. et alt. (J Virol. 2001)
21.-Antibody-dependent sars coronavirus infection is mediated by antibodies against spike proteins. Wang S.F. et alt.(Biochem Biophys Res Commun. 2014)
22.- Effect of dengue serostatus on dengue vaccine safety and efficacy.
Sridhar S. et alt (N Engl J Med. 2018)
23.- An epidemiologic study of altered clinical reactivity to respiratory syncytial (RS) virus infection in children previously vaccinated with an inactivated RS virus vaccine.
Kapikian A.Z. et alt (Am J Epidemiol. 1969)
24.- Respiratory syncytial virus disease in infants despite prior administration of antigenic inactivated vaccine.
Kim H.W.( Am J Epidemiol. 1969)
25.- Respiratory virus immunization. I. A field trial of two inactivated respiratory virus vaccines; an aqueous trivalent parainfluenza virus vaccine and an alum-precipitated respiratory syncytial virus vaccine.
Fulginiti V.A. et alt. (Am J Epidemiol. 1969)
26.- Field evaluation of a respiratory syncytial virus vaccine and a trivalent parainfluenza virus vaccine in a pediatric population.
Chin J. et alt. (Am J Epidemiol. 1969)
27.- Immunoglobulin g antibody-mediated enhancement of measles virus infection can bypass the protective antiviral immune response.
Iankov I.D. et alt (J Virol. 2006)
28.- Measles immunization with killed virus vaccine. Serum antibody titers and experience with exposure to measles epidemic.
Raug L.W. et alt.(Am J Dis Child. 1965)
29.- Fc-Mediated antibody effector functions during respiratory syncytial virus infection and disease.
Van ERP E.A. et alt. (Front Immunol. 2019)
30.- Antibody-mediated complement activation in pathology and protection.
Goldberg B.S. et alt. (Immunol Cell Biol. 2020)
31.- A double-inactivated severe acute respiratory syndrome coronavirus vaccine provides incomplete protection in mice and induces increased eosinophilic proinflammatory pulmonary response upon challenge.
Bolles M. (J Virol. 2011)
32.- Vaccine efficacy in senescent mice challenged with recombinant SARS-CoV bearing epidemic and zoonotic spike variants.
Deming D. et alt. (PLoS Med. 2006)
33.- Sars-CoV-2 ORF3b is a potent interferon antagonist whose activity is further increased by a naturally occurring elongation variant.
Yoriyuki Konno et alt. (Cell reports 2020)
34.- Regulatory evolution of innate immunity through co-option of endogenous retroviruses.
Edward B. Chuong et alt.(Science 2016)
35.- Sindromes hemofagocíticos: La importancia del diagnostico y tratamiento precoces.
Itziar Astigarraga et alt. (Anales de pediatría 2018)
36.- Hemophagocytic síndromes (HPSs) including hemophagocytic lymphohistiocytosis (HLH) in adults: A systematic scoping review.
Anna Hayden et alt.(Elsevier, 2016)
37.- Diagnostic and therapeutics guidelines for hemophagocytic lymphohistiocytosis.
Henter J. et alt.(Pediatr. Blood Cancer, 2007)
38.- Hemophagocytic syndrome in patiens with systemic autoimmune diseases: analysis of 30 cases.
Fukaya S. et alt (Rheumatology, 2008)