Recopilado por: Dra. Liliana Szabó (Médica pediatra y homeópata) Fecha de recopilación de datos: Setiembre de 2020. (Basado en datos extraídos del Ministerio de Salud Pública, en los prospectos de las vacunas existentes actualmente en la Argentina y en la bibliografía científica internacional)
Dra. Liliana Szabo, Por una Libre Elección de Vacunas Auditorio del Anexo A de la Cámara de Diputados, Argentina, 27 de Noviembre 2025 – https://www.bitchute.com/video/UCKxxnKMQJrn
CALENDARIO NACIONAL OFICIAL DE VACUNAS EN ARGENTINA: UN INFORME ANALÍTICO
TOTAL DE INYECCIONES APLICADAS APROXIMADAMENTE HASTA LOS 15 AÑOS: 42 (esta cifra es variable según se agreguen campañas de revacunación a los ya vacunados) mas 6 vacunas orales.
TOTAL DE ANTÍGENOS INOCULADOS APROXIMADAMENTE HASTA LOS 15 AÑOS: 160
Nota aclaratoria: se denomina antígeno a toda sustancia capaz de provocar al sistema inmunológico para que fabrique anticuerpos contra dicha sustancia. En este análisis (TABLA I) solo se contabilizan los antígenos que forman parte de la vacuna propiamente dicha, o sea del virus o bacteria contra la cual es fabricada la vacuna. Es bueno aclarar que hay muchos otros antígenos contenidos en las vacunas que figuran en los prospectos (proteínas y material genético ajeno entre otros).
TABLA I-
Cantidad de inoculaciones y antígenos virales y bacterianos por edad hasta 15 años
| EDAD | INOCULACIONES | ANTÍGENOS | ACLARACIONES |
| Recién nacido | 2 | 2 | |
| 2 meses | 2 más 2 orales | 20 | |
| 3 meses | 1 o 2 | 4 u 8 | Según se apliquen 1 o 2 vacunas para meningococo |
| 4 meses | 2 más 2 orales | 20 | |
| 5 meses | 1 o 2 | 4 u 8 | Según se apliquen 1 o 2 vacunas para meningococo |
| 6 meses | 2 más una 1 oral | 10 | Incluye dosis anual de antigripal |
| 12 meses | 3 | 17 | |
| 15 meses | 2 o 3 | 5 o 9 | Según se apliquen 1 o 2 vacunas para meningococo |
| 18 meses | 2 | 9 | Incluye dosis anual de antigripal |
| 2, 3, 4 y 5 años | 1 por año | 4 x año (=16) | Antigripal anual |
| 6 años | 3 mas 1 oral | 11 | Incluye dosis anual de antigripal |
| 11 años | 3 | 14 | Incluye 2 dosis de vacuna HPV |
| 12, 13, 14 y 15 años | 4 | 16 | Dosis anual antigripal |
| Embarazo | 2 | 7 |
ALGUNOS DE LOS COMPONENTES DE LAS VACUNAS (además de los virus, bacterias y toxoides específicos correspondientes):
- ALUMINIO: contenido en las vacunas
Antihepatitis B, Antihepatitis A, Doble DT, Triple bacteriana DTaP, Cuádruple,
Quíntuple y Séxtuple, Anti Papiloma virus (HPV) y Antimeningococo. - MERCURIO: bajo la forma de Timerosal.
Contenido en las vacunas: Antigripal y Anti meningococo. - MATERIAL GENÉTICO DE CÉLULAS DE FETOS HUMANOS: bajo la
denominación de MRC5 o WI-38. Contenido en las vacunas: Anti hepatitis A,
Quíntuple, MMR II (sarampión, paperas y rubéola), Anti polio (Sabin), Anti
varicela y Antirrábica. - MATERIAL GENÉTICO DE CÉLULAS DE RIÑÓN DE MONO:
denominadas Células Vero. Contenido en las vacunas: Anti Polio (Salk), Séxtuple,
Anti rotavirus y Cuádruple. - MATERIAL GENÉTICO DE CÉLULAS DE EMBRIÓN DE POLLO: MMR II, y
Antirrábica. - ALBÚMINA HUMANA: MMR II (sarampión, paperas y
rubéola) , Antirrábica - PROTEÍNA DE HUEVO:
Antigripal,Fiebre
amarilla. - PROTEÍNA DE LECHE DE VACA (CASEÍNA): Doble
bacteriana DT, Triple bacteriana
(DPT), Anti meningococo, Séxtuple. - PROTEÍNA DE VACA (SUERO BOVINO): Triple
bacteriana DPT; Cuádruple, Quíntuple, Séxtuple, Hepatitis A, MMR II, Anti Polio
(Salk), Antirrábica, Anti Rotavirus. - PÉPTIDOS DE SOJA: Antineumococo.
- ESCUALENO (figura como AS03 o como MF59): Vacunas
antigripales. - POLISORBATO 80 (figura también como MF59 o como Tween
80): Vacunas antigripales, Triple bacteriana DPT, Cuádruple,
Quíntuple, Séxtuple, Anti hepatitis A, Antihepatitis B, Anti Papiloma (HPV),
Anti Meningococo, Anti Neumococo, Anti Rotavirus. - FORMALDEHÍDO o FORMALINA: Doble
bacteriana DT, Triple bacteriana DPT, Cuádruple, Quíntuple, Séxtuple,
Anti hepatitis A, Antihepatitis B, Polio
(Salk), Anti Meningococo, Antigripales. - ANTIBIÓTICOS: NEOMICINA: Cuádruple,
Quíntuple, Séxtuple, Hepatitis A, Anti gripales, MMR II (sarampión, paperas y
rubéola), Anti Varicela. POLIMIXINA B: Cuádruple, Quíntuple, Séxtuple,
Antigripales, Anti Polio (Salk). ESTREPTOMICINA: Anti polio (Salk) - GLUTAMATO MONOSÓDICO: Antigripales, MMR II(sarampión,
paperas y rubéola), Antirrábica, Anti Varicela. - LEVADURAS: Anti Meningococo, Anti Neumococo,
Anti hepatitis A, Antihepatitis B, Anti
Papiloma (HPV), Quíntuple. - ALGUNOS COMPONENTES CONTAMINANTES DE VACUNAS
ENCONTRADOS EN EL ANÁLISIS ACCIDENTAL DE ALGUNAS VACUNAS A LO LARGO DE LA
HISTORIA (8) (17):
VIRUS SV40 (causa tumores de cerebro y se encontró en vacunas de polio oral hasta 1960) (9).
VIRUS AVIAR (en algunas vacunas antigripales de laboratorios Baxter). PROTEÍNAS ATÍPICAS (en vacunas de laboratorio Novartrix en Europa). PRIONES (partículas infecciosas cuya estructura molecular actúa sobre las proteínas de nuestro cuerpo) en suero y gelatina bovinos utilizados en la fabricación de vacunas). INHIBIDORES ENZIMÁTICOS (generadores de enfermedad metabólica). VIRUS AVIARES (en vacuna antisarampionosa). VIRUS ESPUMANTE DE SIMIO (en vacunas contra Rotavirus). CITOMEGALOVIRUS DE SIMIO (en vacunas contra la polio). VIRUS DE CÁNCER AVIAR (en vacunas MMR). VIRUS DE PATO, PERRO Y CONEJO (en antirrubeólica). VIRUS DE LEUCOSIS AVIAR (en vacunas antigripales).
Este compendio de estudios de expertos, contiene la suficiente evidencia para que los padres puedan presentar a sus médicos y abogados y prevenir que su hijos sean intoxicados con vacunas o inyecciones génicas que no tienen los suficientes estudios de seguridad como corresponde. Tambien sirve para educar a los médicos sin pensamiento crítico. Click aqui para descargar este compendio
TOXICIDAD DE ALGUNOS DE LOS COMPONENTES MENCIONADOS
- ALUMINIO
Se usa como adyuvante en las vacunas arriba mencionadas. Su inyección provoca trastornos degenerativos de las neuronas motoras, provocando parálisis entre otros problemas y reacción inflamatoria (16). Según consta en la bibliografía nacional (1) e internacional, la exposición al aluminio puede provocar alteraciones en diversos órganos y tejidos (riñón, huesos y sistema nervioso central). La exposición al aluminio se ha relacionado con el Alzheimer, enfermedad de Parkinson y alteraciones de la conducta. También se ha visto un aumento alarmante de la Esclerosis múltiple en Francia relacionada con la aplicación de vacuna antihepatitis B en adultos (2)
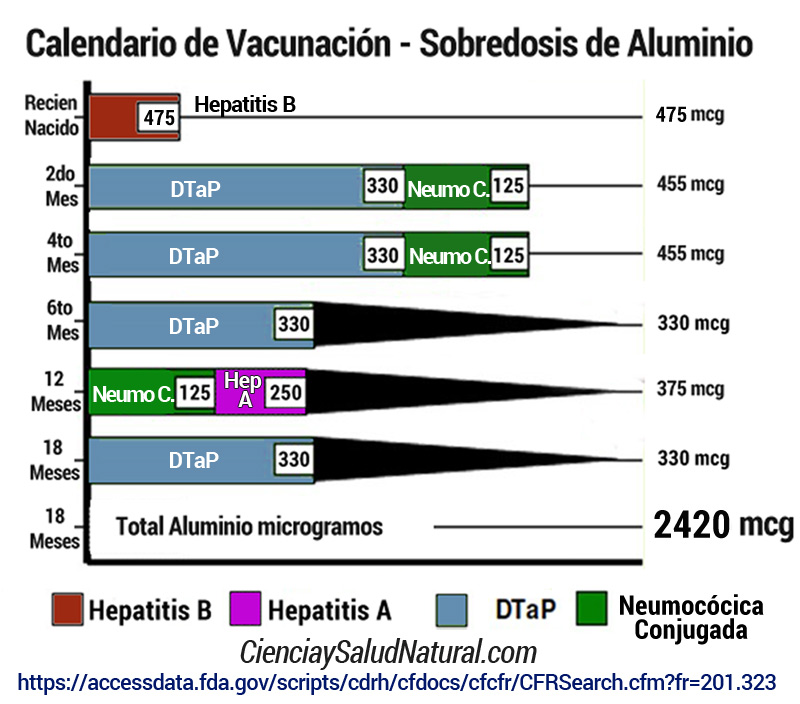
En este cuadro se ha modificado el dato original en el que figuraba que el recién nacido recibe solo 250mcg de aluminio (según prospecto aprobado por la FDA en EEUU), ya que en el prospecto de la vacuna marca Engerix B autorizada por ANMAT figura que la vacuna contiene 950 mcg de aluminio por ml y que se indica inyectar 0,5ml a menores de 10 años, lo que significa una inyección real de aluminio de 475 mcg a un recién nacido, o sea una dosis aproximadamente 30 veces más alta que la dosis diaria tóxica permitida.
El aluminio en las vacunas es neurotóxico y el calendario de vacunación infantil tiene sobredosis de aluminio. Los estudios de seguridad del aluminio tienen graves errores y este tema esta postergado desde hace décadas. Más de 100 referencias científicas de expertos para que Usted presente a su abogado o médico, para eximir a sus hijos de las vacunas. Descargar libro click aqui
- MERCURIO
La gran mayoría de las vacunas pediátricas empleadas en nuestro medio utilizan las dosis más altas permitidas de etilmercurio (25 mg en cada una de ellas). Se encontraron múltiples asociaciones entre la exposición a timerosal y las enfermedades del neurodesarrollo infantil. Tal neurotoxicidad ocurre en los infantes y fetos de gestantes vacunadas por dosis acumulativa de mercurio. Las diversas evidencias implican al timerosal como el agente causante, agravante o disparador de las enfermedades del neurodesarrollo infantil. (4)
Diversos estudios notaron que la curvas de incremento de los casos de autismo (TEA) coincidían con el aumento del número de vacunas pediátricas y sus respectivos refuerzos, estando directamente relacionadas a las dosis de exposición total al timerosal.
Dr. Lawrence Palevsky. El aluminio en las vacunas pueden entrar en el cerebro y es neurotóxico.
La vacunas del calendario escolar de vacunación tienen sobredosis de aluminio, el aluminio causa enfermedades neurológicas y autoinmunes. Han incorporado diferentes nuevas vacunas desde 1986, no por razones de salud sino para justificar la inversión en desarrollo de armas biologicas como la inyección K0 B1T https://www.bitchute.com/video/KK2WMP1YBCrp/
El timerosal se disocia en el organismo en etilmercurio y tiosalicilato, siendo un compuesto químico altamente inestable. Debido a su gran liposolubilidad, puede atravesar fácilmente la barrera hematoencefálica y la placentaria.
Por lo tanto se deposita en el sistema nervioso central (cerebro) (15)
Al tener una vida media tan larga (entre 227 y 540 días) es imposible que el niño logre eliminar el mercurio acumulativo de las vacunas múltiples recibidas con intervalos cortos a veces de tan solo 30 días (4) (5) (6).

- Toxicidad y Riesgos de las Vacunas con Mercurio
- Antecedentes y diferencia entre el etilmercurio y el metilmercurio
- Estudios de la FDA para justificar el uso de etilmercurio
- Pautas para las exposiciones diarias máximas permitidas al mercurio
- Niveles de exposición al etilmercurio según las directrices sobre metilmercurio
- Vacunas con Timerosal
- Historia del Timerosal
- Más de 40 Documentos Científicos demostrando la toxicidad del Thimerosal
- Resúmenes de 240 estudios que muestran los efectos nocivos tanto del timerosal como del mercurio
- Click aqui para descargar documentación
- MATERIAL GENÉTICO DE CÉLULAS DE FETOS HUMANOS: bajo la
denominación de MRC5 o WI-38. Existe una relación directa entre inyectar ADN
fetal y las enfermedades graves en los niños, además de provocar un daño
genético irreparable que se transmite a futuras generaciones (19) (20) (21) desconociéndose su
posible efecto mutagénico ya que en los prospectos no figura que se haya
descartado ni estudiado dicho efecto. - MATERIAL GENÉTICO DE CÉLULAS DE RIÑÓN DE MONO:
denominadas Células Vero. Como todo material genético ajeno al cuerpo, al
incorporarse al genoma humano puede desencadenar reacciones de autoinmunidad y
cáncer. - MATERIAL GENÉTICO DE CÉLULAS DE EMBRIÓN DE POLLO: Como todo
material genético ajeno al cuerpo, al incorporarse al genoma humano puede
desencadenar reacciones de autoinmunidad y cáncer. - ALBÚMINA HUMANA: proteína ajena, capaz de
desencadenar alergia y trastornos inmunológicos. - PROTEÍNA DE HUEVO: otra proteína ajena al
organismo. Los prospectos que la contienen indican claramente que se debe tener
precaución en su administración en personas alérgicas al huevo, sin embargo
esto no se investiga antes de indicar la vacunación sistemática. Puede generar
alergia al huevo. - PROTEÍNA DE LECHE DE VACA (CASEÍNA): caso
similar al de la proteína de huevo. No solo puede desencadenar grave reacción
de alergia sino que puede provocar alergia a la leche de vaca en un individuo
sano al ser inyectada, ya que la caseína en situación normal nunca se absorbe
completa en intestino sino que se digiere para luego absorberse como péptidos y
aminoácidos. - PROTEÍNA DE VACA (SUERO BOVINO): es el
mismo caso que 7) y 8). - ESCUALENO
Figura como coadyuvante AS03 o MF59, y a veces como en las vacunas de la gripe, está en combinación con polisorbato 80 y se identifica en el prospecto como MF59C.1- Es un hidrocarburo natural hidrofóbico obtenido originalmente con propósitos comerciales a partir del aceite de hígado de tiburón, pero que es producido por todos los organismos complejos, incluidos los seres humanos, puesto que es un precursor del colesterol.
Al ser inyectado al ser humano a través de una vacuna, genera anticuerpos contra el propio escualeno natural y desencadena trastornos neurológicos y narcolepsia (10) además de reacción inflamatoria en general (16).
- POLISORBATO 80: es un emulsionante que se
usa como adyuvante para que algunas drogas puedan pasar al cerebro. Puede estar
combinado con escualeno y figurar en el prospecto como MF59C.1. En las vacunas
el polisorbato 80 se adhiere al aluminio y al mercurio, que a su vez se adhieren
al virus o bacteria que contiene la vacuna y gracias al polisorbato atraviesan
la barrera hematoencefálica con su correspondiente efecto tóxico directo sobre
el cerebro. - GLUTAMATO MONOSÓDICO
Conocido en los alimentos como E621 o como MSG. Su toxicidad es mucho mayor al ser inyectado como sucede con todas las sustancias tóxicas en general. Provoca trastornos por acción directa sobre el hipotálamo en los patrones del sueño, la pubertad e incluso el apetito (obesidad) por su condición de excitotoxina. . (11) (12) (13) (14)
La excitotoxicidad es el proceso patológico por el cual las neuronas son dañadas y destruidas por las sobreactivaciones de receptores del neurotransmisor excitatorio glutamato. Por lo tanto es neurotóxico aún a dosis bajas por vía oral. Está contraindicado en Alzheimer, demencia senil, Parkinson, esquizofrenia, epilepsia, etc. Es un gran generador de trastornos vasomotores, reacciones en piel y pulmones
- FORMALINA o FORMALDEHÍDO: según
figura escrito en la Agencia para Sustancias Tóxicas y el Registro de
Enfermedades (ATSDR) de EEUU nuestros cuerpos producen cantidades pequeñas de
formaldehído en forma natural como parte del metabolismo diario normal. Su
absorción inhalatoria o por vía oral puede causar desde irritación local hasta
cáncer de garganta y nariz. No hay estudios acerca de su toxicidad al ser
inyectado en el cuerpo a través de una vacuna.
RESUMEN DE ALGUNAS DE LAS CONTRAINDICACIONES, PRECAUCIONES Y REACCIONES ADVERSAS QUE FIGURAN EN LOS PROSPECTOS DE VACUNAS INCLUÍDAS EN EL CALENDARIO NACIONAL ARGENTINO:
I- VACUNA TRIPLE VIRAL MMR II:
Contraindicaciones: No administrar M-M-R II a mujeres embarazadas. Si se vacuna a mujeres que ya han pasado de la pubertad, éstas deben evitar el embarazo durante los tres meses siguientes a la vacunación. Reacciones anafilácticas o anafilactoides a la neomicina. Antecedentes de reacción anafiláctica o anafilactoide al huevo. Cualquier enfermedad respiratoria febril o infección febril activa. Tuberculosis activa no tratada. Pacientes bajo tratamiento inmunosupresor. Pacientes con discrasias sanguíneas, leucemia, linfomas de cualquier tipo, u otras neoplasias malignas que afectan la médula ósea o el sistema linfático. Estados de inmunodeficiencia primaria y adquirida, incluyendo pacientes inmunosuprimidos en relación con el SIDA u otras manifestaciones clínicas de infección con virus que producen inmunodeficiencia humana; deficiencias inmunológicas celulares y estados hipogamaglobulinémicos y disgamaglobulinémicos. Personas con antecedentes familiares de inmunodeficiencia congénita o hereditaria, hasta que se demuestre la capacidad inmunitaria de quien va a recibir la vacuna. Hipersensibilidad al huevo.
Efectos adversos: Digestivas: Parotiditis, náuseas, vómitos, diarrea. Hematológicas, Linfáticas: Linfadenopatía regional, trombocitopenia, púrpura. Hipersensibilidad: Reacciones alérgicas tales como máculas y pápulas en el sitio de la inyección, reacciones. anafilácticas o anafilactoides, urticaria. Musculoesqueléticas: Artralgia y/o artritis (generalmente transitorias y raramente crónicas, miagia). Sistema Nervioso / Psiquiátricas: Convulsiones febriles en niños, convulsiones afebriles o ataque epiléptico, cefalea, mareos, parestesia, polineuritis, síndrome de Guillain-Barre (parálisis ascendente), ataxia. Dermatológicas: Eritema multiforme. Sentidos: Formas de neuritis óptica, incluyendo neuritis retrobulbar, papilitis y retinitis, parálisis oculares, otitis media, nervio acústico, conjuntivitis. Urogenitales: Orquitis. Existen informes de la aparición de panencefalitis esclerosante subaguda. Artralgia. Artritis.
Los efectos secundarios de la vacuna contra el Sarampión, Rubeola y Paperas, SRP (MMR en EE.UU.) incluyen convulsiones, que ocurren en aproximadamente 1 de cada 640 niños vacunados, aproximadamente 5 veces más frecuentemente que las convulsiones por infección de sarampión, sepa como eximir a sus hijos de esta vacuna. Este compendio de estudios de expertos, contiene la suficiente evidencia para que los padres puedan presentar a sus médicos y abogados y prevenir que su hijos sean intoxicados con vacunas que no tienen los suficientes estudios de seguridad como corresponde. Tambien sirve para educar a los médicos sin pensamiento crítico. Descargar libro click aqui
II- VACUNA SÉXTUPLE BACTERIANA:
Contraindicaciones: no debe aplicarse la vacuna si su hijo ha tenido un trastorno respiratorio o hinchazón de la cara (reacción anafiláctica) tras su administración. Si ha tenido una reacción alérgica a los principios activos, a cualquiera de los demás componentes incluidos en la composición, al glutaraldehído, formaldehído, neomicina, estreptomicina y polimixina B, ya que estas sustancias se utilizan durante el proceso de fabricación, o tras la administración previa de esta o cualquier otra vacuna que contenga difteria, tétanos, tos ferina, poliomielitis, hepatitis B o Hib.
Tampoco si ha padecido una reacción grave que afecta al cerebro (encefalopatía) en los 7 días posteriores a la administración de una dosis previa de una vacuna frente a la tos ferina (acelular o de célula entera).
O si tiene una enfermedad no controlada o enfermedad grave que afecte al cerebro y al sistema nervioso (trastorno neurológico no controlado) o una epilepsia no controlada.
Advertencias y precauciones:
Antes de la vacunación consulte a su médico, farmacéutico o enfermero si su hijo: tiene una temperatura moderada o alta o una enfermedad aguda (fiebre, dolor de garganta, tos, resfriado o gripe). Si ha padecido alguno de los siguientes acontecimientos adversos después de recibir una vacuna frente a la tos ferina, deberá evaluarse cuidadosamente la decisión de administrar otras dosis: – fiebre de 40ºC o superior en las 48 horas siguientes. Colapso o estado similar al shock con episodio hipotónico–hiporreactivo (debilidad) en las 48 horas siguientes a la vacunación. Llanto inconsolable, persistente durante 3 horas o más, producido en las 48 horas siguientes a la vacunación. Ataques (convulsiones) con o sin fiebre, producidas en los 3 días siguientes a la vacunación. Si ha padecido anteriormente síndrome de Guillain-Barré (inflamación temporal de los nervios que provocan dolor, parálisis y trastornos en la sensibilidad) o neuritis braquial (dolor grave y disminución de la movilidad en brazo y hombro) después de la administración de una vacuna que contenga toxoide tetánico. Si está recibiendo un tratamiento que suprime su sistema inmunológico o presenta cualquier enfermedad que provoca una inmunodeficiencia. Si padece una enfermedad aguda o crónica incluyendo insuficiencia renal crónica o fallo. Si padece cualquier enfermedad cerebral no diagnosticada o epilepsia no controlada. Si tiene algún problema de la sangre que provoque la aparición de hematomas con facilidad o sangrado prolongado tras producirse pequeños cortes
Reacciones adversas:
Reacciones alérgicas graves (reacción anafiláctica). – adormecimiento (somnolencia). Vómitos. Irritabilidad. Llanto anormal. Diarrea. Hinchazón de un miembro que se extiende desde el lugar de la inyección hasta más allá de una o ambas articulaciones. Convulsiones con o sin fiebre. Estado similar al shock. Reacciones de hipotonía.
Se ha notificado después de la administración de vacunas que contienen tétanos: inflamación temporal de los nervios que provocan dolor, parálisis y trastornos en la sensibilidad (Síndrome de Guillain-Barré) dolor severo y disminución de la movilidad en el brazo y hombro (neuritis braquial).
Se han notificado después de la administración de vacunas que contengan el antígeno de hepatitis B, inflamación de los nervios que provocan trastornos sensoriales o debilidad de los brazos y/o piernas (poli radiculoneuritis), parálisis facial, trastornos visuales, oscurecimiento o pérdida repentina de la visión (neuritis óptica), enfermedad inflamatoria del cerebro y la médula espinal (desmielinización del sistema nervioso central, esclerosis múltiple). Hinchazón o inflamación del cerebro (encefalopatía/encefalitis). En los niños nacidos muy prematuramente (a las 28 semanas de gestación o antes) se pueden producir intervalos entre respiraciones más largos de lo normal durante 2-3 días posteriores a la vacunación. Tras la administración de vacunas que contienen Haemophilus influenzae tipo b: Hinchazón de uno o ambos pies y extremidades inferiores. Esto puede producirse junto con una coloración azulada de la piel (cianosis), enrojecimiento, pequeñas áreas de sangrado bajo la piel (púrpura transitoria) y llanto grave.
Del mismo modo que hoy nos intentan seguir engañado con los beneficios de la inyección contra Covid, la historia de la vacuna contra la polio ha sido tergiversada. La verdadera historia de la vacuna contra la polio es muy diferente a la que le han relatado a los médicos en la facultad de Medicina y es todo lo opuesto. Descargar click aqui
III- VACUNA TRIPLE BACTERIANA ACELULAR DPaT
Contraindicaciones:
No debe administrarse a sujetos con hipersensibilidad conocida a cualquiera de los componentes de la vacuna ni a sujetos que hayan mostrado signos de hipersensibilidad después de una administración previa de vacunas contra difteria, tétanos o pertussis.
Contraindicada en sujetos que hayan padecido una encefalopatía de etiología desconocida dentro de los siete días posteriores a una vacunación previa con vacunas con el componente pertussis.
No debe administrarse a sujetos que hayan padecido trombocitopenia transitoria o complicaciones neurológicas luego de haber recibido una inmunización previa contra difteria y/o tétanos.
Advertencias y Precauciones:
La vacunación debe ser precedida por una revisión de la historia clínica (especialmente con respecto a una vacunación previa y a la posible ocurrencia de eventos adversos) y por un examen clínico.
Si se sabe que alguno de los siguientes eventos ocurrió en relación temporal a la administración de una vacuna con componente pertussis, se deberá considerar cuidadosamente la decisión de administrar dosis de vacunas con el componente pertussis: temperatura ≥40,0°C dentro de las 48 horas posteriores, estado de colapso o similar al shock (episodio hipotónico – hiporreactivo) dentro de las 48 horas posteriores a la vacunación, llanto persistente e inconsolable, convulsiones.
En niños con trastornos neurológicos progresivos, incluyendo espasmos infantiles, epilepsia no controlada o encefalopatía progresiva, es mejor diferir la vacunación con pertussis.
La decisión de vacunar con pertussis debe realizarse en forma individualizada después de una cuidadosa evaluación de los riesgos y beneficios.
Efectos adversos:
Se han notificado casos de estado de colapso o similar al estado de shock (episodios hipotónicos-hiporreactivos) y convulsiones dentro de los 2 a 3 días posteriores a la vacunación con vacunas DTPa y vacunas combinadas DTPa.
Sólo debe usarse durante el embarazo cuando los posibles beneficios superen los posibles riesgos para el feto.
Infecciones del tracto respiratorio superior. Anorexia. Irritabilidad.
Trastornos del sistema nervioso: convulsiones, somnolencia, cefalea, alteración de la atención. Conjuntivitis. Diarrea, vómitos, desórdenes gastrointestinales. Reacciones anafilácticas.
Erupción cutánea. Fatiga. Linfadenopatía. Mareos. Síncope. Tos. Artralgia, mialgia, rigidez de las articulaciones, rigidez musculoesquelética.
IV- VACUNA ANTIHEPATITIS B:
Efectos Adversos:
Normalmente estos signos comienzan muy poco después de que le administren la inyección: hinchazón de la cara, tensión arterial baja, respiración dificultosa, la piel se vuelve azul (cianosis), pérdida de conocimiento.
Sensación de cansancio, irritabilidad, dolor de cabeza, adormecimiento, náuseas o vómitos, diarrea o dolor abdominal, pérdida de apetito, fiebre, sensación de malestar general, hinchazón e induración. Mareo, dolor muscular, síntomas parecidos a los de la gripe. Glándulas hinchadas, habones, erupción cutánea y prurito. Dolor articular. Hormigueo. Fácil aparición de moratones e incapacidad para detener un sangrado si se hace un corte. Tensión arterial baja.
Inflamación de los vasos sanguíneos, hinchazón repentina de la cara alrededor de la boca y de la zona de la garganta (edema angioneurótico).
Síntomas neurológicos graves: incapacidad para mover los músculos (parálisis)
Inflamación de los nervios (neuritis) que puede causar pérdida de sensibilidad o entumecimiento, incluyendo una inflamación temporal de los nervios, causando dolor, debilidad y parálisis en las extremidades y a menudo progresando al pecho y a la cara (síndrome de Guillain-Barré. Enfermedad de los nervios del ojo (neuritis óptica) y esclerosis múltiple. Problemas para mover los brazos o piernas (neuropatía). Inflamación del cerebro (encefalitis). Enfermedad degenerativa del cerebro (encefalopatía). Infección alrededor del cerebro (meningitis). Convulsiones.
Pérdida de sensibilidad de la piel al dolor o al tacto (hipoestesia).
Piel: bultos de color púrpura o púrpura-rojizo en la piel (líquen plano), dolor y rigidez en las articulaciones (artritis), debilidad de los músculos.
La seguridad de las vacunas contra la hepatitis B que se administran a los recién nacidos no se ha probado en un solo ensayo clínico controlado aleatorio con placebo inerte como se manifiesta en los propios prospectos y tiene sobredosis de aluminio neurotóxico. Este compendio de estudios de expertos, contiene la suficiente evidencia para que los padres puedan presentar a sus médicos y abogados y prevenir que su hijos sean intoxicados con vacunas que no tienen los suficientes estudios de seguridad como corresponde. Tambien sirve para educar a los médicos sin pensamiento crítico. Descargar libro click aqui
V- VACUNA ANTINEUMOCOCO:
Contraindicaciones:
Hipersensibilidad a los principios activos o a alguno de los excipientes incluidos en la sección 6.1, o al toxoide diftérico.
Efectos Adversos:
Trastornos del sistema nervioso: convulsiones, episodios de hiporrespuesta hipotónica, cefaleas. Fiebre, irritabilidad, disminución del apetito y aumento y/o disminución del sueño. Trastornos del sistema inmunológico: reacción de hipersensibilidad, incluidos edema facial, disnea, broncoespasmo. Trastornos gastrointestinales: vómitos y diarrea.
Piel: urticaria o erupción similar, eritema o induración/tumefacción en el lugar de vacunación. Trastornos de la sangre y del sistema linfático:
linfadenopatía (localizada en la zona del lugar de vacunación)
Reacción anafiláctica/anafilactoide, incluido shock; angioedema
Eritema multiforme. Apnea en recién nacidos muy prematuros.
Artralgia; mialgia.
VI- VACUNA ANTIMENINGOCOCO tipo B:
Advertencias y precauciones:
Hemofilia u otros problemas que pudieran afectar a la coagulación de la sangre, como un tratamiento con anticoagulantes. Si su hijo nació prematuramente (a las 28 semanas de gestación o antes), sobre todo si tuvo dificultades respiratorias. Si usted o su hijo tienen alergia al antibiótico kanamicina. Puede producirse desfallecimiento, sensación de pérdida de conocimiento u otras reacciones asociadas al estrés como respuesta a cualquier inyección con aguja. Informe a su médico o enfermero si ha tenido una reacción de este tipo en el pasado.
dolor agudo a la presión en el lugar de la inyección, enrojecimiento de la piel en el lugar de la inyección, hinchazón de la piel en el lugar de la inyección, endurecimiento de la piel en el lugar de la inyección.
Efectos adversos:
Fiebre (≥38 a 40ºC), pérdida del apetito, dolor agudo a la presión en el lugar de inyección (incluyendo dolor intenso en el lugar de inyección que provoca llanto al mover la extremidad en la que se ha administrado la inyección). Articulaciones dolorosas. Erupción cutánea. Somnolencia. Irritabilidad. Llanto inusual. Vómitos. Diarrea. Dolor de cabeza. Erupción cutánea. Convulsiones. Piel seca. Palidez.
Enfermedad de Kawasaki, que puede incluir síntomas como fiebre que dura más de cinco días, asociada a erupción cutánea en el tronco y, a veces, seguida de descamación de la piel de manos y dedos, hinchazón glandular en el cuello y enrojecimiento de ojos, labios, garganta y lengua.
Reacciones alérgicas, que pueden incluir hinchazón intensa de los labios, la boca, la garganta (que puede provocar dificultad para tragar), dificultad para respirar con sibilancia (silbidos al respirar) o tos, erupción, pérdida de conciencia y presión arterial muy baja.
Colapso (aparición de flacidez muscular repentina), nivel de respuesta menor de lo normal o pérdida de consciencia y palidez o coloración azulada de la piel en los niños pequeños.
Sensación de pérdida de conocimiento o desfallecimiento. Rigidez de nuca o excesiva sensibilidad a la luz (fotofobia) indicativos de irritación meníngea.
VII- VACUNA ANTIMENINGOCOCO tipos A, C, W135 e Y
Contraindicaciones:
Hipersensibilidad al principio activo o a cualquier excipiente de la vacuna, incluyendo el toxoide diftérico (CRM197) o una reacción potencialmente mortal después de la administración previa de una vacuna con componentes similares.
Reacciones adversas:
Trastornos de metabolismo y nutrición: desorden alimenticio. Trastornos del Sistema Nervioso: llanto persistente, somnolencia, mareos, síncope, convulsión tónica, convulsión febril, dolor de cabeza, paresia facial, trastorno del equilibrio. Náuseas, diarrea, vómitos. Erupción cutánea. Sensibilidad severa en el lugar de la inyección, fiebre. Poco frecuente: eritema en el sitio de la inyección. Dolor de cabeza. Mialgia, artralgia. Dolores óseos. Trastornos del oído y del laberinto: audición disminuida, dolor de oídos, vértigo, trastorno vestibular. Trastornos oculares: ptosis palpebral. Inflamación e hinchazón, incluyendo hichazón extensa de la extremidad inyectada, fatiga, malestar, pirexia. Trastornos del sistema inmune: hipersensibilidad incluyendo anafilaxia. Exámenes complementarios: alanina aminotransferasa elevada, aumento de la temperatura corporal. Trastornos respiratorios, torácicos y mediastínicos: dolor orofaríngeo. Trastornos de la piel y el tejido subcutáneo: afecciones bullosas.
VIII- VACUNA ANTIGRIPAL:
Reacciones adversas:
Trastornos de la sangre y del sistema linfático: linfadenopatía. Trombocitopenia transitoria. Trastornos del sistema inmunológico: reacciones alérgicas tales como hinchazón de la cara, urticaria, prurito generalizado. Eritema, eritema generalizado.
Reacciones alérgicas graves tales como disnea, angioedema, shock. Cefalea. Sensación de vértigo, somnolencia. Hipoestesia, parestesia, neuralgia, radiculitis braquial. Convulsiones, trastornos neurológicos tales como encefalomielitis, neuritis y síndrome de Guillain Barré. Vasculitis tales como púrpura de Henoch-Schonlein con afección renal transitoria en algunos casos. Diarrea, nausea. Aumento de la sudoración. Trastornos musculoesqueléticos y del tejido conjuntivo: mialgias. Artralgias. Malestar. Astenia. Fiebre, escalofríos, equimosis en el lugar de la inyección. Síndrome pseudogripal.
Este documento contiene la suficiente evidencia cientifica (más de 150 referencias) para que las madres puedan presentar a sus médicos y abogados y lograr exenciones para prevenir ser dañadas con vacunas o inyecciones génicas, que no tienen los suficientes estudios de seguridad como corresponde. Tambien sirve para educar a los médicos sin pensamiento crítico. descargar libro, click aqui
IX- VACUNA ANTI HPV (virus del papiloma):
Efectos Adversos: dolor, hinchazón y enrojecimiento. Dolor de cabeza.
Fiebre y náuseas. Urticaria. Dificultad al respirar (broncoespasmo).
Desfallecimiento, algunas veces acompañado de temblores o rigidez.
Reacciones alérgicas, que pueden incluir dificultad para respirar, silbidos al respirar (broncoespasmo), urticaria y sarpullido. Algunas de estas reacciones han sido graves.
Ganglios inflamados (cuello, axila o ingle); debilidad muscular, sensaciones anormales, hormigueo en los brazos, piernas y parte superior del cuerpo, o confusión (síndrome de Guillain‑Barré, encefalomielitis aguda diseminada); mareos, vómitos, dolor en las articulaciones, dolor en los músculos, cansancio o debilidad inusual, escalofríos, malestar general, sangrado o aparición de moretones más fácilmente de lo normal e infección de la piel en el lugar de inyección.
(Cabe mencionar que existen en EEUU y en Europa varios juicios por daño grave de dicha vacuna inclusive la muerte)
Este documento contiene la suficiente evidencia científica (más de 50) para que las madres puedan presentar a sus médicos y abogados y prevenir sus hijas e hijos sean dañados con vacunas que no tienen los suficientes estudios de seguridad como corresponde. Tambien sirve para educar a los médicos sin pensamiento crítico. No espere hasta último momento para estar protegida… descargar desde: https://cienciaysaludnatural.com/recursos

X- VACUNA SABIN:
Tras la vacunación, los virus de la vacuna se multiplican en el intestino. Por ello los virus se eliminan con las heces (con el consiguiente riesgo de contagiar a otros).
Efectos adversos: desarrollo de signos y síntomas de poliomielitis paralítica.
Reacciones alérgicas (pueden ser erupciones locales o diseminadas que pueden cursar con picor o con ampollas, hinchazón de los ojos y la cara, dificultad para
respirar o tragar, una repentina bajada de la presión arterial y pérdida de conciencia).
XI- VACUNA BCG:
Aumento de tamaño de los ganglios linfáticos (> 1 cm), dolor de cabeza, fiebre, úlcera en la zona de inyección, inflamación con pus de los ganglios.
Infección diseminada, tal como inflamación aguda o crónica de los huesos (osteomielitis), originada o no por una infección, absceso en la zona de inyección, reacción alérgica, reacción de hipersensibilidad (22)
En la práctica pediátrica diaria se observa mayor incidencia de bronquiolitis recurrente y tendencia a otras enfermedades respiratorias desde el primer mes de vida en niños vacunados con BCG al nacer en comparación con niños no vacunados
Comentario: Suecia la ha retirado de su calendario de vacunación, por ser la causa de 1/3500 de muertes (una proporción muchísimo más alta que la causada por la Tuberculosis).
Si no le queda alternativa, No deje que vacunen a su hijo antes de hacer este Test
De acuerdo al Instituto de Medicina de la Academia de Ciencias de los EEUU., IOM: “Tanto las investigaciones epidemiológicas como las mecanicistas sugieren que la mayoría de los individuos que experimentan una reacción adversa a las vacunas tienen una susceptibilidad preexistente. Estas predisposiciones pueden existir por varias razones: variantes genéticas (en el ADN humano o microbioma), exposiciones ambientales, comportamientos, enfermedades intermedias o etapa de desarrolloy pueden interactuar entre ellas. https://www.nap.edu/read/13164/chapter/5#82
Más del 30% de las personas tienen mutaciones geneticas. No se puede vacunar a los niños sin antes comprobar si tiene o no esta mutación de tipo MTHFR. No permita que vacunen a su hijo sin antes hacer este test.
CONCLUSIONES:
Luego de haber efectuado este estudio analítico del Calendario de Vacunación nacional obligatorio, se puede observar que:
- No existen
estudios de seguridad de ninguna vacuna, ni se han estudiado los posibles
efectos adversos al combinar varias vacunas juntas en el mismo día. No se ha
estudiado tampoco la seguridad del intervalo entre la aplicación de tantas
vacunas en el organismo del recién nacido y lactante que aún tienen su sistema
inmunológico inmaduro y además tienen incapacidad para eliminar de su cuerpo
sustancias tóxicas neurológicas tales como el mercurio y el aluminio. - No se han
encontrado estudios serios que comparen la morbimortalidad de las enfermedades
infectocontagiosas naturales con la morbimortalidad de las vacunas que se
aplican para evitarlas. - Desde el
momento en que se indican las vacunas en forma obligatoria, no se tienen en
cuenta las innumerables advertencias de los efectos adversos, ni las
contraindicaciones ni las precauciones que cada fabricante de vacunas expresa
claramente en los prospectos. - Este
calendario de vacunación tampoco contempla los casos individuales en los que
podría haber situaciones genéticas, metabólicas o inmunológicas que ponen al
niño en riesgo de trastornos graves y aún la muerte al ser vacunado sin
evaluación previa completa de su estado actual, a pesar de que en todos los
prospectos de las vacunas revisadas figura que antes de aplicar la vacuna se
debe hacer una historia clínica completa del paciente para descartar que esté incluido
dentro de las categorías de contraindicaciones de dicha vacuna. - Dada la
larga lista de contraindicaciones y precauciones, tanto los médicos como los pacientes
deben estar muy bien informados antes de recibir cualquier vacuna acerca de su
contenido completo y detallado para saber si existe algún riesgo agravado por
la condición de la persona, cumpliendo con la Ley de Consentimiento Informado
Nº 26.529. - La
vacunación es un acto médico y como tal el médico debe indicar libremente las
vacunas que considere necesarias habiendo sopesado cuidadosamente el riesgo
estadístico que implica aplicarse dicha vacuna versus el riesgo estadístico de
padecer alguna complicación grave de la enfermedad para la que indica cada
vacuna. Para ello previamente debe informar al paciente con toda claridad qué
contienen las vacunas a indicar, qué efectos adversos podrían traerle a su
hijo, qué garantía tiene de que las vacunas realmente serán efectivas y cuál es
el riesgo real de que el niño tenga algún problema si no las recibe. De esta
forma los padres podrán ejercer su derecho al Consentimiento Informado y elegir
la mejor opción para su niño sano. - Recordemos
que las vacunas con todo su contenido ya detallado y el riesgo de efectos
adversos a corto, mediano y largo plazo, se administra a niños SANOS.

Descargar desde https://red.cienciaysaludnatural.com/
REFERENCIAS BIBLIOGRÁFICAS
1) Alteraciones neurológicas y psiquiátricas secundarias a la exposición al aluminio. Neurologic and psychiatric alterations for aluminium exposition. Mª S. Gómez Alcalde1 Cuadernos de Medicina Forense Nº 24- Abril 2001
2) Evolución de la esclerosis multiple en Francia desde que se inició la vacunación contra Hepatitis B. Evolution of multiple sclerosis in France since the beginning of hepatitis B vaccination Dominique Le Houe ́zec – Immunol Res (2014) 60:219–225 – DOI 10.1007/s12026-014-8574-4
3) La inyección de hidróxido de aluminio produce deficit motor y degeneración de las neuronas motoras. Aluminum hydroxide injections lead to motor deficits and motor neuron degeneration. Christopher A. Shawa,b,c,* and Michael S. Petrikc J Inorg Biochem. 2009 Nov; 103(11): 1555. An. Fac. med. v.67 n.3 Lima jul.- sep. 20064)
4) El timerosal y las enfermedades del neurodesarrollo infantil. Luis Maya 1,2, Flora Luna 2 – 1 Departamento de Medicina Interna, Hospital Nacional Arzobispo Loayza. 2 Facultad de Medicina, Universidad Nacional Mayor de San Marcos (UNMSM). Lima, Perú.
5) Una evaluación del uso de Timerosal en las vacunas de los niños. Ball L, et al. An assessment of thimerosal use in childhood vaccines. Pediatrics. 2001;107:1147-54. [ Links ]
6) La concentración de mercurio predictible en cabello de los niños proveniente de las vacunas causa preocupación. Predicted mercury concentrations in hair from infant immunizations: cause of concern. Neurotoxicology. 2001;22:691-7. [ Links ] 30. Redwood L, et al.
8) Científicos italianos encuentran contaminantes inesperados en todas las vacunas pediátricas, incluyendo plomo, acero inoxidable, tungsten, hierro, y cromo. Italian scientists find unexpected contaminants in all pediatric vaccines, including lead, stainless steel, tungsten, iron, and chromium. New Quality-Control Investigations on Vaccines: Micro- and Nanocontamination. International Journal of Vaccines and Vaccination, January 2017, Dr. Antonietta M. Gatti, Stefano Montanari.
9) Virus del mono 40 y patogenia humana emergente, su rol en el cáncer. Emergent Human Pathogen Simian Virus 40 and Its Role in Cancer Clin Microbiol Rev. 2004 Jul; 17(3): 495–508. doi: 10.1128/CMR.17.3.495-508.2004. – Regis A. Vilchez1,2 and Janet S. Butel2,*
10) El adyuvante endógeno Escualeno puede inducer una artritis crónica mediada por linfocitos T en ratas. The Endogenous Adjuvant Squalene Can Induce a Chronic T-Cell-Mediated Arthritis in Rats- Am J Pathol. 2000 Jun; 156(6): 2057–2065. doi: 10.1016/S0002-9440(10)65077-8 – Barbro C. Carlson,* Åsa M. Jansson,* Anders Larsson,† Anders Bucht,‡* and Johnny C. Lorentzen*
11) Actualización del Sistema neurotransmisor del glutamato y el rol de la excitotoxicidad en la Esclerosis Lateral Amiot´rofica. Update on the glutamatergic neurotransmitter system and the role of excitotoxicity in amyotrophic lateral sclerosis. Review Muscle Nerve 2002 Oct;26(4):438-58. doi: 10.1002/mus.10186. Paul R Heath 1, Pamela J Shaw
12) El rol del Glutamato y la excitotoxicidad en enfermedades neurológicas. Role of glutamate and excitotoxicity in neurologic diseases. Hugon J, Vallat JM, Dumas M. Rev Neurol (Paris). 1996 Apr;152(4):239-48. PMID: 8763652 Review. French.
13) Muerte celular por excitotoxicidad. Excitotoxic cell death- Review J Neurobiol. 1992 Nov;23(9):1261-76. doi: 10.1002/neu.480230915. D W Choi 1- PMID: 1361523 DOI: 10.1002/neu.480230915
14) MUERTE NEURONAL EXCITOTÓXICA: INTERACCIÓN ENTRE LAS RUTAS DE SEÑALIZACIÓN DEL IGF-I Y EL GLUTAMATO- memoria para optar al grado de doctor presentada por Eva García Galloway Bajo la dirección de los doctores Ignacio Torres Alemán y Sebastián Pons Fuxá- Madrid, 2003- ISBN: 84- Universidad complutense de Madrid- Facultad de ciencias biológicas- Departamento de Biología Celular
15) Efectos neurotóxicos del timerosal, a dosis de vacuna, sobre el encéfalo y el desarrollo en hámsteres de 7 días de nacidos- Jonny Laurente 1 , Fany Remuzgo 1 , Betthina Ávalos 1 , Johnnie Chiquinta 1 , Bladimir Ponce 1 , Ronald Avendaño 1 , Luis Maya 2,3 – Anales de la Facultad de Medicina Universidad Nacional Mayor de San Marcos- ISSN 1025 – 5583
16) ASIA: síndrome autoimmune e inflamatorio inducido por adyuvantes – ‘ASIA’ – autoimmune/inflammatory syndrome induced by adjuvants -Journal of Autoimmun. 2011 Feb;36(1):4-8. doi: 10.1016/j.jaut.2010.07.003. Epub 2010 Aug 13. Yehuda Shoenfeld 1, Nancy Agmon-Levin PMID: 20708902 DOI: 10.1016/j.jaut.2010.07.003
17) Investigación de vacunas: Micro y Nano contaminantes Investigations on Vaccines: Micro-and Nanocontamination. Gatti et al. New Quality-Control Int J Vaccines & Vaccin 2016, 4(1)
18) Mostafa y col. 2014, J Neuroimmunol, vol. 272, págs. 94–98; Mostafa y col. 2015, J Neuroimmunol, vol. 280, págs. 16–20
19) Impacto de factores ambientales en la prevalencia del autismo después de 1979. Impact of environmental factors on the prevalence of autistic disorder after 1979 Author(s): Theresa A. Deisher, Ngoc V. Doan, Angelica Omaiye, Kumiko Koyama and Sarah Bwabye -https://doi.org/10.5897/JPHE2014.0649 Article Number: C98151247042
20) Deisher y col. Issues Law Med, 2015 vol. 30, págs. 25-46
21) https://www.cdc.gov/vaccines/pubs/pinkbook/rubella.html; Plotkin, SA. 2006, Enfermedades infecciosas clínicas, vol. 43, págs. S164–168
22) Severe adverse reactions after vaccination with Japanese BCG vaccine: a review. Reacciones adversas severas luego de la vacuna BCG japonesa: una revisión. Toida, Nakata S, Kekkaku. 2007 Nov;82(11):809-24. PMID: 18078106
23) www.cienciaysaludnatural.com
24) www.cienciaysaludnatural.com
Colabore por favor con nosotros para que podamos incluir mas información y llegar a más personas: contribución en mercado pago o paypal por única vez, Muchas Gracias!
Via PAYPAL: Euros o dólares click aqui
ARGENTINA 10.000$ar https://mpago.la/1srgnEY
5.000$ar https://mpago.la/1qzSyt9
1.000$ar https://mpago.la/1Q1NEKM
Solicite nuestro CBU contactenos
Parásitos, tratamientos naturales, hierbas y alimentos que pueden librarnos de varios tipos de parásitos: Cáscara de nuez negra, Ajenjo, Clavo de olor y otras, desontoxicación durante y post-tratamiento, como restaurar el microbioma. Más de 200 referencias científicas. Descargar aqui
Diferentes alternativas han demostrado una importante actividad antiinflamatoria y antioxidante, lo que contribuye a reducir la inflamación y el daño tisular. Estas ofrecen un método complementario o alternativo para un tratamiento eficaz y seguro. En esta revisión, se toman en cuenta la seguridad y la eficacia (incluidos los resultados en cuanto al dolor y la inflamación). Descargar click aqui













