
Este documento se alojó originalmente en la cuenta de Doctors for Covid Ethics Medium , pero ha sido censurada y se eliminaron los documentos, alegando que la publicación estaba «bajo investigación» :
Usamos el término K0 B¡T para no ser excluidos de los buscadores y redes sociales que responden a los laboratorios como Google, Twitter, FB, Instagram etc.
En resumen, la evidencia y la ciencia disponible indican que las inyecciones K0 B¡T son innecesarias, ineficaces e inseguras. Los fabricantes de vacunas COVID-19 han sido eximidos de responsabilidad legal por daños inducidos por vacunas. Por lo tanto, es de interés para todos aquellos que autorizan, hacen cumplir y administran las vacunas K0 B¡T, comprender la evidencia sobre los riesgos y beneficios de estas vacunas, ya que la responsabilidad por el daño recaerá sobre ellos.
- Necesidad: las personas inmunocompetentes están protegidas contra el SARS-CoV-2 por medio de la inmunidad celular. Por tanto, no es necesario vacunar a los grupos de bajo riesgo. Para las personas inmunodeprimidas que se enferman con K0 B¡T, existe una variedad de tratamientos médicos que han demostrado ser seguros y efectivos. Por lo tanto, vacunar a los vulnerables es igualmente innecesario. Tanto los grupos inmunocompetentes como los vulnerables están mejor protegidos contra variantes del SARS-CoV-2 por inmunidad adquirida naturalmente y por medicación que por vacunación.
- Eficacia: las inyecciones K0 B¡T carecen de un mecanismo de acción viable contra la infección de las vías respiratorias por el SARS-CoV-2. La inducción de anticuerpos no puede prevenir la infección por un agente como el SARS-CoV-2 que invade las vías respiratorias. Además, ninguno de los ensayos de vacunas ha proporcionado evidencia de que la vacunación evite la transmisión de la infección por personas vacunadas; instar a la vacunación para «proteger a los demás», por tanto, no tiene ningún fundamento.
- Seguridad: las vacunas son peligrosas tanto para las personas sanas como para las que padecen enfermedades crónicas preexistentes, por razones como las siguientes: riesgo de alteraciones letales y no letales de la coagulación de la sangre, incluidos trastornos hemorrágicos, trombosis en el cerebro, accidente cerebrovascular y ataque cardíaco ; reacciones autoinmunes y alérgicas; potenciación de la enfermedad dependiente de anticuerpos; e impurezas de vacunas debido a la fabricación apresurada y los estándares de producción no regulados.
Por tanto, el cálculo de riesgo-beneficio es claro: las inyecciones experimentales son innecesarias, ineficaces y peligrosas. Los agentes que autorizan, coaccionan o administran la inyecciones K0 B¡T experimentales están exponiendo a poblaciones y pacientes a riesgos médicos graves, innecesarios e injustificados.
1. LAS VACUNAS SON INNECESARIAS
1. Múltiples líneas de investigación indican que las personas inmunocompetentes muestran una inmunidad celular (de células T) “robusta” y duradera a los virus del SARS-CoV [ 1 ], incluido el SARS-CoV-2 y sus variantes [ 2 ]. La protección de las células T se deriva no sólo de la exposición al propio SARS-CoV-2, sino también de la inmunidad de reacción cruzada posterior a una exposición previa al resfriado común y los coronavirus del SARS [ 1,3-10 ]. Dicha inmunidad fue detectable después de infecciones hasta 17 años antes [1, 3 ]. Por lo tanto, las personas inmunocompetentes no necesitan vacunación contra el SARS-Cov-2.
2. La inmunidad natural de células T proporciona una protección más fuerte y más completa contra todas las cepas del SARS-CoV-2 que las vacunas , porque la inmunidad preparada naturalmente reconoce múltiples epítopos de virus y señales coestimuladoras, no simplemente una proteína (pico). Por lo tanto, las personas inmunocompetentes están mejor protegidas contra el SARS-CoV-2 y cualquier variante que pueda surgir por su propia inmunidad que por la cosecha actual de vacunas.
3. Las vacunas se han promocionado como un medio para prevenir la infección asintomática [ 11 ] y, por extensión, la «transmisión asintomática». Sin embargo, la «transmisión asintomática» es un artefacto de los procedimientos e interpretaciones de las pruebas de PCR no válidos y poco fiables, lo que da lugar a altas tasas de falsos positivos [ 12-15 ]. La evidencia indica que las personas asintomáticas positivas a la PCR son falsos positivos sanos, no portadores. Un estudio exhaustivo de 9.899.828 personas en China encontró que los individuos asintomáticos que dieron positivo por COVID-19 nunca infectaron a otros [ 16 ].
Por el contrario, los artículos citados por el Centro para el Control de Enfermedades [ 17,18 ] para justificar las afirmaciones de transmisión asintomática se basan en modelos hipotéticos, no en estudios empíricos; presentan supuestos y estimaciones en lugar de pruebas. La prevención de la infección asintomática no es una justificación viable para promover la vacunación de la población en general.
4. En la mayoría de los países, la mayoría de las personas ahora tienen inmunidad al SARS-CoV-2 [ 19 ]. Dependiendo de su grado de inmunidad cruzada previamente adquirida, no habrán tenido síntomas, síntomas leves y poco característicos, o síntomas más severos, posiblemente incluyendo anosmia (pérdida del sentido del olfato) u otros signos algo característicos de la enfermedad COVID-19. Independientemente de la gravedad de la enfermedad, ahora tendrán suficiente inmunidad para protegerse de enfermedades graves en caso de una nueva exposición. Esta mayoría de la población no se beneficiará en absoluto de la vacunación.
5. La supervivencia de la población de K0 B¡T supera el 99,8% a nivel mundial [ 20-22 ]. En los países que han estado intensamente infectados durante varios meses, menos del 0,2% de la población ha muerto y sus muertes se han clasificado como ‘con K0 B¡T’. El K0 B¡T también suele ser una enfermedad de leve a moderadamente grave. Por lo tanto, la inmensa mayoría de las personas no corren riesgo de contraer K0 B¡T y no requieren vacunación para su propia protección.
6. En aquellos susceptibles a una infección grave, K0 B¡T es una enfermedad tratable. Una convergencia de pruebas indica que el tratamiento temprano con los fármacos existentes reduce la hospitalización y la mortalidad en aproximadamente un 85% y un 75%, respectivamente [ 23-27 ]. Estos medicamentos incluyen muchos medicamentos antiinflamatorios, antivirales y anticoagulantes probados y verdaderos, así como anticuerpos monoclonales, zinc y vitaminas C y D.
Las decisiones de la industria y del gobierno de dejar de lado estos tratamientos probados a través del apoyo a la investigación selectiva [ 24 ], el sesgo regulatorio e incluso las sanciones directas contra los médicos que se atreven a usar dichos tratamientos por su propia iniciativa, han estado fuera de sintonía con las leyes existentes, la práctica médica estándar y investigar; el requisito legal de considerar las pruebas del mundo real se ha quedado en el camino [ 28 ].
La negación y denigración sistemática de estas terapias efectivas ha apuntalado la falsa justificación para la autorización de uso de emergencia de las vacunas, que requiere que “no se disponga de un tratamiento estándar aceptable” [ 29 ]. En pocas palabras, las vacunas no son necesarias para prevenir enfermedades graves.
2. LAS VACUNAS CARECEN DE EFICACIA
1. A nivel mecanicista, el concepto de inmunidad al K0 B¡T mediante la inducción de anticuerpos, según la vacuna K0 B¡T, es una equivocación médica. Los virus transmitidos por el aire, como el SARS-CoV-2, ingresan al cuerpo a través de las vías respiratorias y los pulmones, donde las concentraciones de anticuerpos son demasiado bajas para prevenir infecciones. Los anticuerpos inducidos por vacunas circulan principalmente en el torrente sanguíneo, mientras que las concentraciones en las membranas mucosas de los pulmones y las vías respiratorias son bajas.
Dado que K0 B¡T se propaga y causa principalmente enfermedades al infectar estas membranas mucosas, las vacunas pierden la marca inmunológica. Los documentos presentados por los fabricantes de vacunas a los distintos organismos reguladores no contienen evidencia de que la vacunación prevenga la infección de las vías respiratorias, lo que sería crucial para romper la cadena de transmisión. Por lo tanto, las vacunas son inmunológicamente inapropiadas para K0 B¡T.
2. Se desconoce la eficacia de la vacuna a medio y largo plazo. Los ensayos de fase 3, a mediano plazo, de 24 meses no estarán completos hasta 2023: no hay datos longitudinales a mediano o largo plazo con respecto a la eficacia de la vacuna COVID-19.
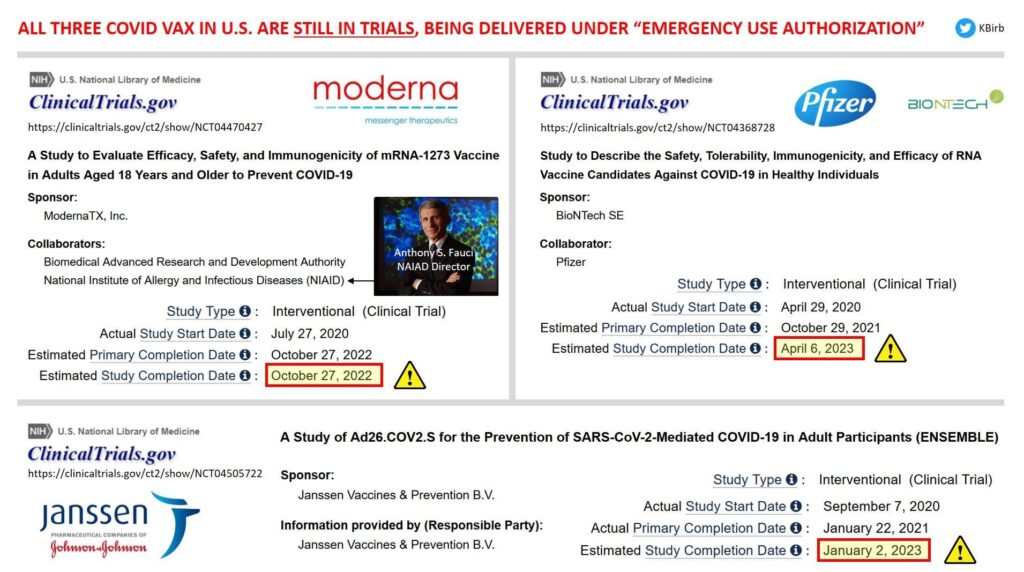
3. Los datos a corto plazo no han establecido la prevención de enfermedades graves. La Agencia Europea de Medicamentos ha señalado sobre la vacuna Comirnaty (ARNm de Pfizer) que los casos graves de K0 B¡T “fueron raros en el estudio y no se pueden extraer conclusiones estadísticamente seguras” [ 30 ]. De manera similar, el documento de Pfizer presentado a la FDA [ 31 ] concluye que no se pudo demostrar la eficacia contra la mortalidad. Por lo tanto, no se ha demostrado que las vacunas prevengan la muerte o enfermedades graves, incluso a corto plazo.
4. Se desconocen los correlatos de la protección contra COVID-19. Los investigadores aún no han establecido cómo medir la protección contra COVID-19. Como resultado, los estudios de eficacia están avanzando en la oscuridad. Después de la finalización de los estudios de Fase 1 y 2, por ejemplo, un artículo en la revista Vaccine señaló que «sin comprender los correlatos de protección, es imposible abordar actualmente las preguntas sobre la protección asociada a la vacuna, el riesgo de reinfección de K0 B¡T, la inmunidad colectiva y la posibilidad de eliminación del SARS-CoV-2 de la población humana ”[ 32 ]. Por lo tanto, la eficacia de la vacuna no se puede evaluar porque aún no hemos establecido cómo medirla.
3. LAS VACUNAS SON PELIGROSAS
1. Así como se predijo que fumar podría causar cáncer de pulmón según los primeros principios, se puede esperar que todas las vacunas basadas en genes causen coagulación sanguínea y trastornos hemorrágicos [ 33 ], según sus mecanismos moleculares de acción. De acuerdo con esto, se han observado enfermedades de este tipo en todos los grupos de edad, lo que ha llevado a suspensiones temporales de vacunas en todo el mundo: las vacunas no son seguras.
2. Contrariamente a las afirmaciones de que los trastornos sanguíneos posteriores a la vacunación son «raros», muchos efectos secundarios comunes de la vacuna (dolores de cabeza, náuseas, vómitos y «erupciones» similares a hematomas en el cuerpo) pueden indicar trombosis y otras anomalías graves . Además, las microtrombosis difusas inducidas por la vacuna en los pulmones pueden simular una neumonía y pueden diagnosticarse erróneamente como COVID-19. Los eventos de coagulación que actualmente reciben atención de los medios de comunicación probablemente sean solo la “punta de un enorme iceberg” [ 34 ]: las vacunas no son seguras.
3. Debido a la preparación inmunológica, se puede esperar que aumenten los riesgos de coagulación, sangrado y otros eventos adversos con cada revacunación y cada exposición al coronavirus que interviene. Con el tiempo, ya sean meses o años [ 35 ], esto hace que tanto la vacunación como los coronavirus sean peligrosos para los grupos de edad jóvenes y saludables, para quienes sin la inyeccion K0 B¡T no representa un riesgo sustancial. Desde el lanzamiento de la vacuna, la incidencia de K0 B¡T ha aumentado en numerosas áreas con altas tasas de vacunación [ 36-38 ].
Además, se han producido múltiples series de muertes por K0 B¡T poco después del inicio de las vacunaciones en hogares de ancianos [ 39,40 ]. Estos casos pueden deberse no sólo a la potenciación dependiente de anticuerpos, sino también a un efecto inmunosupresor general de las vacunas, sugerido por el aumento de la aparición de herpes zóster en determinados pacientes [ 41 ].
La inmunosupresión puede haber provocado la manifestación clínica de una infección previamente asintomática. Independientemente del mecanismo exacto responsable de estas muertes informadas, debemos esperar que las vacunas aumenten en lugar de disminuir la letalidad de K0 B¡T; las vacunas no son seguras.
4. Las vacunas son experimentales por definición. Permanecerán en los ensayos de fase 3 hasta 2023. Los receptores son sujetos humanos con derecho al consentimiento informado libre en virtud de Nuremberg y otras protecciones, incluida la resolución 2361 de la Asamblea Parlamentaria del Consejo de Europa [ 43 ] y las condiciones de autorización de uso de emergencia de la FDA [ 29 ]. Con respecto a los datos de seguridad de los ensayos de Fase 1 y 2, a pesar de los tamaños de muestra inicialmente grandes, la revista Vaccine informa que “la estrategia de vacunación elegida para un mayor desarrollo puede haberse dado a tan solo 12 participantes” [ 32 ].
Con tamaños de muestra tan extremadamente pequeños, la revista señala que «serán necesarios estudios de Fase 3 más grandes realizados durante períodos de tiempo más largos» para establecer la seguridad. Los riesgos que quedan por evaluar en los ensayos de fase 3 hasta 2023, con poblaciones enteras como sujetos, incluyen no solo trombosis y anomalías hemorrágicas, sino también otras respuestas autoinmunes, reacciones alérgicas, tropismos desconocidos (destinos tisulares) de nanopartículas lipídicas [ 35 ], anticuerpos. -mejora dependiente [ 43-46 ] y el impacto de métodos de fabricación apresurados, ejecutados de manera cuestionable, mal regulados [ 47 ] y supuestamente inconsistentes, lo que confiere riesgos de impurezas potencialmente dañinas como residuos de ADN no controlados [ 48]. Las vacunas no son seguras, ni para los destinatarios ni para quienes las administran o autorizan su uso.
5. La experiencia inicial podría sugerir que las vacunas derivadas de adenovirus (AstraZeneca / Johnson & Johnson) causan efectos adversos más graves que las vacunas de ARNm (Pfizer / Moderna). Sin embargo, tras la inyección repetida, la primera pronto inducirá anticuerpos contra las proteínas del vector de adenovirus. Luego, estos anticuerpos neutralizarán la mayoría de las partículas del virus de la vacuna y provocarán su eliminación antes de que puedan infectar cualquier célula, lo que limitará la intensidad del daño tisular.
Por el contrario, en las vacunas de ARNm, no hay antígeno proteico que los anticuerpos reconozcan. Por lo tanto, independientemente del grado de inmunidad existente, el ARNm de la vacuna alcanzará su objetivo: las células del cuerpo. Estos luego expresarán la proteína de pico y posteriormente sufrirán el ataque completo del sistema inmunológico.
Con las vacunas de ARNm, está prácticamente garantizado que el riesgo de eventos adversos graves aumentará con cada inyección sucesiva. Por tanto, a largo plazo, son incluso más peligrosas que las vacunas de vectores. Su aparente preferencia sobre este último es preocupante en el más alto grado; estas vacunas no son seguras.
4. ASPECTOS ÉTICOS Y LEGALES A TENER EN CUENTA
Los conflictos de intereses abundan en la literatura científica y dentro de las organizaciones que recomiendan y promueven vacunas, mientras que demonizan estrategias alternativas (dependencia de la inmunidad natural y tratamiento temprano). Las autoridades, los médicos y el personal médico deben protegerse evaluando muy de cerca las fuentes de su información en busca de conflictos de intereses.
Las autoridades, los médicos y el personal médico deben tener el mismo cuidado de no ignorar la literatura creíble e independiente sobre la necesidad, seguridad y eficacia de las vacunas, dadas las previsibles muertes masivas y los daños que deben esperarse a menos que se detenga la campaña de vacunación.
Los fabricantes de vacunas se han eximido de responsabilidad legal por eventos adversos por una razón. Cuando ocurren muertes y daños por vacunas, la responsabilidad recaerá en los responsables de la autorización, administración y / o coerción de las vacunas mediante pasaportes de vacunas, ninguno de los cuales puede justificarse en un análisis de riesgo-beneficio sobrio y basado en evidencia.
Todos los actores políticos, regulatorios y médicos involucrados en la vacunación COVID-19 deben familiarizarse con el código de Nuremberg y otras disposiciones legales para protegerse.




