SARS–CoV–2 Spike Impairs DNA Damage Repair and Inhibits V(D)J Recombination In Vitro DOI: 10.3390/v13102056 – Hui Jiang , Ya-Fang Mei

Una nueva y sorprendente investigación publicada en Virus , que forma parte de la edición de las interacciones de la célula huésped SARS-CoV-2 de MDPI (Open Access Journals). El artículo de investigación se titula “El proteina pico del SARS – CoV – 2 afecta la reparación del daño del ADN e inhibe la recombinación de V (D) J in vitro” y está escrito por Hui Jiang y Ya-Fang Mei, del Departamento de Biociencias Moleculares, The Wenner– Instituto Gren, Universidad de Estocolmo, SE-10691 Estocolmo, Suecia, y el Departamento de Microbiología Clínica, Virología, Universidad de Umeå, SE-90185 Umeå, Suecia, respectivamente.
Hemos guardado una copia del trabajo de investigación en un documento PDF en servidores privados en caso de que lo retiren sin aviso ni dar razones, como esta pasando con otros estudios opuestos al relato de los laboratorios.
En la conclusión del artículo, los autores escriben: “Encontramos que la proteína de pico inhibió marcadamente la formación de focos BRCA1 y 53BP1 (Figura 3D-G). Juntos, estos datos muestran que la proteína espiga (spike) de longitud completa del SARS-CoV-2 inhibe la reparación del daño del ADN al obstaculizar el reclutamiento de la proteína de reparación del ADN «.
El mecanismo de reparación del ADN, conocido como NHEJ (Non-Homologous End Joining – unión de extremos no homólogos) es una especie de sistema de «respuesta de emergencia» intracelular que repara las roturas del ADN de doble hebra. Sin el mecanismo NHEJ, toda la vida multicelular avanzada dejaría de existir. Ningún ser humano, animal o planta puede sobrevivir sin la integridad de su código genético y estar protegida y constantemente reparada a través de múltiples mecanismos.
El daño al ADN puede ser causado por la exposición a la radiación, a los productos químicos que se encuentran en los alimentos y productos de cuidado personal, o incluso a la exposición al equipo de mamografía. La exposición excesiva a la luz solar también puede causar roturas del ADN, y las mutaciones menores del ADN ocurren espontáneamente en todos los organismos vivos. Los pilotos de líneas aéreas, por ejemplo, se exponen habitualmente a la radiación ionizante debido a volar en altitud.
En una persona normal y sana, el mecanismo NHEJ repara el ADN y evita que se produzca una mutación patógena. Pero en presencia de la proteína de pico de la vacuna, la efectividad del NHEJ se suprime hasta en un 80% , lo que significa que no puede realizar sus funciones debido a la capacidad suprimida de reclutar proteínas para su reparación.
Como resultado, los siguientes «errores» se introducen en los cromosomas dentro de los núcleos de las células humanas, todo debido a la presencia de la proteína de pico (spike) de las inyecciones de ARNm:
- Mutaciones o «errores» en la secuencia genética.
- Supresiones de segmentos enteros de código genético.
- Inserciones de segmentos incorrectos.
- Mezcla y emparejamiento / permutaciones de código genético.
Estos errores, cuando se expresan a través de la división y replicación celular, dan como resultado:
- Cáncer y tumores cancerosos en todo el cuerpo.
- Pérdida de producción de células T y B del sistema inmunológico (es decir, inmunodeficiencia inducida)
- Trastornos autoinmunes
- Envejecimiento acelerado y reducción de la longitud de los telómeros.
- Pérdida de funcionamiento de sistemas de órganos complejos como circulatorio, neurológico, endocrino, musculoesquelético, etc.
- Daño celular que se asemeja al envenenamiento por radiación cuando las células se destruyen a sí mismas desde adentro
Muchos de estos efectos son fatales. También pueden ocurrir lesiones debilitantes y disfunciones de órganos que requerirán una intervención médica de por vida.
La proteína de pico (spike) entra en el núcleo de la célula.
«Mecánicamente, encontramos que la proteína de pico se localiza en el núcleo e inhibe la reparación del daño del ADN al impedir el reclutamiento de las proteínas BRCA1 y 53BP1 de reparación del ADN clave en el sitio del daño». (Mechanistically, we found that the spike protein localizes in the nucleus and inhibits DNA damage repair by impeding key DNA repair protein BRCA1 and 53BP1 recruitment to the damage site. Our findings reveal a potential molecular mechanism by which the spike protein might impede adaptive immunity and underscore the potential side effects of full-length spike-based vaccines.)
Esto significa que la proteína de pico, que se genera en los ribosomas celulares después de que las células han sido afectadas por las inyecciones de ARNm, no siempre sale de la célula y entra en el torrente sanguíneo como se ha dicho. En algunos casos, la proteína espiga (spike) ingresa al núcleo celular . Allí, interfiere con el mecanismo de reparación del ADN como se describe a lo largo de este artículo.
«Sorprendentemente, encontramos la abundancia de la proteína de pico en el núcleo» (Figura 1A)», concluyeron los autores del estudio. (Surprisingly, we found the abundance of the spike protein in the nucleus)
Esto significa, sin lugar a dudas, que las inyecciones de ARNm provocan alteraciones cromosómicas en las células del cuerpo . Es una confirmación de que tales inyecciones están, de hecho, causando modificaciones en la integridad genética y exhibiendo efectos secundarios que no han sido previstos o descritos por los fabricantes de la vacuna de ARNm.
El Dr. Thomas Levy escribe sobre la toxicidad de la proteína de pico en Orthomolecular.org :
Se ha expresado preocupación con respecto a la diseminación de la proteína de pico por todo el cuerpo después de la vacunación. En lugar de permanecer localizado en el lugar de la inyección para provocar la respuesta inmune y nada más, se ha detectado la presencia de proteína de pico en todo el cuerpo de algunos individuos vacunados. Además, parece que algunas de las proteínas de pico circulantes simplemente se unen a los receptores ACE2 sin entrar en la célula, induciendo una respuesta autoinmune a toda la entidad de proteína de pico celular. Dependiendo del tipo de célula que se une a la proteína de pico, puede producirse cualquiera de una serie de afecciones médicas autoinmunes.
Lo que es más alarmante, el Dr. Levy explica que la evidencia actual muestra que la proteína de pico continúa produciéndose en el cuerpo, luego de la inyección inicial de ARNm . El explica:
Si bien la patología subyacente aún no se ha definido por completo, una explicación de los problemas con las tendencias trombóticas y otra sintomatología observada en los pacientes con COVID crónico y posvacunación se relaciona directamente con la presencia persistente de la parte proteica del pico del coronavirus. Algunos informes afirman que la proteína de pico se puede seguir produciendo después de la unión inicial a los receptores ACE2 y la entrada en algunas de las células a las que se dirige inicialmente. Los cuadros clínicos del COVID crónico y la toxicidad posterior a la vacuna parecen muy similares, y es probable que ambos se deban a esta presencia continua y diseminación por todo el cuerpo de la proteína de pico (Mendelson et al., 2020; Aucott y Rebman, 2021; Levy , 2021; Raveendran, 2021).
La proteína de pico de longitud completa resultó en la mayor supresión del mecanismo de reparación del ADN NHEJ
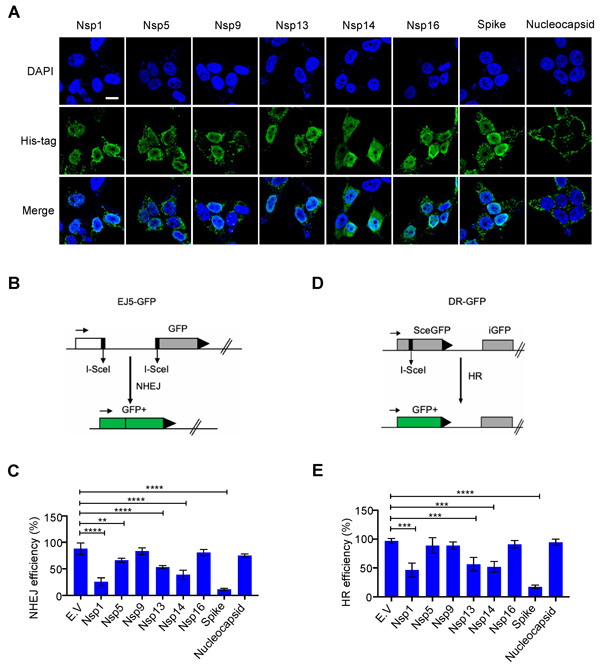
Vea las figuras a continuación. Los fragmentos virales del SARS-CoV-2 se denominan “Nsp1, Nsp5” y así sucesivamente. El pico de longitud completa se llama «pico» y la nucleocápside, otra parte estructural del patógeno de la proteína de pico completo, se identifica por separado.
Del estudio:
La sobreexpresión de Nsp1, Nsp5, Nsp13, Nsp14 y las proteínas de pico disminuyeron las eficiencias de reparación de HR y NHEJ (Figura 1B-E y Figura S2A, B).
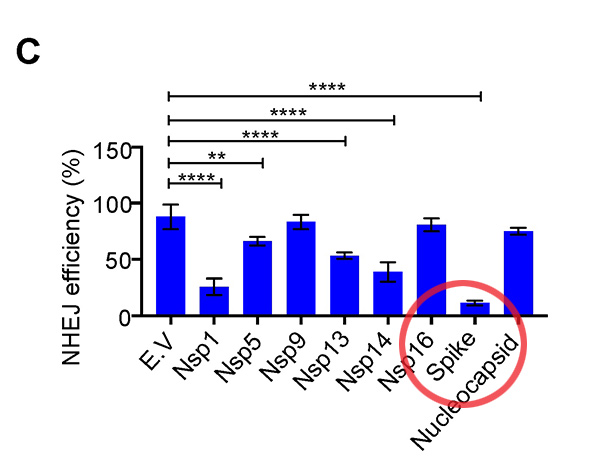
Las Figuras C y E muestran la supresión de la reparación de NHEJ por estas diversas porciones de fragmentos virales. (Vea las líneas gráficas verticales azules que representan los niveles de actividad / eficiencia del mecanismo de reparación del ADN).
Lo que muestran estos datos es que la mayor supresión de la actividad NHEJ se mide cuando está presente la proteína de pico completa. Del estudio:
Juntos, estos datos muestran que la proteína espiga de longitud completa del SARS-CoV-2 inhibe la reparación del daño del ADN al obstaculizar el reclutamiento de la proteína de reparación del ADN.
Esta es la proteína de pico que generan las propias células del cuerpo después de ser inyectada con una vacuna de ARNm:
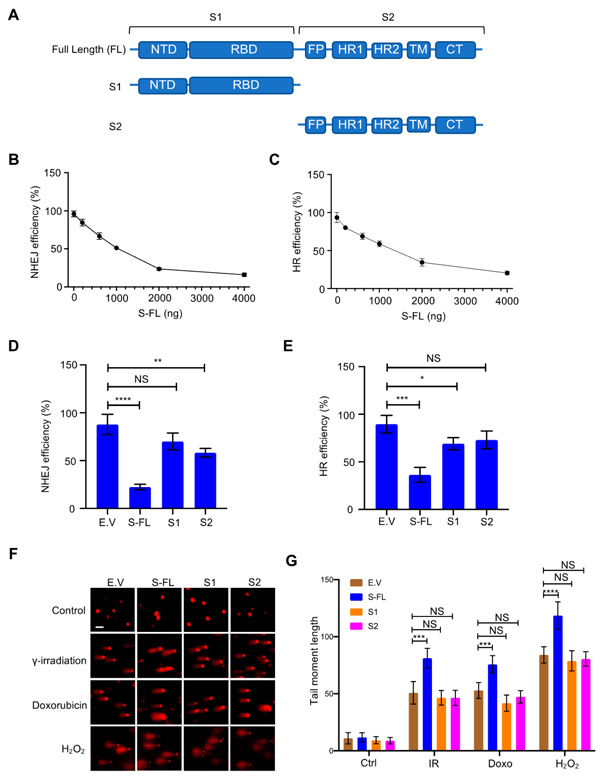
En la figura 2, a continuación, vemos que la supresión de la actividad NHEJ exhibe una respuesta dependiente de la dosis a la presencia de proteína de pico (figuras 2B y 2C). Esto indica que cuantas más proteínas espiga estén presentes, mayor será la supresión de la reparación del ADN:
La figura abajo a la derecha, 2G, muestra cómo la presencia de la proteína de pico inhibe la reparación del ADN después de varias agresiones al ADN, como radiación, exposición química u oxidación. Es importante destacar que, como explican los autores del estudio:
Después de diferentes tratamientos de daño del ADN, como la irradiación \ beta, el tratamiento con doxorrubicina y el tratamiento con H2O2, hay menos reparación en presencia de la proteína de la espiga (Figura 2F, G). Juntos, estos datos demuestran que la proteína de pico afecta directamente a la reparación del ADN en el núcleo.
La exposición a 5G, la exposición a estelas químicas, la exposición a productos químicos alimentarios, la mamografía e incluso la exposición a la luz solar causarán estragos en quienes hayan recibido inyecciones de ARNm
El resultado espantoso de este hallazgo es que las personas que han recibido inyecciones de ARNm experimentarán una reparación del ADN suprimida , lo que aumentará las exposiciones que alguna vez se pensó que eran problemas menores a amenazas significativas para su salud.
En otras palabras, las personas expuestas a la radiación 5G, los exámenes de mamografía, los plastificantes químicos en los productos alimenticios y los carcinógenos en los productos de cuidado personal (detergentes para ropa, perfumes, champús, lociones para la piel, etc.) no podrán reparar el daño del ADN causado por estas exposiciones. Después de exposiciones relativamente pequeñas, comenzarán a mutar y desarrollar cánceres.
Esto incluso podría describirse como una especie de sistema de armas binarias en el que las inyecciones de ARNm debilitan la reparación del ADN, y la exposición a 5G (o exposición química en el suministro de alimentos) proporciona el arma que rompe las cadenas de ADN y hace que el cuerpo no pueda mantener la integridad genética durante replicación celular.
La presencia de la proteína de pico interfiere con la función inmunológica normal y conduce a una inmunodeficiencia (una condición similar al SIDA)
Esta investigación también encuentra que las proteínas de pico de las inyecciones de ARNm pueden conducir a condiciones de inmunodeficiencia, similares al SIDA. Esto es consistente con lo informado anteriormente acerca de la disminución de la función inmunológica de aproximadamente un 5% por semana en aquellos que han recibido inyecciones contra la k0 bit. Del estudio:
… [La] pérdida de función de proteínas clave de reparación del ADN como ATM, DNA – PKcs, 53BP1, et al., Conduce a defectos en la reparación de NHEJ que inhiben la producción de células B y T funcionales, lo que conduce a inmunodeficiencia.
La función inmunológica también se ve críticamente afectada por la presencia de la proteína de pico, lo que puede provocar mutaciones cancerosas en todas las células del cuerpo. Como explica el estudio:
La reparación del daño del ADN, especialmente la reparación del NHEJ, es esencial para la recombinación V (D) J, que se encuentra en el núcleo de la inmunidad de las células B y T.
Como también explica Science Direct :
Mantener la integridad genómica es imperativo para la supervivencia de un organismo. Entre los diferentes daños del ADN, las roturas de doble hebra (DSB) se consideran las más perjudiciales, ya que pueden provocar la muerte celular si no se reparan o reordenamientos cromosómicos cuando se reparan incorrectamente, lo que lleva al cáncer.
Además, las mutaciones en los genes NHEJ, incluidos Ku70 y Ku80, se han asociado con una menor esperanza de vida en ratones [54]. Además, los defectos en el ADN-PKcs (proteína quinasa dependiente del ADN) provocaron un deterioro del mantenimiento de los telómeros y una reducción de la vida útil de los ratones [55]. En conjunto, estas líneas de evidencia sugieren que NHEJ juega un papel importante en la prevención del aumento relacionado con la edad en la inestabilidad genómica y el deterioro funcional.
En efecto, esto significa que la supresión del mecanismo de reparación del ADN NHEJ por parte de la proteína de pico también conduce a una vida útil reducida y un envejecimiento acelerado .
Ahora tenemos otra comprensión más profunda de los mecanismos por los cuales pueden ocurrir estas muertes inducidas por inyecciones de ARNm.
Colabore con Nosotros, sea parte del equipo click aqui , su participación es fundamental! ayuda a que podamos llegar a mas indecisos y seamos cada vez más los que defendemos a nuestros hijos e hijas…
Bill Gates poseía una gran participación en el fabricante de remdesivir, Gilead. [124] Los propios estudios de la OMS mostraron claramente, como incluso la OMS reconoció, que el remdesivir no era útil contra el COVID. [125] Peor aún, la extrema toxicidad del fármaco (los efectos secundarios del remdesivir imitan los síntomas de la última etapa del COVID [126 , 127] ) en realidad puede empeorar la gravedad de la enfermedad. [128] Para superar estos obstáculos, el Dr. Fauci financió y manipuló una serie de estudios defectuosos para sugerir, engañosamente, que remdesivir podría reducir levemente la cantidad de días que un paciente permanecería en el hospital. [129] Los estudios mucho más amplios de la OMS demostraron que no hubo reducción en la duración de la estancia hospitalaria. Sin embargo, utilizando su “investigación” descaradamente orquestada, el Dr. Fauci forzó la aprobación de remdesivir a través de la FDA como “estándar de atención” para COVID. Al mismo tiempo, el Dr. Fauci y Bill Gates estaban financiando y promoviendo estudios para desacreditar la cloroquina y la hidroxicloroquina y sabotear la ivermectina, dos remedios efectivos contra el COVID que representaban una amenaza existencial para el remdesivir y toda la empresa de vacunas contra el COVID de Fauci/Gates.
Extractado de el libro de Robert Kennedy Jr. sobre Fauci, ver mas en : https://cienciaysaludnatural.com/la-historia-criminal-del-dr-anthony-fauci-documentada-en-un-libro-de-robert-kennedy-jr/
- Gilead Sciences, Inc., U.S. Securities and Exchange Commission, Form 10-K (Dec. 31, 2005), sec.gov/Archives/edgar/data/882095/000119312506045128/d10k.htm
- World Health Organization, “WHO recommends against the use of remdesivir in COVID-19 patients” (Nov 20, 2020), who.int/news-room/feature-stories/detail/who-recommends-against-the-use-of-remdesivir-in-covid-19-patients
- Drugs.com, Remdesivir Side Effects (Feb 13, 2021), drugs.com/sfx/remdesivir-side-effects.html
- Centers for Disease Control and Prevention, Symptoms of COVID-19 (Feb. 22, 2021), cdc.gov/coronavirus/2019-ncov/symptoms-testing/symptoms.html
- Jason D. Goldman et al., “Remdesivir for 5 or 10 Days in Patients with Severe Covid-19,” New England Journal of Medicine (May 27, 2020), nejm.org/doi/full/10.1056/NEJMoa2015301
- John H. Beigel et al., “Remdesivir for the Treatment of Covid-19—Final Report,” New England Journal of Medicine (Oct. 8, 2020), nejm.org/doi/10.1056/NEJMoa2007764
Ver más sobre este tema en
https://cienciaysaludnatural.com/farmacocinetica-y-toxicidad-de-la-inyeccion-de-arnm-de-pfizer/ https://cienciaysaludnatural.com/la-proteina-espiga-es-la-responsable-de-los-efectos-adversos-en-las-vacunas-k0-b1t/
Referencias
- V’Kovski, P.; Kratzel, A.; Steiner, S.; Stalder, H.; Thiel, V. Coronavirus biology and replication: Implications for SARS-CoV-2. Nat. Rev. Microbiol. 2021, 19, 155–170. [Google Scholar] [CrossRef]
- Suryawanshi, R.K.; Koganti, R.; Agelidis, A.; Patil, C.D.; Shukla, D. Dysregulation of Cell Signaling by SARS-CoV-2. Trends Microbiol. 2021, 29, 224–237. [Google Scholar] [CrossRef]
- Qin, C.; Zhou, L.; Hu, Z.; Zhang, S.; Yang, S.; Tao, Y.; Xie, C.; Ma, K.; Shang, K.; Wang, W.; et al. Dysregulation of Immune Response in Patients With Coronavirus 2019 (COVID-19) in Wuhan, China. Clin. Infect. Dis. 2020, 71, 762–768. [Google Scholar] [CrossRef] [PubMed]
- Wang, F.; Nie, J.; Wang, H.; Zhao, Q.; Xiong, Y.; Deng, L.; Song, S.; Ma, Z.; Mo, P.; Zhang, Y. Characteristics of Peripheral Lymphocyte Subset Alteration in COVID-19 Pneumonia. J. Infect. Dis. 2020, 221, 1762–1769. [Google Scholar] [CrossRef] [PubMed]
- Zhang, G.; Nie, S.; Zhang, Z.; Zhang, Z. Longitudinal Change of Severe Acute Respiratory Syndrome Coronavirus 2 Antibodies in Patients with Coronavirus Disease 2019. J. Infect. Dis. 2020, 222, 183–188. [Google Scholar] [CrossRef] [PubMed]
- Long, Q.X.; Liu, B.Z.; Deng, H.J.; Wu, G.C.; Deng, K.; Chen, Y.K.; Liao, P.; Qiu, J.F.; Lin, Y.; Cai, X.F.; et al. Antibody responses to SARS-CoV-2 in patients with COVID-19. Nat. Med. 2020, 26, 845–848. [Google Scholar] [CrossRef]
- Bednarski, J.J.; Sleckman, B.P. Lymphocyte development: Integration of DNA damage response signaling. Adv. Immunol. 2012, 116, 175–204. [Google Scholar] [PubMed]
- Malu, S.; Malshetty, V.; Francis, D.; Cortes, P. Role of non-homologous end joining in V(D)J recombination. Immunol. Res. 2012, 54, 233–246. [Google Scholar] [CrossRef]
- Bednarski, J.J.; Sleckman, B.P. At the intersection of DNA damage and immune responses. Nat. Rev. Immunol. 2019, 19, 231–242. [Google Scholar] [CrossRef]
- Gapud, E.J.; Sleckman, B.P. Unique and redundant functions of ATM and DNA-PKcs during V(D)J recombination. Cell. Cycle 2011, 10, 1928–1935. [Google Scholar] [CrossRef]
- Difilippantonio, S.; Gapud, E.; Wong, N.; Huang, C.Y.; Mahowald, G.; Chen, H.T.; Kruhlak, M.J.; Callen, E.; Livak, F.; Nussenzweig, M.C.; et al. 53BP1 facilitates long-range DNA end-joining during V(D)J recombination. Nature 2008, 456, 529–533. [Google Scholar] [CrossRef] [PubMed]
- Schwarz, K.B. Oxidative stress during viral infection: A review. Free Radic. Biol. Med. 1996, 21, 641–649. [Google Scholar] [CrossRef]
- Xu, L.H.; Huang, M.; Fang, S.G.; Liu, D.X. Coronavirus infection induces DNA replication stress partly through interaction of its nonstructural protein 13 with the p125 subunit of DNA polymerase delta. J. Biol. Chem. 2011, 286, 39546–39559. [Google Scholar] [CrossRef] [PubMed]
- Delgado-Roche, L.; Mesta, F. Oxidative Stress as Key Player in Severe Acute Respiratory Syndrome Coronavirus (SARS-CoV) Infection. Arch. Med. Res. 2020, 51, 384–387. [Google Scholar] [CrossRef] [PubMed]
- Pierce, A.J.; Hu, P.; Han, M.; Ellis, N.; Jasin, M. Ku DNA end-binding protein modulates homologous repair of double-strand breaks in mammalian cells. Genes Dev. 2001, 15, 3237–3242. [Google Scholar] [CrossRef]
- Bennardo, N.; Cheng, A.; Huang, N.; Stark, J.M. Alternative-NHEJ is a mechanistically distinct pathway of mammalian chromosome break repair. PLoS Genet. 2008, 4, e1000110. [Google Scholar] [CrossRef]
- Sadofsky, M.J.; Hesse, J.E.; McBlane, J.F.; Gellert, M. Expression and V(D)J recombination activity of mutated RAG-1 proteins. Nucleic Acids Res. 1993, 21, 5644–5650. [Google Scholar] [CrossRef]
- Trancoso, I.; Bonnet, M.; Gardner, R.; Carneiro, J.; Barreto, V.; Demengeot, J.; Sarmento, L. A Novel Quantitative Fluorescent Reporter Assay for RAG Targets and RAG Activity. Front. Immunol. 2013, 4, 110. [Google Scholar] [CrossRef]
- Zhang, J.; Cruz-cosme, R.; Zhuang, M.-W.; Liu, D.; Liu, Y.; Teng, S.; Wang, P.-H.; Tang, Q. A systemic and molecular study of subcellular localization of SARS-CoV-2 proteins. Signal Transduct. Target. Ther. 2020, 5, 269. [Google Scholar] [CrossRef]
- Shang, J.; Wan, Y.; Luo, C.; Ye, G.; Geng, Q.; Auerbach, A.; Li, F. Cell entry mechanisms of SARS-CoV-2. Proc. Natl. Acad. Sci. USA 2020, 117, 11727–11734. [Google Scholar] [CrossRef]
- Du, L.; He, Y.; Zhou, Y.; Liu, S.; Zheng, B.J.; Jiang, S. The spike protein of SARS-CoV—A target for vaccine and therapeutic development. Nat. Rev. Microbiol. 2009, 7, 226–236. [Google Scholar] [CrossRef] [PubMed]
- Huang, Y.; Yang, C.; Xu, X.F.; Xu, W.; Liu, S.W. Structural and functional properties of SARS-CoV-2 spike protein: Potential antivirus drug development for COVID-19. Acta Pharmacol. Sin. 2020, 41, 1141–1149. [Google Scholar] [CrossRef] [PubMed]
- Hoffmann, M.; Kleine-Weber, H.; Schroeder, S.; Kruger, N.; Herrler, T.; Erichsen, S.; Schiergens, T.S.; Herrler, G.; Wu, N.H.; Nitsche, A.; et al. SARS-CoV-2 Cell Entry Depends on ACE2 and TMPRSS2 and Is Blocked by a Clinically Proven Protease Inhibitor. Cell 2020, 181, 271–280.e8. [Google Scholar] [CrossRef]
- Hsu, A.C.-Y.; Wang, G.; Reid, A.T.; Veerati, P.C.; Pathinayake, P.S.; Daly, K.; Mayall, J.R.; Hansbro, P.M.; Horvat, J.C.; Wang, F.; et al. SARS-CoV-2 Spike protein promotes hyper-inflammatory response that can be ameliorated by Spike-antagonistic peptide and FDA-approved ER stress and MAP kinase inhibitors in vitro. bioRxiv 2020, 2020, 317818. [Google Scholar]
- Poland, G.A.; Ovsyannikova, I.G.; Kennedy, R.B. SARS-CoV-2 immunity: Review and applications to phase 3 vaccine candidates. Lancet 2020, 396, 1595–1606. [Google Scholar] [CrossRef]
- Davanzo, G.G.; Codo, A.C.; Brunetti, N.S.; Boldrini, V.; Knittel, T.L.; Monterio, L.B.; de Moraes, D.; Ferrari, A.J.R.; de Souza, G.F.; Muraro, S.P.; et al. SARS-CoV-2 Uses CD4 to Infect T Helper Lymphocytes. medRxiv 2020, 2020, 20200329. [Google Scholar]
- Borsa, M.; Mazet, J.M. Attacking the defence: SARS-CoV-2 can infect immune cells. Nat. Rev. Immunol. 2020, 20, 592. [Google Scholar] [CrossRef]
- Barberis, E.; Vanella, V.V.; Falasca, M.; Caneapero, V.; Cappellano, G.; Raineri, D.; Ghirimoldi, M.; De Giorgis, V.; Puricelli, C.; Vaschetto, R.; et al. Circulating Exosomes Are Strongly Involved in SARS-CoV-2 Infection. Front. Mol. Biosci. 2021, 8, 632290. [Google Scholar] [CrossRef]
- Sur, S.; Khatun, M.; Steele, R.; Isbell, T.S.; Ray, R.; Ray, R.B. Exosomes from COVID-19 patients carry tenascin-C and fibrinogen-β in triggering inflammatory signals in distant organ cells. bioRxiv 2021, 2021, 430369. [Google Scholar]