En recientes análisis de del British Journal of Medicine (BJM) se describe el manejo de la Organización Mundial de la Salud OMS con la vacuna contra la malaria en África. Profesores Peter Aaby y Christine Stabell Benn, autores del análisis del BMJ, cuestionan seguridad de esta vacuna.
En 1978, el profesor Aaby estableció el Proyecto de Salud Bandim (BHP). El BHP llevaba un sistema de vigilancia demográfica en Guinea Bissau en África Occidental. En ese momento, la mortalidad infantil era muy alta en Guinea-Bissau. Se asumió que la causa principal era la desnutrición. El programa de vacunación de la comunidad en Guinea Bissau se inició en 1981 bajo la dirección de Aaby. Más tarde, en 1986, se implementó un programa nacional con el apoyo de UNICEF que hoy continua.
El Dr. Aaby y su equipo de investigación descubrieron que la nueva vacuna de sarampión estaba asociada con dos veces mayor mortalidad femenina . Hallazgos similares se observaron en Haití y Sudán por otros investigadores. Después de ignorar los hallazgos de Aaby, la OMS finalmente retiró la nueva vacuna contra el sarampión “ sin explicación valedera ” ni tampoco hizo “ ningún intento de aclarar lo que había sucedido. ” Como Aaby explica:
“La vacuna que es protectora contra una enfermedad específica, pero puede estar altamente asociada con la mortalidad … que no figura en ninguna parte de los libros de medicina”.
Volviendo a la actualidad en estos dias en África, se estan haciendo los ensayos de fase III de la vacuna contra la malaria RTS, S / AS01 y se identificaron tres problemas de seguridad:
- un mayor riesgo de meningitis,
- malaria cerebral,
- y se duplicó la mortalidad femenina.
Dice Aaby en su articulo del BJM mencionado al principio :
“Una decisión después de 24 meses es muy temprana el estudio podría estar sesgado a favor de la vacuna, que fue más eficaz en el primer año de seguimiento que en la fase III de ensayos; los riesgos relativos de la malaria cerebral y la mortalidad femenina aumentaron después de la dosis de refuerzo a los 20 meses”
Aaby ha sido reconocido por las comunidades científicas y médicas por su estudio del 2018 titulado «La evidencia de aumento de la mortalidad después de la introducción de la difteria-tétanos-tos ferina vacuna a niños de 6-35 meses en Guinea Bissau «. Aaby y su equipo llegaron a a conclusión:
“… los niños vacunados con DTP de 6-35 meses de edad tienden a tener una mayor mortalidad que los niños no vacunados con DTP. Todos los estudios de la introducción de la vacuna DTP han encontrado aumento de la mortalidad global “.
Aaby sugiere un enfoque científico y usar “la mortalidad global” para evaluar el desempeño de la vacuna en lugar de un marcador de posición artificial sustituto*. Además, recomiendan seguir estudios en las poblaciones por 4-5 años completos antes de usar la vacuna en otras partes.
* Los médicos se guían a menudo por marcadores “indirectos” en el manejo de los medicamentos, sobre todo en enfermedades crónicas. Marcador sustitutivo o “indirecto” puede ser un test de laboratorio o un signo que mide como un paciente se siente, funciona o sobrevive”. Los marcadores indirectos pueden conducir a la toma de decisiones erróneas si se utilizan para predecir riesgos de mortalidad.
La falta de controles y seguridad en la OMS no es sólo un incidente aislado en un continente lejano.
En 2017 La Red de Acción Informado Consentimiento (ICAN) solicitó legalmente al Departamento de Salud y Servicios Humanos (HHS), una lista de información básicas con respecto a sus obligaciones sobre el control de la seguridad de la vacunas.
Pero tuvieron que llegar a una disputa legal para que ICAN recibiera la documentación del HHS sobre las licencia de las vacunas recomendadas para los bebés y esta puso en evidencia que los estudios de seguimiento sobre el control y seguridad de las vacunas eran demasiado breves para determinar las condiciones de salud crónicas resultantes.
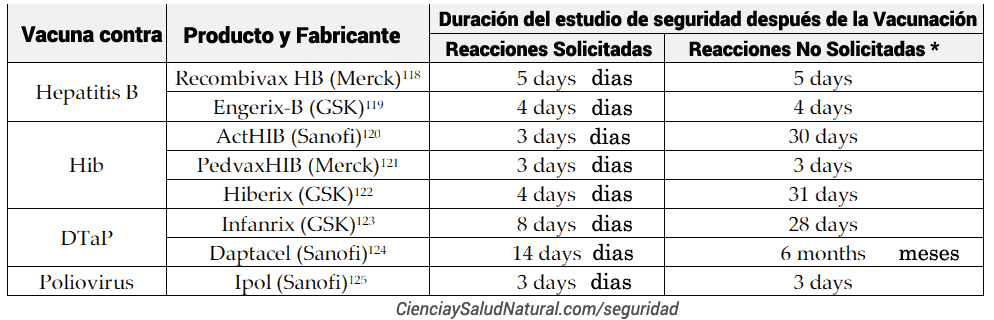
* En los ensayos clínicos, se busca, o se solicita signos y síntomas esperados después de la vacunación a los participantes. Cuando se les pide a los participantes que los informen espontáneamente se llama síntomas no solicitados. https://www.nature.com/articles/s41541-019-0132-6
ICAN también reclama al HHS el por qué no ha habido ningún intento de utilizar los datos del Vaccine Safety Datalink (VSD) para comparar los resultados de salud totales de vacunas entre poblaciones vacunadas y no vacunadas. Hay suficientes datos para comparar a vacunados vs. no vacunados pero este estudio fundamental no se lleva a cabo oficialmente.
Después de los científicos empezaron a tener acceso a la VSD para realizar estudios que revelan el daño de la vacuna, en el 2001 el HHS trasladó estos datos a una Asociación de la Industria de la Salud (Health industry trade association). Esto hizo que los datos del Vaccine Safety Datalink VSD ya no estén disponible para solicitar información a través del Freedom of Information Act (FOIA – Acta de Libertad de Información), y se aseguró que sólo los científicos para estudios que el HHS aprueba, pueden utilizar esta base de datos. Otros abusos y comportamientos no éticos se detallan aquí .
Estudios sin grupo de control o placebo
Según lo definido por los CDC, un «placebo» es: «Una sustancia o tratamiento que no tiene ningún efecto en los seres humanos» . Como el HHS sabe, los ejemplos comunes de un placebo son una inyección de solución salina o una píldora de azúcar. La razón por la que los medicamentos Primero se evalúa en un ensayo clínico contra un grupo de control con placebo, antes de ser lanzado al público, es para evaluar la seguridad y la eficacia del medicamento. Según lo explicado por HHS:
Al realizar un ensayo clínico, los investigadores no quieren dejar nada al azar. Quieren estar tan seguros como sea posible de que los resultados de las pruebas muestran si un tratamiento es seguro y efectivo. El «estándar de oro» para evaluar las intervenciones en personas es el ensayo clínico «aleatorizado, controlado con placebo». …
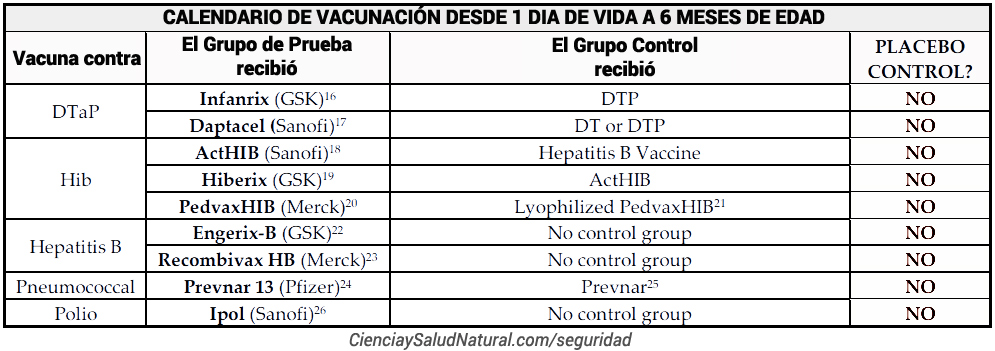
- 15 La mayoría de las vacunas tuvieron múltiples ensayos; algunos ensayos usaron un control y otros no, solo se enumera el control.
- 16 https://www.fda.gov/downloads/biologicsbloodvaccines/vaccines/approvedproducts/ucm124514.pdf
- 17 https://www.fda.gov/downloads/biologicsbloodvaccines/vaccines/approvedproducts/ucm103037.pdf (lists DT vaccine in one of its efficacy trials as a “placebo”)
- 18 https://www.fda.gov/downloads/BiologicsBloodVaccines/Vaccines/ApprovedProducts/UCM109841.pdf
- 19 https://www.fda.gov/downloads/BiologicsBloodVaccines/Vaccines/ApprovedProducts/UCM179530.pdf
- 20 https://www.fda.gov/downloads/BiologicsBloodVaccines/Vaccines/ApprovedProducts/UCM253652.pdf
- 21 En los ensayos previos a la licencia de PedvaxHIB liofilizado, el grupo de prueba recibió PedvaxHIB, OPV y DTP liofilizados, y el grupo de control recibió un placebo, OPV y DTP. Ibídem. La inyección concomitante de OPV y DTP niega el beneficio de tener un placebo, ya que evita evaluar el perfil de seguridad real entre PedvaxHIB liofilizado y un placebo.
- 22 https://www.fda.gov/downloads/BiologicsBloodVaccines/Vaccines/ApprovedProducts/UCM224503.pdf
- 23 https://www.fda.gov/downloads/BiologicsBloodVaccines/Vaccines/ApprovedProducts/UCM110114.pdf
- 24 https://www.fda.gov/downloads/BiologicsBloodVaccines/Vaccines/ApprovedProducts/UCM574852.pdf (Si bien se usó un placebo en ensayos para adultos mayores de 65 años, no se usó placebo en ensayos para autorizar esta vacuna para niños.)
- 25 “Prevnar” También fue licenciado sin un ensayo controlado con placebo. http://labeling.pfizer.com/showlabeling.aspx?id=134 26 https://www.fda.gov/downloads/BiologicsBloodVaccines/Vaccines/ApprovedProducts/UCM133479.pdf

- 29 https://www.fda.gov/downloads/BiologicsBloodVaccines/Vaccines/ApprovedProducts/UCM224555.pdf
- 30 https://www.fda.gov/downloads/BiologicsBloodVaccines/Vaccines/ApprovedProducts/UCM110049.pdf (“Placebo (Aluminio Diluyente)” contained 300µg AAHS y timerosal, ver https://www.nejm.org/doi/full/10.1056/NEJM199208133270702)
- 31 https://www.fda.gov/downloads/BiologicsBloodVaccines/Vaccines/ApprovedProducts/UCM123789.pdf (El prospecto del paquete para M-M-R-II (triple viral SRP) cita una serie de ensayos previos a la licencia, por lo general con tamaños de muestra pequeños y que a menudo utilizan niños de orfanatos, instituciones psiquiátricas o escuelas para discapacitados. En total, cita: un ensayo para el MMR-II comparándolo con otras vacunas (ref. # 16), hay uno para la vacuna contra el sarampión en el que tanto el grupo de prueba como el grupo de control recibieron la vacuna contra el sarampión (ref. # 7), tres Ensayos para la vacuna contra las paperas en los que los controles fueron inyectados con varias vacunas experimentales (ref. # 8, 9, 11) y quince ensayos para la vacuna contra la rubéola que compararon diferentes tipos de vacuna contra la rubéola, excepto un ensayo con 23 controles aparentemente no tratados y un ensayo con 19 controles que reciben un aerosol nasal salino donde también se administró la vacuna contra la rubéola por vía intranasal (ref. # 1, 2, 19-26, 28, 29, 31, 56, 57).)
- 32 https://www.fda.gov/downloads/BiologicsBloodVaccines/Vaccines/ApprovedProducts/UCM142813.pdf (Si bien este prospecto indica que 465 niños recibieron un ‘placebo’, la publicación revisada por pares de Merck explica que ‘el placebo consistía en un estabilizador liofilizado que contenía aproximadamente 45 mg de neomicina’. Https://www.ncbi.nlm.nih.gov/pubmed/6325909. La neomicina es un antibiótico con efectos secundarios graves cuando se ingiere.: www.pdr.net/drug-summary/neomycin-sulfate?druglabelid=819&mode=preview)
- 33 https://www.fda.gov/downloads/BiologicsBloodVaccines/Vaccines/ApprovedProducts/UCM123793.pdf (En un ensayo clínico, 799 niños recibieron ProQuad + Placebo, MMR II + Placebo o MMR II + Varivax, pero ninguno recibió solo un placebo; Por lo tanto, este no fue un ensayo controlado con placebo ni pretende estar en su Revisión Clínica: http://wayback.archive-it.org/7993/20170723150913/https://www.fda.gov/downloads/ BiologicsBloodVaccines/Vaccines/ApprovedProducts/UCM123800.pdf)
- 34 Esta y la siguiente tabla incluyen todas las vacunas contra la gripe que los CDC enumeran para inyectarse en niños durante la temporada de gripe 2018-2019.. https://www.cdc.gov/flu/ protect/vaccine/vaccines.htm. Una vacuna contra la gripe, FluMist (LAIV4), se administra por pulverización nasal, no por inyección, y por lo tanto no se discute.
- 35 https://www.fda.gov/downloads/BiologicsBloodVaccines/Vaccines/ApprovedProducts/UCM619534.pdf (El control con placebo solo se usa en ensayos con adultos, pero desafortunadamente nunca en ensayos para autorizar esta vacuna para niños)
- 36 https://www.fda.gov/downloads/BiologicsBloodVaccines/Vaccines/ApprovedProducts/UCM619548.pdf 37 https://www.fda.gov/downloads/BiologicsBloodVaccines/Vaccines/ApprovedProducts/UCM356094.pdf
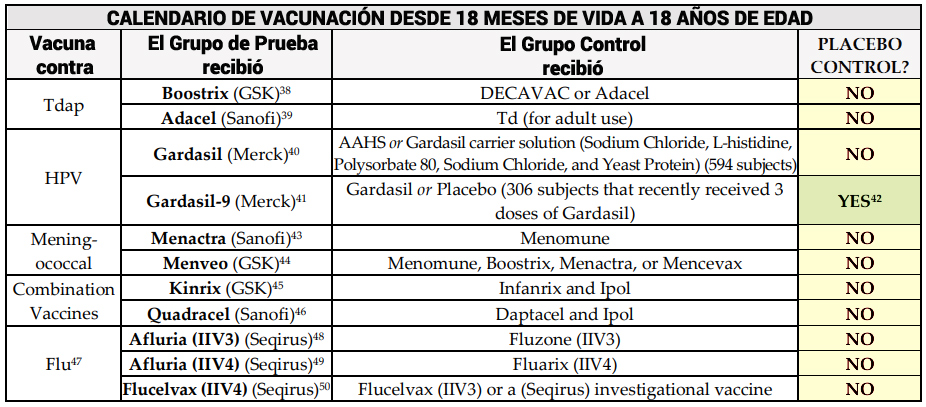
- 38 https://www.fda.gov/downloads/BiologicsBloodVaccines/UCM152842.pdf
- 39 https://www.fda.gov/downloads/BiologicsBloodVaccines/Vaccines/ApprovedProducts/UCM142764.pdf
- 40 https://www.fda.gov/downloads/BiologicsBloodVaccines/Vaccines/ApprovedProducts/UCM111263.pdf (Si bien este prospecto indica que 594 controles recibieron un ‘placebo salino’, la publicación revisada por pares de Merck explica que ‘el placebo utilizado en este estudio contenía componentes idénticos a los de la vacuna, con la excepción de las HPV L1 VLP y el adyuvante de aluminio’, lo que significa que ‘ Placebo ‘contenía cloruro de sodio, L-histidina, polisorbato 80, cloruro de sodio y proteína de levadura. https://www.ncbi.nlm.nih.gov/pubmed/17484215)
- 41 https://www.fda.gov/downloads/BiologicsBloodVaccines/Vaccines/ApprovedProducts/UCM429166.pdf
- 42 En solo un ensayo clínico, 306 controles recibieron un placebo, y Merck requirió que los 618 sujetos en este ensayo que recibieron Gardasil-9 hayan recibido recientemente 3 dosis de Gardasil y que estén en buen estado de salud. https://clinicaltrials.gov/ct2/show/NCT01047345. Por lo tanto, no se pueden sacar conclusiones de seguridad generalizadas de este pequeño ensayo, ya que solo incluyó sujetos con un historial comprobado de recibir Gardasil sin complicaciones de salud. Sin embargo, este ensayo demuestra que un placebo de solución salina puede usarse en ensayos clínicos de vacunas..
- 43 https://www.fda.gov/downloads/BiologicsBloodVaccines/Vaccines/ApprovedProducts/UCM131170.pdf (En un ensayo clínico, 509 adolescentes (entre 11 y 18 años) recibieron Td para uso en adultos más Menactra y 28 días después recibieron una inyección de solución salina, y 512 adolescentes recibieron Td para uso en adultos más una inyección de solución salina y 28 días después recibieron Menactra . A pesar de incluir una inyección de solución salina, este no es un ensayo controlado con placebo ni pretende estar en su Revisión Clínica: http://wayback.archive-it.org/7993/20170722073019/ https://www.fda.gov/BiologicsBloodVaccines/Vaccines/ApprovedProducts/ucm176044.htm)
- 44 https://www.fda.gov/downloads/BiologicsBloodVaccines/Vaccines/ApprovedProducts/UCM201349.pdf
- 45 https://www.fda.gov/downloads/BiologicsBloodVaccines/Vaccines/ApprovedProducts/UCM241453.pdf
- 46 https://www.fda.gov/downloads/BiologicsBloodVaccines/Vaccines/ApprovedProducts/UCM439903.pdf
- 47 Esta y la tabla anterior enumeran todas las vacunas inyectables contra la gripe para niños durante la temporada actual de gripe.: https://www.cdc.gov/flu/protect/vaccine/vaccines.htm
- 48 https://www.fda.gov/downloads/BiologicsBloodVaccines/Vaccines/ApprovedProducts/UCM263239.pdf (El control con placebo solo se usa en ensayos con adultos, pero desafortunadamente nunca en ensayos para autorizar esta vacuna para niños)
- 49 https://www.fda.gov/downloads/BiologicsBloodVaccines/Vaccines/ApprovedProducts/UCM518295.pdf
- 50 https://www.fda.gov/downloads/BiologicsBloodVaccines/Vaccines/ApprovedProducts/UCM619588.pdf (El control con placebo solo se usa en ensayos con adultos, pero desafortunadamente nunca en ensayos para autorizar esta vacuna para niños)
No es fácil lograr consentimiento informado, antes de aceptar la vacunación es necesario conocer y entender los eventos adversos graves que las diferentes vacunas. Antes de la inyección se debe saber si su hija/o tienen o no alguna vulnerabiliad genética que se debe saber antes de cualquier vacuna, ver en https://cienciaysaludnatural.com/prueba-de-mutacion-mthfr/
De acuerdo al Instituto de Medicina de la Academia de Ciencias de los EEUU., IOM: “Tanto las investigaciones epidemiológicas como las mecanicistas sugieren que la mayoría de los individuos que experimentan una reacción adversa a las vacunas tienen una susceptibilidad preexistente. Estas predisposiciones pueden existir por varias razones: variantes genéticas (en el ADN humano o microbioma), exposiciones ambientales, comportamientos, enfermedades intermedias o etapa de desarrollo, por nombrar solo algunas, todas las cuales pueden interactuar entre ellas. Algunas de estas reacciones adversas son específicas de la vacuna en particular, mientras que otras pueden no serlo”. https://www.nap.edu/read/13164/chapter/5#82
Los estudios de seguridad de la vacuna son casi siempre conducidos por los fabricantes de vacunas y ninguna de las vacunas en el calendario escolar han sido probadas con placebo inerte, fueron probadas contra una vacuna anterior o con un adyuvante como el aluminio, que es neurotóxico.
Ver más sobre inseguridad de la vacuanas y sobredosis de aluminio en el calendario de vacunacón en https://cienciaysaludnatural.com/aluminio




