Immunogenicity and Safety of a Measles-Mumps-Rubella Vaccine Administered as a First Dose to Children Aged 12 to 15 Months: A Phase III, Randomized, Noninferiority, Lot-to-Lot Consistency Study https://doi.org/10.1093/jpids/piz010 https://academic.oup.com/jpids/article/9/2/194/5372494

https://academic.oup.com/jpids/advance-article/doi/10.1093/jpids/piz010/5372494
PMID: 30849175 DOI: 10.1093/jpids/piz010
A medida que el caso de denuncia de irregularidades del Laboratorio Merck, fabricante de la vacuna Triple Viral SRP, contra Sarampión, Rubeola y Paperas (en inglés MMR) avanza hacia una resolución sobre la vacuna MMRII de Merck, los funcionarios del Departamento de Salud y Servicios Humanos de los Estados Unidos (DHHS) están luchando por obtener la versión de esta vacuna (SRP) de laboratorios Glaxo para llenar el posible vacío de stock si el fraude de Merck sale a la luz finalmente.
Antecedentes: Dos científicos de alto nivel de los laboratorios Merck, Stephen Krahling y Joan Wlochowski, presentaron su demanda federal de denuncias en 2010 alegando que Merck agregó de manera fraudulenta anticuerpos de conejo a muestras de sangre humana para que los funcionarios de la FDA creyeran que la vacuna era 95% efectiva y, por lo tanto, ganar el monopolio de la vacuna SRP (MMR). Cuando los científicos amenazaron con exponer el fraude, los funcionarios de Merck les ofrecieron sobornos, los amenazaron con prisión y luego destruyeron las pruebas de laboratorio.
La vacuna SRP (MMRII) defectuosa de Merck actualmente está causando epidemias de paperas enfermedad que es peligrosa en adultos completamente vacunados en todo el mundo. A instancias de la FDA (GSK) publicó recientemente los resultados de los ensayos clínicos en los EE. UU. Para la licencia apresurada de la vacuna su Glaix (MMR) Priorix® ( Klein et al.2019 ). Sabiendo que ninguna vacuna SRP (MMR) puede sobrevivir a las pruebas de seguridad contra un placebo inerte, la FDA permitió a GSK probar Priorix contra la MMR II de Merck. Los resultados fueron tan horribles para ambas formulaciones de vacunas que Glaxo y la FDA decidieron no publicarlos en el documento principal enterrándolos en su lugar en una tabla complementaria dentro de un apéndice.
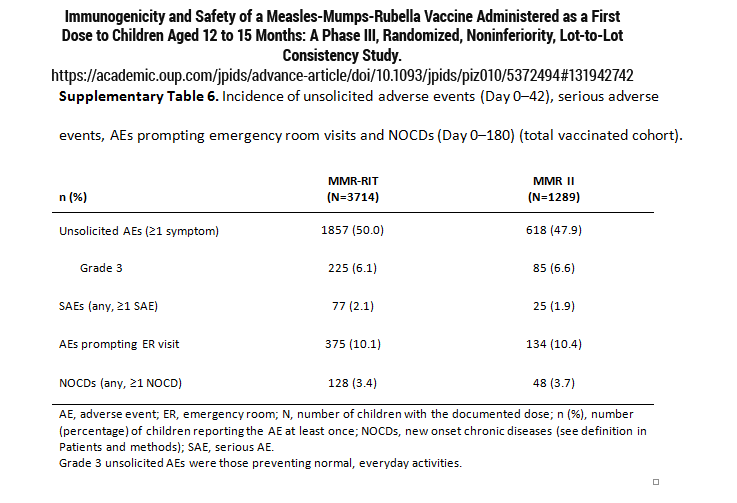
La Tabla 6 muestra los resultados impactantes; Casi el 50% de los receptores de vacunas experimentaron eventos adversos dentro de los 42 días posteriores a la vacunación y más del 10% de estos requirieron visitas a la sala de emergencias. Aproximadamente el 2% de estos eventos adversos fueron «graves» y el 3,5% de los receptores de la vacuna fueron diagnosticados con una «enfermedad crónica de nueva aparición» dentro de los 6 meses posteriores a la vacunación. Estos resultados de seguridad documentados son astronómicamente más altos que los puntos de discusión de la industria de las vacunas que afirman que los eventos adversos de la vacuna son «uno en un millón». Están mucho más en línea con los resultados del estudio Lazarus del DHHS donde 1 de cada 39 receptores de vacunas mostró una reacción adversa.

Referencias:
Immunogenicity and safety of a measles-mumps-rubella vaccine administered as a first dose to children 12–15 months of age: a phase III, randomized, non-inferiority, lot-to-lot consistency study
Authors: Nicola P Klein et al. – Running title: Immunogenicity and safety of MMR vaccineRunning title: Immunogenicity and safety of MMR vaccine Corresponding author: Nicola P Klein – Kaiser Permanente Vaccine Study Center e-mail: nicola.klein@kp.org
Immunogenicity and Safety of a Measles-Mumps-Rubella Vaccine Administered as a First Dose to Children Aged 12 to 15 Months: A Phase III, Randomized, Noninferiority, Lot-to-Lot Consistency Study https://academic.oup.com/jpids/advance-article/doi/10.1093/jpids/piz010/5372494 – Journal of the Pediatric Infectious Diseases Society, piz010, https://doi.org/10.1093/jpids/piz010
Extractado de https://childrenshealthdefense.org/news/merck-whistleblower-case-proceeds-toward-a-resolution/




