Los Centros para el Control de Enfermedades de EE.UU. , CDC ocultan los daños de las inyecciones K0 B1T (Covid). El CDC diseña el sistema de reportes adversos de inyecciones V-Safe para garantizar que los daños estén ocultos en campos de texto libre para poder controlar lo que se vuelve público, incluidos los daños enviados a VAERS que es la base de datos de efectos adversos en EE.UU.
Los Medicos: Dr. Aseem Malhotra, Dr. Peter McCullough, Dr. Eduardo Yahbes y Dr. Claudio Linares, denuncian los daños graves de la inyección Ko B1T y actos de negligencia graves departe de las autoridades responsables al vacunar a los que ya tenian inmunidadad natural por haber padecido la infección. https://www.bitchute.com/video/c5pVoatgVqJI/
V-Safe es una mejor base de datos que VAERS
¿Qué es v-safe?
V-safe es una herramienta basada en teléfonos inteligentes que utiliza mensajes de texto y encuestas web para proporcionar controles de salud personalizados después de recibir una inyección contra el COVID-19. A través de v-safe, supuestamente se puede informar rápidamente a los CDC si tiene algún efecto secundario después de recibir la inyección contra el COVID-19.
La aplicación para teléfonos inteligentes v-safe recopiló evaluaciones de salud posteriores a la vacunación de aproximadamente 10 millones de personas entre el 14 de diciembre de 2020 y el 31 de julio de 2022. Los datos de v-safe ya revelaron que 3,35 millones de personas informaron verse afectadas de alguna manera por las inyecciones, el 48,3 % recibió la inyección de Moderna.
A diferencia de VAERS, los datos en v-safe se recopilan de un universo de personas conocido y cuantificable. De hecho, v-safe tiene precisamente 10.108.273 usuarios registrados a partir de agosto de 2022. A estos usuarios se les pide que respondan las mismas preguntas. Al agregar respuestas a preguntas idénticas en v-safe, se puede calcular la tasa de una reacción adversa. Eso no es posible con VAERS.
Por ejemplo, de los 10.108.273 usuarios registrados de v-safe, 782.913 informaron que necesitaban atención médica después de la vacunación. Entonces, divide 782.913 entre 10.108.273 y, ahora sabes que el 7.7% de todos los usuarios registrados de v-safe buscaron atención médica al menos una vez después de la vacunación. Puede ver estos números usted mismo en el panel de ICAN v-safe:

(Tenga en cuenta que si las aproximadamente 528.381 personas que se registraron pero nunca completaron un solo control de salud se excluyeron de los 10.108.273 usuarios de v-safe, el denominador sería más pequeño y, por lo tanto, el porcentaje del 7,7 % sería mayor, a aproximadamente el 8,2 %).
VAERS, por otro lado, es un sistema de vigilancia pasiva y ese tipo de matemática no es posible porque no hay un número conocido de «usuarios» de VAERS para usar como denominador.
(Por lo que vale, VAERS tiene dos ventajas sobre v-safe. Primero, un usuario puede enviar una cantidad ilimitada de información a VAERS sobre un impacto adverso para la salud. Eso no es cierto para v-safe, que limita sus campos de texto libre, donde los usuarios pueden informar síntomas, hasta 250 caracteres. En segundo lugar, de conformidad con la ley federal, una gran parte de la información no identificada enviada a VAERS se hace pública de inmediato, aunque hay problemas con este sistema. Eso no es asi para v-safe.
V-Safe causado por informar a VAERS
Hay muchos indicios, incluido el sentido común, de que era menos probable que los usuarios de v-safe informaran a VAERS, ya que ya habían informado a v-safe. Una pregunta clave es si esto fue solo una consecuencia no deseada de v-safe.
Si v-safe no hubiera existido, existe una alta probabilidad de que más personas hubieran informado a VAERS y, de nuevo, en teoría, el público tendría acceso a esos datos. Es posible que nunca sepamos el contenido o la cantidad precisa de envíos de campos de texto libre en v-safe, que aún están ocultos a la vista del público (aunque seguimos luchando para obtener estos datos), mientras que tendríamos acceso a los informes de VAERS para informar al público. .
El CDC sabía que los usuarios de v-safe no informarían también a VAERS. Esto se refleja en la guía pública de los CDC con respecto a v-safe. Primero, los CDC trataron a VAERS como la alternativa si v-safe no estaba disponible. Por ejemplo, le dice a los miembros del público que «si no puede participar en v-safe, puede enviar informes de eventos adversos después de la vacunación al Sistema de Informe de Eventos Adversos de Vacunas (VAERS)». O bien, si un usuario pierde un registro de v-safe y aún desea informar , entonces debe usar VAERS.
En segundo lugar, los CDC afirmaron que harían un seguimiento con las personas que hicieran ciertos tipos de informes a v-safe y los ayudarían a enviar un informe VAERS «si corresponde». El protocolo v-safe de los CDC del 28 de enero de 2021 dispuso que cualquier impacto adverso para la salud informado debería resultar en una llamada telefónica. Presumiblemente, sin darse cuenta del volumen de informes que implicaría (¡millones!), Para la próxima versión del protocolo v-safe , emitida el 20 de mayo de 2021, los CDC limitaron las llamadas de seguimiento activas a «receptores que informan un problema de salud significativo atendido médicamente». impacto durante los controles de salud de v-safe”. Este es un grupo mucho más reducido que recibiría contacto de los CDC y, nuevamente, la agencia solo haría un informe VAERS «si corresponde». De esta manera, el CDC ahora se ha convertido en el intermediario entre las personas vacunadas y VAERS.
El mayor problema es que este plan de operar como intermediario para ayudar con los informes de VAERS aparentemente era teatro. El lenguaje «si corresponde» probablemente signifique que los CDC solo hicieron informes de VAERS cuando se trataba de lesiones que debían informarse a VAERS, y esa es una lista extremadamente limitada de eventos. Puedes ver la lista aquí .
Es decir, en lugar de que los informes se realicen directamente a VAERS, los CDC crearon una lista limitada de condiciones para las cuales incluso llamaría a los usuarios de v-safe y luego solo asistiría con un informe de VAERS si lo considerara apropiado. Esto, sin duda, resultó en una gran cantidad de informes de lesiones que de otro modo se habrían informado a VAERS y nunca llegaron a ese sistema.
Confirmación de que los CDC eligieron relegar las lesiones a las entradas de texto libre
Los CDC «manipularon» aún más v-safe al relegar los daños informados a campos de texto libre que los mantuvieron fuera de VAERS y ocultos al público.
Además los CDC no incluyeron opciones para marcar la casilla para los daños graves que etiquetaron como «Eventos adversos de especial interés» y enumeraron en un cuadro bajo el encabezado «Condiciones médicas preespecificadas». Los eventos adversos de especial interés enumerados en este gráfico incluyeron miocarditis, pericarditis, infarto agudo de miocardio, accidente cerebrovascular, SGB y mielitis transversa, entre otros eventos. Este cuadro estaba en la versión 2 del protocolo v-safe de los CDC del 28 de enero de 2021. Puede recordar que v-safe se lanzó en diciembre de 2020.
Ahora hemos obtenido una copia de la versión 1 del protocolo v-safe de los CDC con fecha del 19 de noviembre de 2020, antes de que se lanzara v-safe. Y la versión 1 muestra el gráfico preciso de la versión 2 del protocolo v-safe de los CDC. Aquí hay una copia de la versión 1 del protocolo y aquí está la lista relevante:
Estos eventos adversos fueron de hecho graves e incluyeron los siguientes:
- Infarto agudo de miocardio
- Anafilaxia
- Coagulopatía
- Enfermedad por COVID-19
- Muerte
- Síndrome de GuiIlain-Barre
- Enfermedad de Kawasaki
- Síndrome inflamatorio multisistémico en niños
- Síndrome inflamatorio multisistémico en adultos
- Miocarditis/Pericarditis
- Narcolepsia/Cataploría
- Embarazo y condiciones preespecificadas
- Convulsiones/Convulsiones
- Accidente cerebrovascular
- Mielitis transversa
A pesar de lo anterior, v-safe se lanzó y nunca se actualizó, para incluir campos de verificación para estas condiciones.
Si los CDC hubieran incluido las opciones de casilla de verificación para estos eventos adversos, podrían haber calculado claramente una tasa por cada daño para los 10 millones de usuarios de v-safe. Por ejemplo, si 400.000 reportaron miocarditis, entonces eso sería alrededor de un 4% de tasa reportada para esta condición. Sin embargo, los CDC optaron por no incluir estos daños como opciones para marcar la casilla. ¡En cambio, los relegó para que solo se capturaran potencialmente en campos de texto libre!
Luego, el CDC se involucró en llamar solo a ciertos usuarios de v-safe y luego solo hacer informes a VAERS cuando lo consideró apropiado. De esta manera, ocultó los eventos adversos de especial interés en los campos de texto libre y los mantuvo, sin duda, en su mayoría enterrados y fuera de la vista del público al no incluirlos a todos en VAERS.
Los CDC no contactan a tiempo a los usuarios de V-Safe que informan sobre lesiones
Si bien el CDC evitó poder calcular fácilmente una tasa de daño al no usar campos de verificación para eventos adversos de intereses especiales, la esperanza sería que al menos hiciera un seguimiento oportuno con los usuarios de v-safe que informaron daños graves en el campos de texto libre para obtener más información sobre sus lesiones. De esta manera, puede evaluar qué daños estaba causando la inyección y abordarlos rápidamente. Después de todo, los CDC afirmaron que v-safe es un sistema de vigilancia » en tiempo real » para las inyecciones contra el covid-19 «para que los científicos puedan estudiarlas rápidamente y determinar si existe un problema de seguridad con una inyección en particular».
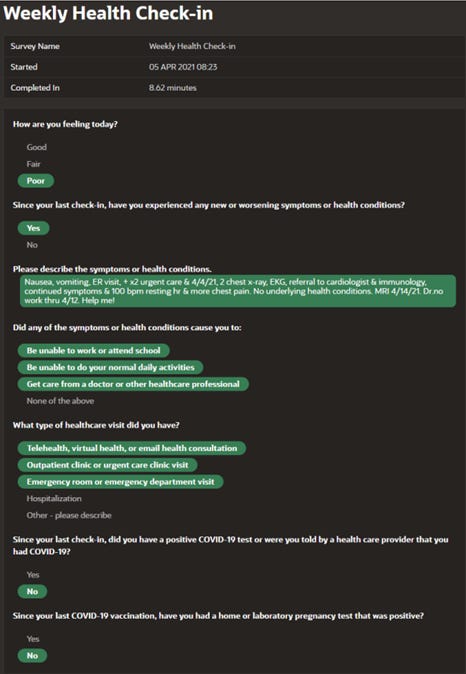
La siguiente es la historia de un Ph.D. quien se vacunó pronto para dar ejemplo y animar a sus alumnos a hacer lo mismo, refleja la negligencia del slo CDC: A pesar de informar claramente un impacto significativo en la salud médicamente atendido en numerosas ocasiones, que incluyó inflamación cerebral, reacción tóxica, ritmo cardíaco anormal, entumecimiento y hormigueo, fiebre alta, dolor en el pecho, dolor en las articulaciones, sensibilidad a la luz, mareos, problemas de equilibrio, náuseas, vómitos y letargo, y suplicando que alguien la ayudara con sus informes de v-safe, y tratando de llamar a v-safe ella misma, ¡los CDC no la llamaron hasta más de 200 días después de que informó su lesión grave!
Esto, por ejemplo, es lo que envió a v-safe solo un par de semanas después de su vacunación, que incluía la súplica «¡Ayúdame!»:
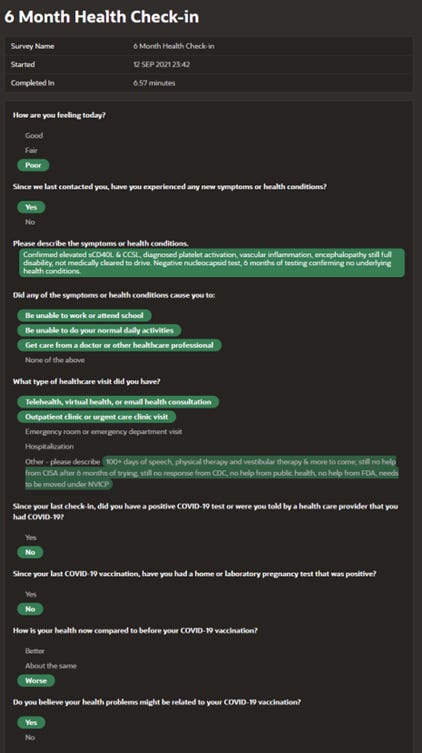
Sus súplicas de ayuda continuaron con cada control de salud durante los siguientes meses, que detallaron una condición médica grave y que empeoraba debido a la inyección y aún no había seguimiento por parte de los CDC. Vea su registro de 6 meses a continuación, donde señala que «todavía no hay respuesta de los CDC»:
Cuando los CDC finalmente la llamaron más de 200 días después de pedir ayuda, la primera pregunta de los CDC fue la fecha en que se recuperó. Explicó que no se recuperó, que todavía tenía una discapacidad total, que todavía no tenía permiso para conducir, que todavía no tenía permiso para caminar más de un número limitado de pasos por día, etc. Estaba claro que el representante de los CDC ni siquiera había leído su v-safe informes y no tenía ningún interés en evaluar realmente lo que le había sucedido a este Ph.D.
Uno se pregunta cuánto tiempo necesitaron esperar para recibir una llamada de los CDC las personas que informaron que «simplemente» estaban hospitalizadas o buscaban tratamiento en la sala de emergencias, sin ningún pedido de ayuda o descripciones de los síntomas y pruebas médicas. Y también está claro que cuando finalmente llegó una llamada, no se trataba de mejorar la seguridad de estos productos.
Esto en cuanto a la vigilancia » en tiempo real » de los CDC «para que los científicos puedan estudiarlos rápidamente y determinar si existe un problema de seguridad con una vacuna o inyección en particular».
La brecha que evita que el tren de carga de los problemas con los medicamentos obligatorios del gobierno se estrelle contra usted y su familia es la capacidad de decir «no» sin penalización o coacción. La importancia de ese derecho (a nunca ser obligado o coaccionado a recibir un producto médico) ya debería estar claro.
La inyección de Pfizer con licencia de la FDA no estuvo sometida el proceso normal de aprobación
Los reguladores de medicamentos de EE. UU. reconocieron haberse desviado del proceso normal de aprobación de vacunas al tratar con la inyección COVID-19 de Pfizer, según documentos recientemente revelados.
Semanas después de que Pfizer y su socio BioNTech anunciaran que comenzaron una presentación continua de documentos para la aprobación de su inyección COVID-19 , un funcionario de la Administración de Alimentos y Medicamentos (FDA) de EE.UU. redactó un memorandum autorizando la licencia de linyección (Biologics License Application, BLA) incluso cuando los reguladores estaban evaluando si aprobar el BLA, demuestran los documentos .
Christopher Joneckis, director asociado de gestión de revisión de la FDA, dijo que la decisión se debió en parte a que la FDA otorgó la Autorización de uso de emergencia (EUA) para la inyección a fines de 2020. Eso significa que la FDA «está familiarizada y ha revisado gran parte de la información proporcionada en la solicitud BLA», que consistía principalmente de datos utilizados en la solicitud de autorización de emergencia, dijo.
Las EUA se pueden otorgar si se ha declarado una emergencia de salud pública y la FDA determina que es «razonable creer» que la inyección u otro producto en cuestión «puede ser efectivo» para prevenir, diagnosticar o tratar la enfermedad o condición causada por el público. amenaza para la salud
Los BLA requieren un umbral más alto de evidencia que demuestre que un producto es «seguro, puro y potente».
Un documento separado que se hizo público esta semana mostró que el número de licencia se le dio a Pfizer a pesar de que no se había tomado una decisión de aprobación después de que Pfizer lo solicitara.
“El solicitante solicitó un número de licencia de EE. UU. para BioNTech Manufacturing GmbH con el acuerdo de que no lo usarán hasta después de que se apruebe el BLA” , afirma el documento , un resumen de una reunión de la FDA del 29 de junio de 2021 en la que se discutió la solicitud de Pfizer.
El resumen señaló que Joneckis escribió el memorando autorizando la publicación del número “antes de la notificación típica en la carta de aprobación”. Después de eso, la FDA “generó el número de licencia que se le proporcionará al Solicitante, después de la presentación, en un mensaje de correo electrónico”.
La FDA otorgó una BLA a la inyección de Pfizer para personas mayores de 16 años el 23 de agosto de 2021. Posteriormente, la inyección se aprobó para niños de hasta 6 meses de edad. La FDA también autorizó o aprobó múltiples refuerzos debido a que la inyección tuvo un desempeño deficiente frente a variantes más nuevas.
Los documentos fueron publicados por Informed Consent Action Network , que convenció con éxito a un tribunal para que ordenara a la FDA que presentara documentos relacionados con sus acciones sobre las inyecciones contra el COVID-19 después de que la agencia afirmara que tardaría décadas en hacerlo.
El gobierno ha estado proporcionando documentos de la Red de Acción de Consentimiento Informado en respuesta a la demanda y las solicitudes de la Ley de Libertad de Información.
Si encuentra este artículo útil, considere apoyarnos y en conjunto podamos aclarar el tema en conversaciones con familiares, amigos, funcionarios y empleadores. No ponemos avisos y necesitamos de su colaboración. Muchas gracias. Puede Apoyarnos en https://cienciaysaludnatural.com/colaboracion
Colabore por favor con nosotros para que podamos incluir mas información y llegar a más personas: contribución en mercado pago o paypal por única vez, Muchas Gracias!
Via PAYPAL: Euros o dólares click aqui
ARGENTINA 10.000$ar https://mpago.la/1srgnEY
5.000$ar https://mpago.la/1qzSyt9
1.000$ar https://mpago.la/1Q1NEKM
Solicite nuestro CBU contactenos