Concerns over informed consent for pregnant women in Pfizer’s RSV vaccine trial doi: https://doi.org/10.1136/bmj.p2620 – https://www.bmj.com/content/383/bmj.p2620 – Por Megan Redshaw Ctualización 19-Dic.-23

Pfizer no informó a las mujeres embarazadas que participaban en su ensayo clínico de la vacuna contra el virus respiratorio sincitial o sincicial (VRS) que el ensayo clínico de una vacuna similar de GlaxoSmithKline (GSK) se detuvo después de que una «señal de seguridad» (entiendase inseguridad) revelara un riesgo potencial de partos prematuros que provocaran muertes neonatales.
Aunque Pfizer conocía la posible señal de seguridad y estaba estudiando los nacimientos prematuros como un “evento adverso de especial interés”, continuó inscribiendo mujeres en su ensayo clínico y no informó completamente a los participantes sobre los riesgos que la vacuna podría representar para sus bebés. y en algunos casos, proporcionaron declaraciones engañosas y contradictorias, según una investigación de The BMJ .
Grave riesgo de partos prematuros y muertes neonatales en el prospecto de la vacuna “Abrysvo” de Pfizer contra el virus sincitial respiratorio. Carla Vizzotti, antes de irse, autorizó la vacuna Abrysvo de Pfizer contra el Virus Sincitial respiratorio, obligatoria para mujeres embarazadas y en el propio prospecto de la vacuna se advierte sobre potenciales partos prematuros. https://www.fda.gov/media/168889/download
“El artículo del BMJ demuestra el continuo desprecio de Pfizer por la ley y la elección del paciente”, dijo el abogado Thomas Renz. “El objetivo del consentimiento informado es garantizar que un paciente pueda tomar una decisión basándose en toda la información disponible. En lugar de abrazar el Código de Nuremberg y las leyes y regulaciones implementadas desde hace décadas, Pfizer parece ver el consentimiento informado como una barrera para las ventas, algo que causa dudas sobre las vacunas o los medicamentos”.
El Dr. Peter McCullough dice que las enfermedades raras que son leves no deberían ser el objetivo de una vacunación masiva. Debido a que tan pocas personas padecen el problema, y en el caso del virus respiratorio sincitial, la enfermedad es tan leve y fácilmente tratable con nebulizadores de albuterol y budesonida.
Este compendio de estudios de expertos, contiene la suficiente evidencia para que los padres puedan presentar a sus médicos y abogados y prevenir que su hijos sean intoxicados con vacunas o inyecciones génicas que no tienen los suficientes estudios de seguridad como corresponde. Tambien sirve para educar a los médicos sin pensamiento crítico. Click aqui para descargar este compendio
“Nunca debería haber habido un ensayo clínico en mujeres embarazadas que estudiara inyecciones dirigidas al virus sincitial respiratorio, VSR en mujeres embarazadas”, dijo Sasha Latypova. «El embarazo y la posibilidad de quedar embarazada son históricamente la clase de sujetos humanos más protegida de la investigación clínica porque los riesgos y la posibilidad de causar daños involuntarios son demasiado devastadores para justificar el interés científico en temas como el VSR».
El 29-12-2023 se publica que el Gobierno compró a Pfizer 530.000 dosis de vacunas por más de 28 millones de dólares. La vacuna fue comprada por contratación directa tras la autorización excepcional del Ministerio de Salud mediante la Resolución 4216/2023 . La Decisión Administrativa, que lleva la firma de Nicolás Posse (jefe de Gabinete) y Mario Russo (secretario de Salud), detalla que la tuvo un costo total de 28,8 millones de dólares.
Carla Vizzotti, informó a sus colegas provinciales que el ente encargado de controlar los medicamentos, alimentos y dispositivos médicos había dado luz verde a una vacuna dirigida a mujeres embarazadas contra el virus sincitial respiratorio. La vacuna será obligatoria para todas las madres que se encuentren en el período gestacional comprendido entre las semanas 32 a 36 !
Latypova es una ejecutiva jubilada de la industria farmacéutica con 25 años de experiencia en investigación y desarrollo farmacéutico y cofundadora de varias organizaciones que trabajan con compañías farmacéuticas para diseñar, ejecutar, recopilar datos y enviar datos de ensayos clínicos al Departamento de Alimentos y Medicamentos de EE. UU. Administración (FDA).
La seguridad de las vacunas contra la hepatitis B que se administran a los recién nacidos no se ha probado en un solo ensayo clínico controlado aleatorio con placebo inerte como se manifiesta en los propios prospectos y tiene sobredosis de aluminio neurotóxico. Este compendio de estudios de expertos, contiene la suficiente evidencia para que los padres puedan presentar a sus médicos y abogados y prevenir que su hijos sean intoxicados con vacunas que no tienen los suficientes estudios de seguridad como corresponde. Tambien sirve para educar a los médicos sin pensamiento crítico. Descargar libro click aqui
Dos personas de unos 60 años de aproximadamente 20.000 personas que recibieron la vacuna RSV de Pfizer fueron diagnosticadas con síndrome de Guillain-Barré, un trastorno poco común en el que el sistema inmunológico del cuerpo ataca sus nervios, reconoció la semana pasada la FDA.
Según Latypova, lo que antes se consideraba un resfriado inofensivo ahora se denomina virus sincitial respiratorio, VSR o RSV en inglés.
“La gran mayoría de los padres no han oído hablar del VSR si no han estado expuestos a la campaña de alarmismo de los CDC y al cambio de nombre de resfriados comunes que de otro modo serían inofensivos. La incidencia o prevalencia del VSR no se conoce precisamente porque no representa ningún peligro para nadie”, afirmó Latypova. «En los EE. UU., el VRS se atribuye como causa de muerte a aproximadamente 17 bebés por año cada 4.000.000 de bebés, según una revisión de los certificados de defunción de 12 años «. Según los Centros para el Control y la Prevención de Enfermedades (CDC), el VSR es un virus respiratorio común que generalmente causa síntomas leves parecidos a los de un resfriado. Aunque la mayoría de las personas se recuperan en una o dos semanas, puede ser grave y se diagnostica con mayor frecuencia en bebés.
Los efectos secundarios de la vacuna contra el Sarampión, Rubeola y Paperas, SRP (MMR en EE.UU.) incluyen convulsiones, que ocurren en aproximadamente 1 de cada 640 niños vacunados, aproximadamente 5 veces más frecuentemente que las convulsiones por infección de sarampión, sepa como eximir a sus hijos de esta vacuna. Este compendio de estudios de expertos, contiene la suficiente evidencia para que los padres puedan presentar a sus médicos y abogados y prevenir que su hijos sean intoxicados con vacunas que no tienen los suficientes estudios de seguridad como corresponde. Tambien sirve para educar a los médicos sin pensamiento crítico. Descargar libro click aqui
Tanto GSK como Pfizer estaban desarrollando una vacuna contra el VRS para mujeres embarazadas, pero GSK detuvo su ensayo de fase 3 de la vacuna en febrero de 2022 por un posible mayor riesgo de partos prematuros y muertes neonatales en los participantes vacunados.
Inmediatamente después de ser informada de la señal de seguridad, GSK informó a las autoridades sanitarias y actualizó sus formularios de consentimiento. No había explicación para el aumento de nacimientos prematuros, pero GSK dijo a The BMJ que todavía estaba investigando la señal de seguridad y que ya no estaba desarrollando su vacuna. Entonces surgió una disputa sobre si Pfizer tenía la obligación de informar a las mujeres que participaban en su ensayo clínico sobre el VRS sobre el riesgo potencial y si sus formularios de consentimiento debían actualizarse en consecuencia.
Pfizer no informó a las mujeres embarazadas sobre el riesgo de parto prematuro
El BMJ preguntó a Pfizer si las mujeres embarazadas que participaban en su ensayo clínico estaban informadas sobre el riesgo potencial de parto prematuro, pero el gigante farmacéutico no respondió. Como resultado, el BMJ se puso en contacto con las autoridades sanitarias gubernamentales en los 18 países donde Pfizer tenía sitios de ensayo y contactó a más de 80 investigadores del ensayo.
Según la investigación, el BMJ no recibió ninguna respuesta que indicara que Pfizer informó a las participantes embarazadas sobre el riesgo, y Pfizer continuó inscribiendo y vacunando a mujeres embarazadas durante meses después de que se publicitara el riesgo potencial de parto prematuro del ensayo clínico de GSK.
Charles Weijer, bioético y profesor de la Western University de Londres, Canadá, especializado en ética de la investigación, dijo a The BMJ que las mujeres embarazadas deberían haber sido informadas de la señal de seguridad revelada durante el ensayo clínico de GSK para que pudieran considerar si querían recibir la vacuna. o si ya habían recibido la vacuna, si debían buscar consejo médico o hacer seguimiento.
«Cualquier falla en proporcionar información de seguridad nueva y potencialmente importante a los participantes del ensayo es éticamente problemática», dijo el Sr. Weijer.
Rose Bernabe, profesora de ética e integridad de la investigación en la Universidad de Oslo, dijo a The BMJ: «La renovación del consentimiento informado es imprescindible», especialmente porque Pfizer afirmó seguir las directrices del Consejo de Organizaciones Internacionales de Ciencias Médicas y el Directriz internacional para la buena práctica clínica, las cuales contienen pasajes similares que establecen que el consentimiento informado debe renovarse “si se dispone de nueva información que pueda afectar la voluntad de los participantes de continuar”.
Este documento contiene la suficiente evidencia cientifica (más de 150 referencias) para que las madres puedan presentar a sus médicos y abogados y lograr exenciones para prevenir ser dañadas con vacunas o inyecciones génicas, que no tienen los suficientes estudios de seguridad como corresponde. Tambien sirve para educar a los médicos sin pensamiento crítico. descargar libro, click aqui
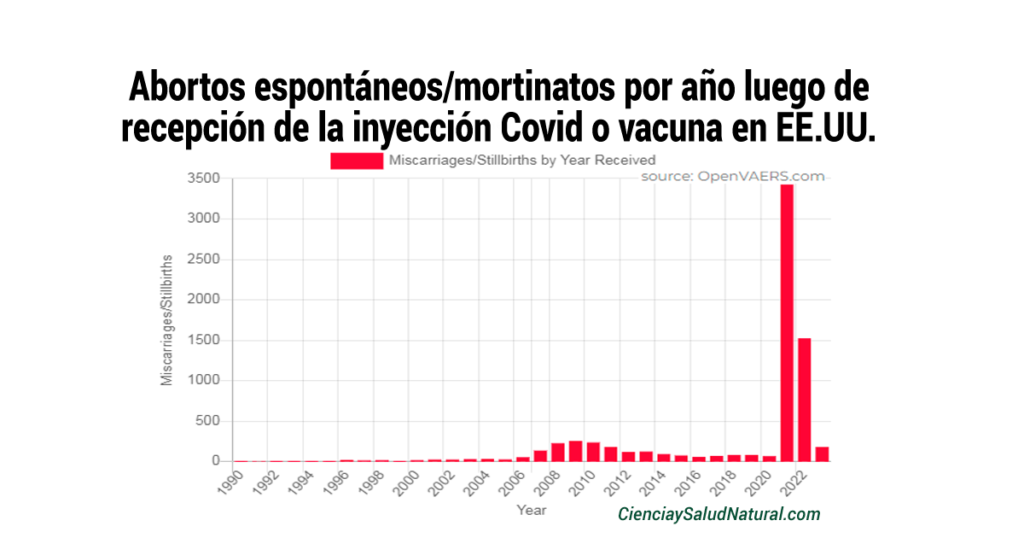
La Sra. Latypova dijo que estaba consternada de que “cualquier ensayo de cualquier producto fuera aprobado por la IRB [Junta de Revisión Institucional- Institutional Review Board] para proceder en esta población”.»Pfizer tenía la obligación ética de informar a los participantes en su ensayo clínico que GSK puso fin a su experimento», dijo Latypova. Al mismo tiempo, no está segura de por qué se esperaría un comportamiento ético de Pfizer, dada su respuesta a miles de muertes y lesiones reportadas, incluidos abortos espontáneos, en sus ensayos de la inyección COVID-19.
Los datos de la fase 3 de Pfizer sugieren un posible riesgo de parto prematuro
Según The BMJ, un año después de que se detuviera el ensayo clínico de GSK, los expertos pidieron una investigación del ensayo de fase 3 de Pfizer después de que de sus datos surgiera un desequilibrio numérico en los nacimientos prematuros. Incluso entonces, Pfizer no reveló en los formularios de consentimiento de los pacientes para su ensayo de fase 3 que estaba estudiando el parto prematuro como un “evento adverso de especial interés”, según documentos de Estados Unidos, Canadá, Países Bajos, Finlandia y Nueva Zelanda. obtenido por The BMJ.
Algunos formularios de consentimiento obtenidos por The BMJ contienen declaraciones inconsistentes que advierten sobre posibles efectos “peligrosos para la vida” de la vacuna en el bebé y al mismo tiempo afirman que solo la futura madre corre el riesgo de experimentar efectos adversos.
Los formularios de consentimiento establecen: «Los riesgos asociados con la vacuna del estudio (RSVpreF o placebo) pueden ser experimentados por usted, pero no por su bebé, ya que su bebé no recibirá la vacuna del estudio ni el placebo directamente».
El aluminio en las vacunas es neurotóxico y el calendario de vacunación infantil tiene sobredosis de aluminio. Los estudios de seguridad del aluminio tienen graves errores y este tema esta postergado desde hace décadas. Más de 100 referencias científicas de expertos para que Usted presente a su abogado o médico, para eximir a sus hijos de las vacunas. Descargar libro click aqui
«Sabiendo lo que sabemos ahora, la declaración en cuestión es irresponsable y, visto en retrospectiva, en realidad es objetivamente incorrecta», dijo la Sra. Bernabé a The BMJ. “La declaración da la falsa sensación de seguridad de que el feto o el neonato no estará expuesto a ningún riesgo o inconveniente. Considerando la gravedad del riesgo que encubre esta declaración irresponsable, esta declaración engañosa debería ser motivo para cuestionar la validez del proceso de consentimiento”.
El organismo nacional holandés de ética de la investigación también estuvo de acuerdo en que la declaración podría “potencialmente causar confusión” entre los participantes del ensayo clínico después de haber sido informado del problema por The BMJ. Posteriormente, la autoridad holandesa se puso en contacto con Pfizer sobre el lenguaje confuso y recomendó que se adaptara, pero desde entonces se supo que no se inscribirían nuevos participantes en el estudio, lo que hacía que el asunto fuera discutible.
“El hecho de que Pfizer estuviera investigando si el medicamento estaba provocando un parto prematuro pero luego decidiera no revelarlo parece indicar intencionalidad. Esta intencionalidad proporcionaría causas civiles de acción muy graves e incluso podría significar que esta acción podría alcanzar el nivel de actividad criminal”, dijo Renz.
“En este punto, el público realmente necesita empezar a preguntarse cuántas leyes puede violar Pfizer antes de que sus lobistas ya no puedan darse el lujo de pagar a nuestros políticos para que hagan la vista gorda”, añadió Renz.
No todos estuvieron de acuerdo en que Pfizer tuviera la obligación de informar a las mujeres embarazadas en su ensayo clínico sobre los riesgos potenciales.
Beate Kampmann, directora del Centro para la Salud Global del Hospital Universitario Charité de Berlín y autora principal de la publicación del ensayo de fase 3 de Pfizer, que supervisó un sitio de ensayos clínicos en Gambia, dijo a The BMJ que los resultados de GSK no eran relevantes para los participantes de su ensayo. ya que la mayoría de los participantes ya estaban en seguimiento”.
Kampmann dijo que la vacuna de GSK no era la misma que la de Pfizer, y que la Junta de Monitoreo de Seguridad y Datos del ensayo, que revisa y evalúa los datos del estudio para proteger la seguridad de los participantes y monitorear el progreso del estudio, «no planteó ninguna preocupación».
Dijo que los resultados de GSK eran específicos de cada lugar e implicaban un hallazgo temporal que aún no se comprende bien. Kampmann dijo a The BMJ que las preguntas sobre el consentimiento informado y los posibles efectos secundarios en el ensayo equivalían a «obsesionarse con cuestiones que no están confirmadas por el análisis y que están distorsionando los beneficios que esta vacuna puede aportar».
Plantas que comúnmente se utilizan para tratar la neumonía, la bronquitis, el asma, los resfriados y la tos. Plantas medicinales como Quimpe, Gordolobo, Acacia torta, Tulsi (Ocimum sanctum), Menta haplocalyx, Lechuga Silvestre (Lactucavirosa), Shankhpushpi (Convolvulus pluricaulis), Ricinela (Acalypha indica), más… Descargar libro click aqui
La FDA aprueba la vacuna RSV de Pfizer, a pesar del riesgo de seguridad
El Comité Asesor de Vacunas y Productos Biológicos Relacionados de la FDA (VRBPAC) discutió en mayo los datos de los ensayos clínicos de Pfizer y un análisis publicado por la FDA.
El comité VRBPAC de la FDA autorizó la inyección a pesar de que cuatro de los 14 miembros del comité, incluido el Dr. Paul Offit, dijeron que los datos de Pfizer eran inadecuados para respaldar su seguridad. El doctor Offit, pediatra y reconocido experto en virología e inmunología, se mostró preocupado por los resultados de GSK porque su vacuna era “casi idéntica” a la de Pfizer.
El Dr. Offit dijo que GSK presentó sus datos durante una reunión de dos días sobre el VRS en Lisboa, y lo que encontraron fue que, al igual que Pfizer, había una asociación temporal en los países de ingresos bajos y medios, lo que significa que «había una especie de período de varios meses en el que hubo ese aumento en la asociación estadística con los nacimientos prematuros, pero no en otros momentos”.
También cuestionó por qué había “claramente un mayor riesgo” de parto prematuro en los participantes vacunados y una disminución en el grupo de placebo.
El Dr. Offit señaló además que aunque fue la “muerte” durante el ensayo clínico de GSK lo que inicialmente “llamó la atención de todos”, fueron los nacimientos prematuros graves los que provocaron esas muertes.
La Dra. Hana El Sahly, presidenta de VRBPAC, dijo que la señal que muestra un mayor riesgo de partos prematuros asociado con la vacuna RSV de Pfizer fue «significativa» en las fases dos y tres de su ensayo clínico y «en un producto muy similar que se administró». , en otro estudio.»
«Dicho esto, ¿es motivo suficiente para hacer una pausa? Probablemente sí», dijo el Dr. Sahly. «Quiero decir, aumentar el riesgo de que las mujeres embarazadas tengan un 20% más de riesgo de parto prematuro no es trivial, incluso si se trata de un parto prematuro tardío. El hecho de que las estemos sometiendo a un parto prematuro mientras estamos sentados aquí debatiendo el asunto intelectualmente no es trivial.»
Cuando la FDA autorizó la vacuna, determinó que los datos disponibles eran “insuficientes para establecer o excluir una relación causal entre el parto prematuro y la vacuna ABRYSVO RSV de Pfizer, pero limitó su uso a mujeres que tienen entre 32 y 36 semanas de embarazo para mitigar el riesgo potencial.
La FDA también exige a Pfizer que realice estudios posteriores a la comercialización para «evaluar la señal de riesgo grave de parto prematuro».
En 2022, la FDA también exigió a Pfizer que realizara varios estudios de seguridad posteriores a la comercialización para evaluar los posibles impactos a largo plazo de la miocarditis, un tipo de inflamación cardíaca asociada con la inyección COVID-19 de Pfizer, como parte de su proceso de aprobación. Se requirió que los datos se entregaran a la FDA en diciembre de 2022, pero la FDA silenciosamente concedió a Pfizer una extensión cuando no cumplió con su fecha límite.
Ya hay una larga tradición de autorizar vacunas con efectos adversos graves no resueltos, en este caso ACIP autoriza la Vacuna contra hepatitis B con efectos adversos graves sin resolver… https://www.bitchute.com/video/IYPOfVI5S2mo/
Los datos informados por Pfizer a los CDC indicaron que el 14% de las mujeres embarazadas que participaron en el ensayo de Pfizer sufrieron un evento adverso, y el 4,2% sufrió un evento adverso «grave», el 1,7% sufrió un evento adverso. % que experimentó un evento adverso «grave» y 0,5 % que sufrió un evento adverso «que pone en peligro la vida».
De manera similar, los mismos datos mostraron que el 37,1% de los bebés cuyas madres recibieron la vacuna experimental de Pfizer experimentaron eventos adversos dentro del mes posterior al nacimiento: el 15,5% se clasificó como “graves”, el 4,5% como “graves” y el 1% como “con peligro para la vida”. ”, mientras que la eficacia disminuyó a los pocos meses de la vacunación.
Según el Centro Nacional de Información sobre Vacunas (NVIC), “Los datos del ensayo clínico sobre el VSR también incluyeron la muerte de una mujer embarazada, 18 muertes fetales (diez en mujeres embarazadas vacunadas y ocho en mujeres embarazadas no vacunadas) y 17 muertes infantiles (cinco en el grupo de embarazo vacunado y 12 en el grupo de embarazo no vacunado)”.
La Dra. Meryl Nass dijo a que había esencialmente tres problemas con los datos del ensayo clínico de Abrysvo, «dos de los cuales fueron identificados por Pfizer y la FDA». Ella dijo:
“Había aproximadamente un 20% más de bebés prematuros y de bajo peso al nacer en el grupo cuyas madres habían sido vacunadas en comparación con el grupo cuyas madres habían recibido un placebo. Esto fue muy preocupante, pero la mayor parte del comité lo ignoró.
“No me quedó claro si Pfizer había recopilado suficiente información sobre la salud de las mujeres embarazadas después de la vacunación. Es difícil saber cuando se estudiaba, recién nacidos y bebés, si han tenido algún efecto secundario por la vacunación de sus madres. Los niños no fueron estudiados durante el tiempo suficiente para comparar su capacidad intelectual u otros parámetros”.
“Nadie cuestionó la veracidad de los datos presentados por Pfizer, a pesar de que Pfizer presentó repetidamente a este comité datos sobre la eficacia de su vacuna COVID que hicieron que las vacunas parecieran mucho más eficaces de lo que resultaron ser”, dijo Nass.
El Dr. Peter McCullough, también cuestionó los datos del ensayo clínico de Abrysvo. “Pfizer ha avanzado agresivamente ECA [ensayos controlados aleatorios] en la población embarazada sin garantías sobre los resultados a largo plazo. No hay ningún beneficio directo para las madres”.
Deberíamos exigir seguridad a largo plazo, alta eficacia… y al menos un año de durabilidad, para una condición tan rara y fácil de tratar en los bebés”, añadió.
Se ignoran los llamados a un “escrutinio más estricto” de la vacuna contra el VSR
Algunos expertos en salud pidieron un “escrutinio más estricto” de Abrysvo antes de la reunión VRBPAC del jueves, informó Axios, “después de que los ensayos de GlaxoSmithKline detuvieran el ensayo para una vacuna similar sobre mayores riesgos de nacimientos prematuros y muertes neonatales”.
En Argentina incorporan al Calendario Nacional de Vacunación, con carácter obligatorio, la vacuna contra el Virus Sinticial Rrespiratorio para su aplicación a personas gestantes.
La ministra de Salud de la Nación, Carla Vizzotti anunció los ministros y ministras de Salud de las provincias que la Administración Nacional de Medicamentos, Alimentos y Tecnología Médica (ANMAT) registró el 8 de setiembre 2023 la vacuna para personas gestantes contra el virus sincicial respiratorio.
El 9 de diciembre 2023 resuelve:
ARTÍCULO 1° —. Incorpórase al Calendario Nacional de Vacunación, con carácter gratuito y obligatorio, la vacuna contra el VIRUS SINCICIAL RESPIRATORIO para su aplicación a personas gestantes.
ARTÍCULO 2° —. La presente medida entrará en vigencia a partir del día 1° de enero de 2024.
ARTÍCULO 3° —. Comuníquese, publíquese, dese a la DIRECCIÓN NACIONAL DEL REGISTRO OFICIAL y archívese.
Esta Administración Nacional informa que, mediante la disposición 7397/23, autorizó la inscripción en el Registro de Especialidades Medicinales (REM) del producto “ABRYSVO”, vacuna bivalente contra el virus sincicial respiratorio recombinante de la firma PFIZER S.R.L.
10 días antes de que asuma el nuevo presidente de la Nación, Javier Milei, el Estado nacional se preparó para realizar un desembolso cercano a los u$s 55 millones. Dicha suma será para saldar dos procesos licitatorios relativos a diferentes procesos relativos a vacunas.
Uno de los procesos tiene como protagonista a la norteamericana Pfizer, empresa que resultó adjudicataria en una de las licitaciones públicas. La misma busca proveer al Estado de su vacuna contra el meningococo Nimenrix. Todo será por un total de u$s 47.9 millones. Son en total 3 millones de unidades, las que resultaron vencedoras ante el francés Sanofi, laboratorio que se había presentado con su marca Menactra.
La licitación adjudicada bajo las firmas de la Ministra de Salud de la Nación, Carla Vizzotti y del jefe de Gabinete, Agustín Rossi, implica a vacunas tetravalentes conjugadas contra los serogrupos A, C, Y y W-135. La compra había sido solicitada por la Dirección de Control de Enfermedades Inmunoprevenibles encabezada por Florencia Bruggesser. Ver Boletín Oficial.
Colabore por favor con nosotros para que podamos incluir mas información y llegar a más personas: contribución en mercado pago o paypal por única vez, Muchas Gracias!
Via PAYPAL: Euros o dólares click aqui
ARGENTINA 10.000$ar https://mpago.la/1srgnEY
5.000$ar https://mpago.la/1qzSyt9
1.000$ar https://mpago.la/1Q1NEKM
Solicite nuestro CBU contactenos











