Este es parte del estudiode la Dra. Loretta Bolgan de la Asociación Corvelva. Recomendamos el trabajo completo o suscribase a nuestro sitio y le enviaremos la traduccion en español. Traducido y revisado por el Dr. Oscar Botta. Descargar estudio original click aqui
En el pasado, varios equipos de investigación desarrollaron vacunas experimentales contra el virus del SARS, que pertenece a la misma familia que el virus COVID-19 y también infecta los pulmones. En algunos casos, los animales que recibieron algunos tipos de vacunas experimentales de SARS parecen desarrollar una inflamación pulmonar más severa cuando se infectaron posteriormente con SARS que los animales no vacunados.
La Vacuna de ARN mensajero entre otros problemas críticos que no se han resuelto por completo incluyen la inmunidad preexistente en humanos contra el vector que se utiliza en la vacuna. Esto puede producir respuestas inflamatorias como reacciones adversas, incautación de vectores en el hígado y el bazo y la inmunodominancia de los genes del vector en los transgenes (es decir, el sistema inmunitario forma anticuerpos contra el vector adenoviral en lugar del antígeno), y para los vectores competentes la reversión a adenovirus infeccioso y la capacidad potencial de integrarse en el ADN.
Posibles plataformas de vacunación contra el SARS-CoV-2 [91]
Los laboratorios adoptan diferentes técnicas para diseñar vacunas contra un microorganismo patógeno. Estas opciones están condicionadas por la naturaleza del patógeno y la infección, así como por consideraciones prácticas sobre el uso de la vacuna. Algunas de las opciones incluyen
- vacunas inactivadas,
- vacunas de ADN
- vacunas de RNAm (mensajero)
- vacunas vectores virales recombinates
- vacunas de subunidades recombinantes.
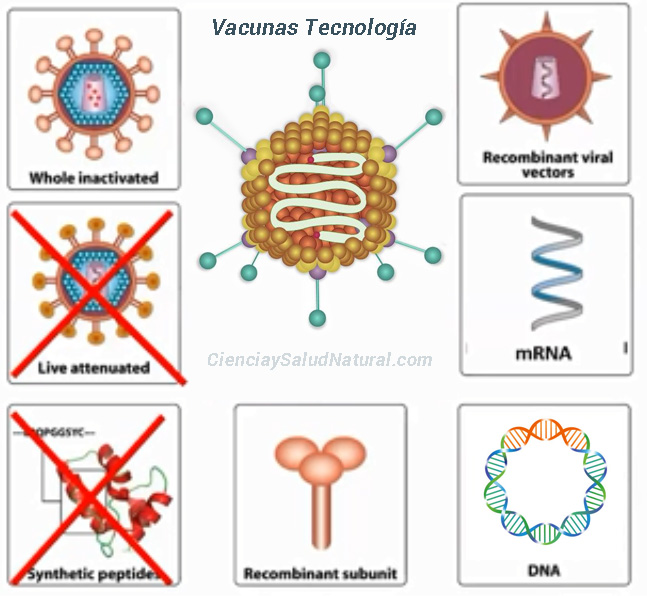
Las nuevas vacunas contra el coronavirus pueden ser Vacunas de ácido nucleico que a su vez puden ser
• vacunas de ADN
• vacunas de ARN
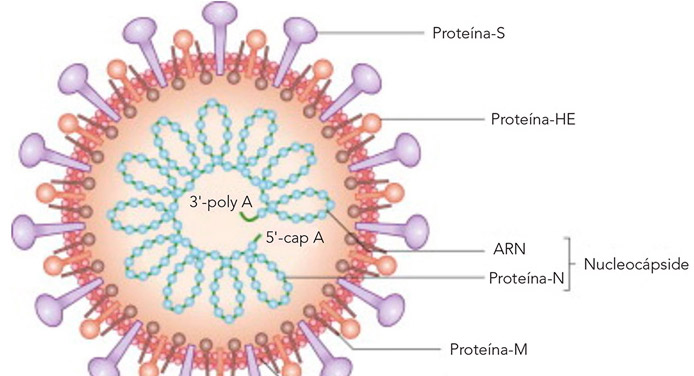
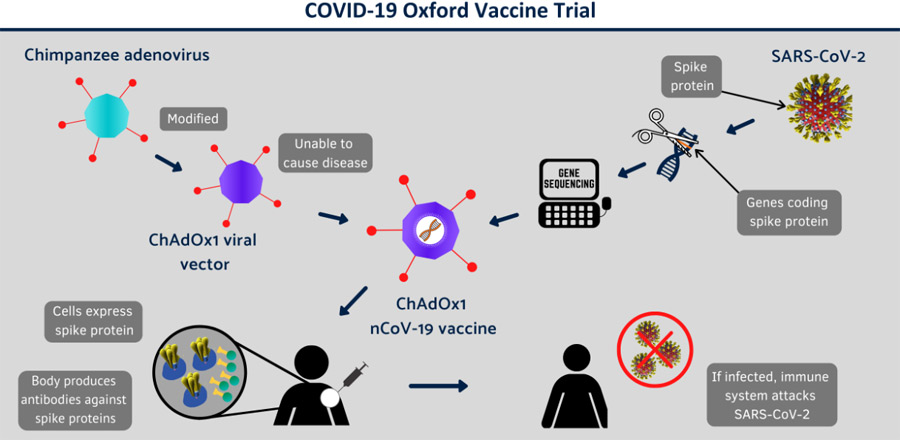
La estructura de una partícula de coronavirus se representa en al figura arriba con las diversas proteínas virales indicadas. La proteína S es el objetivo principal para el desarrollo de vacunas. De estas plataformas, ahora profundizaremos en lo relacionado con la vacuna que, con alta probabilidad, estará disponible en el mercado italiano en otoño, es decir, la vacuna vector atenuada viva ChadOx1 nCov-19. [92]
Como veremos, estas son vacunas de última generación obtenidas por tecnología de ADN recombinante, con el uso de un vector de adenovirus modificado genéticamente que permite que el antígeno de la proteína S del SARS-Cov-2 sea transportado dentro del células del sistema inmunitario.
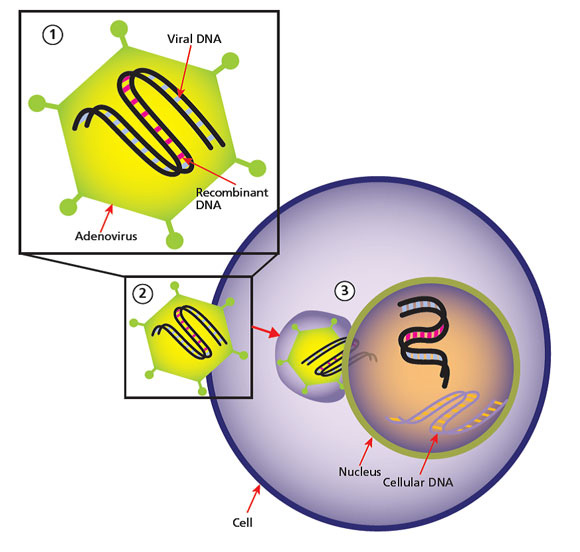
Estos tipos de vacunas no han sido autorizadas para su uso hoy en día como vacunas para la prevención de enfermedades infecciosas, mientras están en uso, principalmente todavía a nivel experimental, como vacunas terapéuticas contra el cáncer y para terapia génica (con vectores capaces de integrarse en el ADN). Para su uso como vacunas para la profilaxis, el vector es defectuoso, es decir, no debe poder integrarse en el ADN o infectar células. Por lo tanto, la creación del vector es un paso particularmente crítico para el que el fabricante debe garantizar la seguridad. Por lo tanto, sería importante poder obtener más información a este respecto de las agencias reguladoras, ya que la capacidad de integrarse en el ADN y transformar las células es un riesgo que no puede excluirse por completo.
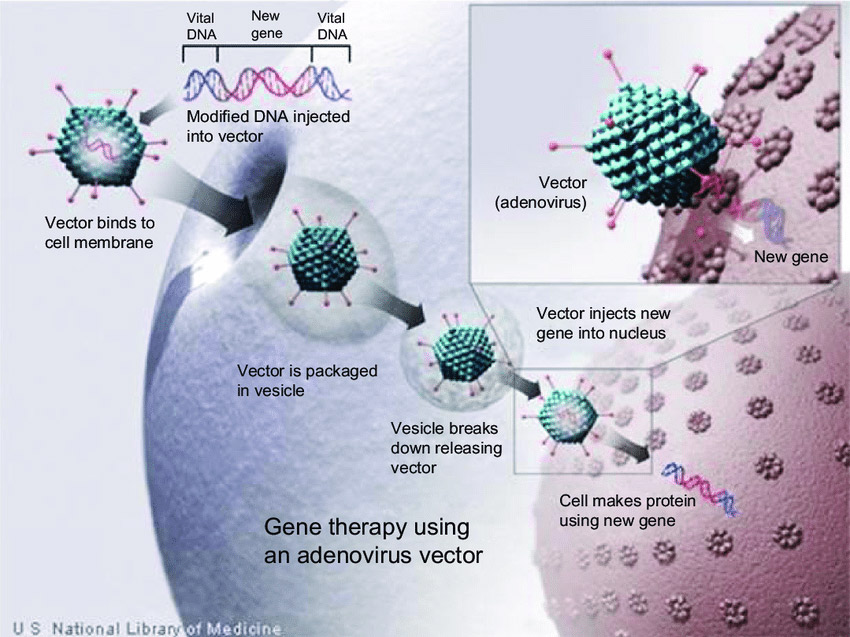
El fragmento del virus SARS-Cov-2 que pertenece a la proteína Spike, que es la proteína que se une al receptor de células ACE2 y que es atacado por anticuerpos en caso de infección, se agrega al vector. Por lo tanto, el objetivo es garantizar que la célula inmune en la que se introduce el vector diseñado produzca grandes cantidades de proteína espiga que luego se expone en la membrana celular para su reconocimiento por el sistema inmune y la producción de anticuerpos específicos.
Suscríbase a nuestro boletín. click aqui
La secuencia de proteína espiga que se inserta proviene de una única secuencia viral y, por lo tanto, debido al fenómeno de las poblaciones mutantes discutidas anteriormente, conducirá a la formación de anticuerpos específicos para el antígeno de la vacuna y poco específicos para toda la población viral en continuo la evolución. La pobre especificidad de los anticuerpos de la vacuna como se detalla anteriormente predispone a los vacunados a las dos inmunopatologías particularmente peligrosas:
- el pecado antigénico original y
- la mejora dependiente de anticuerpos.
La presencia de secuencias superponibles en las de las proteínas humanas, como lo demuestra el análisis bioinformático en dos artículos recientes publicación, puede ser responsable de una respuesta inmune autoinmune / inflamatoria contra las estructuras del cuerpo.
En cuanto a la calidad, actualmente no se conoce la formulación exacta de la vacuna y para la producción se ha hecho público que el vector diseñado se propaga en líneas celulares humanas inmortalizadas, por lo tanto cancerígenas, procedentes de tejidos fetales / embrionarios.
De ello se deduce que es posible el riesgo de que existan residuos de material genético de la línea celular (ADN cancerígeno y virus adventicios cancerígenos), así como la posible presencia de material genético derivado del proceso de ingeniería, que podría integrarse en el ADN.
https://www.corvelva.it/speciale-corvelva/corvelva-ebook/covid-19-il-vaccino-che-verra.html
—————
Estas críticas muy importantes que afectan a los tres aspectos de la vacuna (calidad, eficacia y seguridad) requieren una optimización cuidadosa del proceso de purificación del producto y la experimentación preclínica antes de pasar a las diversas fases clínicas.
La necesidad de aplicar el principio de precaución aumenta aún más por el hecho de que hasta la fecha no ha sido posible que las empresas obtengan el registro de vacunas efectivas y seguras contra el SARS-Cov-1 y el MERS, por lo que es necesario exigir un mayor escrupulosidad en el estudio de las diversas fases del proceso de autorización [94] Considerando la extensa literatura que respalda todo lo informado hasta ahora, la elección de acelerar la fase de investigación clínica y producción a gran escala sigue siendo altamente cuestionable, debido a la falta de justificación científica que lo fundamente y, sobre todo, arriesgado para futuras personas vacunadas.
Método de preparación del antígeno viral de la vacuna ChadOx1 nCov-19 [96]
Construcción del mensajero
Los adenovirus (AdV) son virus de ADN icosaédrico sin pericapsida (o envoltura) de tamaños entre 70 y 90 nm que pertenecen a la familia de los adenovirus. Designado por el tejido adenoideo (amígdalas) del que se identificaron por primera vez, ahora se sabe que los AdV infectan una amplia gama de tejidos, causando infecciones principalmente benignas como congestión nasal y secreción nasal, tos y conjuntivitis.
Los vectores de la vacuna AdV vienen en una variedad de formas diferentes basadas en la estrategia terapéutica planificada.
Los vectores defectuosos se diseñan con la eliminación del locus E1 responsable de la replicación y generalmente carecen de los genes de la proteasa E3 para crear espacio adicional para la inserción de transgenes. Los vectores competentes retienen genes para la replicación en las células, pero tienen una capacidad más limitada para los insertos transgénicos.
La elección entre un vector competente o defectuoso para la replicación depende de las características del virus utilizado, su inmunogenicidad, seguridad y el inserto de ADN necesario. Un aspecto crítico muy importante en la preparación de las vacunas de vectores adenovirales es que el inserto tiende a eliminarse después de la replicación del propio vector o durante la producción o después de la administración de la vacuna (reversión) con pérdida total de efectividad. [96] Otros problemas críticos que no se han resuelto por completo incluyen la inmunidad preexistente en humanos contra el vector, respuestas inflamatorias como reacciones adversas, incautación de vectores en el hígado y el bazo y la inmunodominancia de los genes del vector en los transgenes (es decir, el sistema el sistema inmunitario forma anticuerpos contra el vector adenoviral en lugar del antígeno), y para los vectores competentes la reversión a adenovirus infeccioso y la capacidad potencial de integrarse en el ADN.
Vacunas contra infecciones virales y bacterianas: vectores no replicantes, no diseminantes
Los especialistas insertan el código genético del antígeno (en nuestro caso, la secuencia de la proteína Spike) en el vector, cuya proteasa viral y la región E1 han sido eliminados. Luego, producen placas de virus recombinantes, amplifican el vector usando una línea celular apropiada y lo purifican. Cuando se inyecta, el vector ingresa al tejido celular objetivo y produce altos niveles de antígeno. Debido a la ausencia de E1 y proteasas, el vector no puede replicarse o extenderse a otras células. La producción transitoria de alto nivel del antígeno por las células infectadas genera una respuesta inmunitaria protectora (humoral y celular) contra el agente infeccioso del que deriva el antígeno. (Figura siguiente)
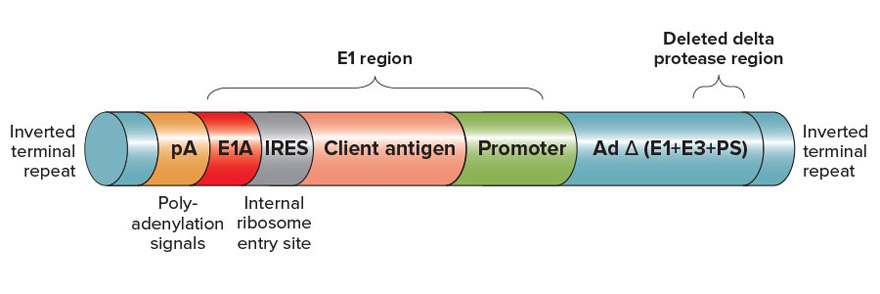
Vacunas y terapia contra el cáncer altamente potentes: vector replicante, no diseminante. Para agentes infecciosos, los especialistas insertan la secuencia genética del antígeno en el vector. La región E1 está presente, lo que permite que el vector se replique y aumente significativamente el número de copias del antígeno. Las placas del vector recombinante se producen y amplifican usando una línea celular adecuada.

En las vacunas contra agentes infecciosos, el vector se replica en las células del tejido inyectado y produce grandes cantidades de antígeno, pero no se propaga. La creación del vector viral se puede hacer de diferentes maneras: Típicamente, la producción del vector adenoviral recombinante se basa en el uso de líneas celulares tales como HEK293 (de riñón embrionario humano) y PER.C6 (de células retinianas embrionarias humanas) que complementan las funciones del vector adenoviral que se han eliminado o rediseñado.
La línea celular principal utilizada para los vectores de adenovirus sin E1 es la línea celular 293 derivada de células de riñón embrionario humano que contiene la región E1 del adenovirus.

Otra línea celular popular es la línea celular de la retina embrionaria humana, PER.C6® (promotor PGK, que contiene E1 y retina, clon número 6). La línea celular PER.C6® se deriva de una sola célula retinerizada humana, que se inmortalizó deliberadamente utilizando tecnología de ADN recombinante. Como resultado, las células PER.C6® pueden replicarse indefinidamente, permitiendo crecer en suspensión de células individuales en condiciones sin suero en cantidades apropiadas para tamaños grandes. Uno de los principales grupos que trabajan en esta área es el Oxford Jenner Institute, que está desarrollando vacunas para el SARS, MERS, Zika, VIH, Tuberculosis y Ébola. Su programa dedicado de ingeniería de vectores está enfocando sus esfuerzos en los vectores adenovirales del chimpancé, que no se ven obstaculizados por la inmunidad contra el vector existente en las poblaciones humanas. Como ya se vio, uno de los programas actuales para SARS-Cov-2 está dirigido por el equipo de la profesora Sarah Gilbert, quien desarrolló un vector adenovírico de chimpancé (ChAdOx1) contra el coronavirus MERS. [98]
Respuesta celular a la vacuna [99]
En cuanto al mecanismo de inducción de respuestas celulares y de anticuerpos específicas de transgén por vacunas de vectores virales con replicación defectuosa, la administración por inyección intramuscular provoca la infección de las células musculares (no productivas en el caso de vectores virales defectuosos de replicación) seguido de expresión transgénica en 24 horas y desde la activación de respuestas inmunes innatas a través de interacciones con receptores virales para el reconocimiento de ácidos nucleicos y patógenos.
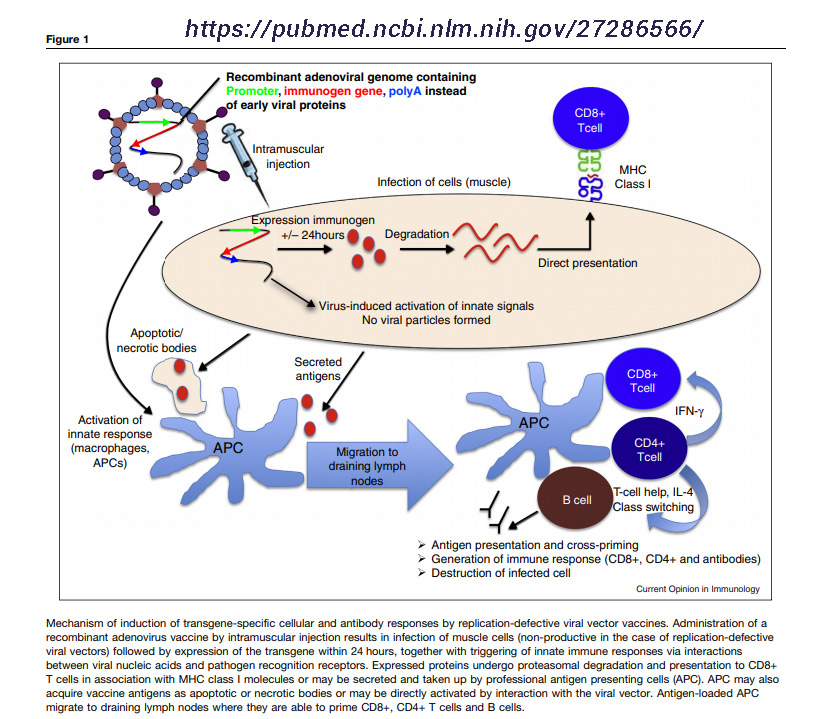
Las proteínas expresadas sufren degradación proteasómica y presentación a las células T CD8 + en asociación con las moléculas de MHC de clase I o pueden ser secretadas y absorbidas por las células que presentan el antígeno profesional (APC). El APC también puede adquirir antígenos vacunales, como cuerpos apoptóticos o necróticos, o puede activarse directamente al interactuar con el vector viral. Las APC cargadas con el antígeno migran a los ganglios linfáticos de drenaje donde pueden desencadenar células T CD8 +, CD4 + y células B.
SARS-Cov-2 y Covid-19 la vacuna
Problemas críticos para la calidad del producto terminado
Por lo tanto, la creación de la vacuna implica dos fases distintas:
- la producción del vector adenoviral y
- la producción del fragmento viral de la proteína Spike del SARS-Cov-2 utilizando tecnología de ADN recombinante;
Posteriormente, el vector diseñado se cultiva en líneas celulares inmortalizadas para producir grandes cantidades de antígeno de vacuna. Tanto la composición de la vacuna SARS-Cov-2 en uso para el estudio clínico 1, y el proceso de producción específico con más detalle, se desconocen actualmente. Sin embargo, al ser producido a partir de líneas celulares y tejidos para la extracción y cultivo de virus y utilizando tecnología de ADN recombinante, ya se puede considerar que los pasos para la purificación de ADN residual, virus adventicios de líneas celulares y los fragmentos de material genético de la ingeniería del vector son ciertamente particularmente críticos.
Desde el punto de vista clínico, el uso de estos vectores presenta una importancia crítica: la primera generación de vectores para vacunas basadas en adenovirus humano arquetípico AdHu5 ha mostrado poca eficacia. Posteriormente se descubrió que un gran porcentaje de adultos humanos albergan títulos significativos de anticuerpos neutralizantes contra serotipos humanos comunes como AdHu2 y AdHu5, después de una infección natural. Los anticuerpos neutralizantes podrían reducir la potencia de las vacunas virales de vectores al bloquear la entrada viral en las células huésped y, por lo tanto, la liberación del transgén en el objetivo. La aparición de inmunidad anti-vector preexistente se aborda mediante el desarrollo de nuevos vectores adenovirales basados en serotipos a los que es menos probable que la población humana haya estado expuesta, incluidos los de origen chimpancé. Sin embargo, algunos de estos vectores adenovirales de chimpancés también tienen una eficacia limitada a partir de varios niveles de reactividad cruzada con adenovirus humanos, inexplicables en poblaciones humanas y crecimiento subóptimo en líneas celulares transformadas, por lo que las industrias tienen una gama de vectores diferentes medicamentos adenovirales disponibles para su uso en inmunización contra diversas enfermedades, ya que la inducción de anticuerpos neutralizantes contra un vector puede evitar su readministración para otra indicación.

Consecuencias de la inmunidad del vector adenoviral (Ad). La inmunidad HAd preexistente inhibe la transducción inicial con vectores HAd y, por lo tanto, evita el primer uso de muchos vectores HAd. En sujetos sin inmunidad HAd preexistente, el primer uso del vector HAd induce fuertes respuestas inmunes innatas, celulares y humorales. La inmunidad celular elimina la mayoría de las células transducidas, mientras que la inmunidad humoral bloquea la infección posterior con el mismo vector HAd.
¿Podría la vacuna ChadOx1 nCov-19 empeorar la enfermedad de COVID-19?
En el pasado, varios equipos de investigación desarrollaron vacunas experimentales contra el virus del SARS, que pertenece a la misma familia que el virus COVID-19 y también infecta los pulmones. En algunos casos, los animales que recibieron algunos tipos de vacunas experimentales de SARS parecen desarrollar una inflamación pulmonar más severa cuando se infectaron posteriormente con SARS que los animales no vacunados.
Actualmente se están realizando estudios sobre la vacuna ChAdOx1 nCoV-19, en animales, pero aún no sabemos si esto también podría ser un efecto secundario de la exposición al virus pandémico COVID-19 en este estudio de la vacuna COVID-19, si este efecto pudiera ocurrir en humanos o si en algunos casos esto podría conducir a una enfermedad COVID-19 más grave.
A partir de la revisión de la hoja de estudio clínico propuesta, se pueden observar los siguientes problemas críticos que no permiten evaluar correctamente la seguridad de la futura vacuna:
a) las vacunas en las que se usó el mismo vector adenoviral utilizado para preparar la vacuna SARS-Cov-2 se probaron en la fase I (320 personas) [101] y, por lo tanto, los datos son extremadamente limitados. La afirmación anterior de que este tipo de vacuna es segura y bien tolerada es engañosa porque un estudio tan limitado no puede dar ninguna garantía de seguridad.
b) un grupo de vacunas vacunadas con la vacuna antimeningocócica, definida como segura porque ya ha sido autorizada y administrada durante algún tiempo, se utiliza como control.
Sin Grupo Control o Placebo real
Por lo tanto, faltan el grupo de control negativo con placebo (agua fisiológica) y el grupo de nunca vacunados, lo que permitiría cuantificar la incidencia real de reacciones adversas agudas y especialmente a largo plazo. De esta manera, un sesgo de datos ya está presente con una subestimación significativa de las reacciones adversas.
Deben tenerse en cuenta las reacciones adversas informadas en la hoja de datos de la vacuna antimeningocócica: La siguiente información se toma del resumen de las características del producto de Nimenrix declarado por el fabricante: [102]
• Síncope: el síncope (desmayo) puede ocurrir después o incluso antes de cualquier vacunación, especialmente en adolescentes como respuesta psicógena a la inyección con aguja. Puede ir acompañado de varios signos neurológicos, como trastornos visuales transitorios, parestesia y movimientos tónico-clónicos de las extremidades durante la fase de recuperación.
• Trombocitopenia y trastornos de la coagulación: Nimenrix debe administrarse con precaución en sujetos con trombocitopenia o cualquier 70 – SARS-Cov-2 y Covid-19 la vacuna trastorno de la coagulación ya que puede ocurrir sangrado después de la administración intramuscular en estos sujetos.
• Inmunodeficiencia: es posible que no se induzca una respuesta inmune adecuada en pacientes que reciben tratamiento inmunosupresor o en pacientes con inmunodeficiencia. Los sujetos con deficiencia hereditaria del complemento (por ejemplo, deficiencia de C5 o C3) y las personas que reciben tratamientos que inhiben la activación terminal del complemento (por ejemplo, eculizumab) tienen un mayor riesgo de enfermedad invasiva causada por el serogrupo A, C de Neisseria meningitidis , W-135 e Y, aunque desarrollan anticuerpos después de la vacunación con Nimenrix.
Farmacovigilancia activa: 7 días; sigue la farmacovigilancia pasiva durante 3 semanas y luego a discreción de la persona visitada después de un año. En este modo, solo se detectan reacciones agudas no graves comunes. La anafilaxia aguda y el síndrome de Guillain Barrè (que tiene un tiempo de inicio de hasta 6 semanas y es un posible evento adverso de la vacuna antimeningocócica que actúa como control [103] también se consideran reacciones adversas graves graves, incluso si ya afirma que estas son reacciones respectivamente raras y extremadamente raras, mientras que puede surgir la posibilidad de reacciones a más largo plazo.
Agravamiento de la enfermedad en caso de infección (ADE): información sobre la posibilidad teórica de esta enfermedad muy grave: a partir de la comparación entre animales vacunados y no vacunados, el grupo de pacientes vacunados ha experimentado complicaciones graves después de la infección secundaria a la vacunación. Esta evidencia, aunque teórica en humanos porque la vacuna nunca se ha probado antes, pero es extremadamente grave para la seguridad de los vacunados, debería haber requerido por esta razón estudios preclínicos con grupos no vacunados en animales y el grupo de control con placebo y nunca vacunado en el estudio clínico.
Por lo tanto, se puede concluir que este tipo de experimentación, que será la única que se llevará a cabo antes de la comercialización de la vacuna, es absolutamente incapaz para proporcionar datos sobre la seguridad de la vacuna, porque para evaluar el riesgo de ADE es necesario esperar a que los voluntarios vacunados contraigan la enfermedad en ambos grupos, lo que no puede suceder durante el estudio clínico, sino solo después de la comercialización. El síndrome autoinmune / inflamatorio, que es la reacción adversa potencialmente más grave para esta vacuna, seguramente tendrá un tiempo de latencia de más de 7 días durante el cual tiene lugar la farmacovigilancia activa porque, como hemos visto, requiere la intervención de la respuesta inmune posterior, y por lo tanto puede no estar causalmente asociado con la vacuna
Conclusión
De lo anterior y a la luz del reciente gran desastre de la vacuna Sanofi para el dengue, una vacuna que incluso había sido probada en 35.000 sujetos, se sigue el siguiente hecho: hoy, para el SARS-CoV-2 era obligatorio proceder con atención multiplicada a estudios preclínicos, estudios de fase II y III antes de proceder con protocolos de validación apresurados, especialmente considerando que en los protocolos actuales solo se permiten personas con salud óptima, mientras que cuando se administrará a toda la población, el riesgo de reacciones adversas graves ciertamente es mayor y más significativo para las categorías ya afectadas por patologías más invalidantes para las cuales se recomendará la vacuna o, peor aún, se fuera obligatoria.
Comentarios:
Las vacunas recombinantes pueden producir una potenciación de la enfermedad. Una de las explicaciones está en la respuesta inmunitaria que genera la vacuna contra el antígeno recombinante de la proteína S, (que es parte de las proyecciones de la corona, o Spikes), que usa el virus para adherirse al receptor celular para poder entrar.
Probablemente los anticuerpos que genera este tipo de vacuna no son anticuerpos neutralizantes, es decir, no son inhibidores del virus.
Más bien parece ser que la respuesta inmunitaria produciría anticuerpos de tipo opsonizantes, es decir anticuerpos que inmovilizan al virus y lejos de impedir que infecten, los acercarían al receptor celular y les facilitarían la infección de las células.
El anticuerpo producido contra la proteína S recombinante no neutraliza al virus, sino lo inmoviliza y lo acerca al receptor celular, teniendo un efecto facilitador de la infección, provocando una enfermedad mucho más grave
Esta es una de las explicaciones más probables de porqué las vacunas recombinantes probadas en animales provocan una enfermedad mucho más grave cuando el vacunado entrega en contacto con el virus. Roxana Bruno PhD. en Inmunología
Ver estudio original Este estudio fue proporcionado gratuitamente por la Asociación Corvelva en formato digital (eBook), Dra. Loretta Bolgan ni de la Asociación Corvelva.
Referencias
89 – https://www.who.int/vaccine_safety/publications/gvs_aefi/en/ Causality assessment of an adverse event following immunization (AEFI) User manual for the revised WHO AEFI causality assessment classification (Second edition)
90 – Version 2. F1000Res. 2018 Feb 28 [revised 2018 May 29];7:243. doi: 10.12688/f1000research.13694.2. Revised World Health Organization (WHO)’s causality assessment of adverse events following immunization-a critique. Puliyel J1, Naik P2.
91 – Methods Mol Biol. 2019;2013:165-176. doi: 10.1007/978-1-4939-9550-9_12. Vaccine Development: From Preclinical Studies to Phase 1/2 Clinical Trials. Artaud C1, Kara L2,3,4, Launay O5,6,7. https://pubmed.ncbi.nlm.nih.gov/31267501/?from_single_result=Methods+Mol+Biol.+2019%3B2013%3A165-176&expanded_search_query=Methods+Mol+Biol.+2019%3B2013%3A165-176#
92 – Immunity. 2020 Apr 14;52(4):583-589. doi: 10.1016/j.immuni.2020.03.007 SARS-CoV-2 Vaccines: Status Report. Amanat F1, Krammer F2.
93 – Guideline on quality, non-clinical and clinical aspects of live recombinant viral vectored vaccines https://www.ema.europa.eu/en/documents/scientific-guideline/guideline-quality-non-clinical-clinical-aspects-live-recombinant-viral-vectored-vaccines_en.pdf
Mol Ther. 2014 Mar;22(3):668-674. doi: 10.1038/mt.2013.284. Clinical assessment of a novel recombinant simian adenovirus ChAdOx1 as a vectored vaccine expressing conserved Influenza A antigens. Antrobus RD1, Coughlan L1, Berthoud TK1, Dicks MD1, Hill AV1, Lambe T2, Gilbert SC3.
PLoS One. 2012;7(7):e40385. doi: 10.1371/journal.pone.0040385. A novel chimpanzee adenovirus vector with low human seroprevalence: improved systems for vector derivation and comparative immunogenicity. Dicks MD1, Spencer AJ, Edwards NJ, Wadell G, Bojang K, Gilbert SC, Hill AV, Cottingham MG.
Pathogens. 2019 Nov 12;8(4). pii: E231. doi: 10.3390/pathogens8040231. A Single and Un-Adjuvanted Dose of a Chimpanzee Adenovirus-Vectored Vaccine against Chikungunya Virus Fully Protects Mice from Lethal Disease. Campos RK1, Preciado-Llanes L2, Azar SR1, Lopez-Camacho C2, Reyes-Sandoval A2, Rossi SL3.
Front Microbiol. 2019 Aug 2;10:1781. doi: 10.3389/fmicb.2019.01781. Recent Advances in the Vaccine Development Against Middle East Respiratory Syndrome-Coronavirus. Yong CY1,2, Ong HK3, Yeap SK4, Ho KL3, Tan WS1,2.
94 – Clin Immunol. 2020 Apr 18;215:108426. doi: 10.1016/j.clim.2020.108426. On the molecular determinants of the SARS-CoV-2 attack. Kanduc D1, Shoenfeld Y2. https://www.ncbi.nlm.nih.gov/pmc/articles/PMC7165084/pdf/main.pdf J Transl Autoimmun. 2020 Apr 9:100051. doi: 10.1016/j.jtauto.2020.100051. Pathogenic Priming Likely Contributes to Serious and Critical Illness and Mortality in COVID-19 via Autoimmunity.
Lyons-Weiler J1. https://www.ncbi.nlm.nih.gov/pmc/articles/PMC7142689/ 95 – Nature. 2020 Mar;579(7800):481. doi: 10.1038/d41586-020-00798-8. Coronavirus vaccines: five key questions as trials begin. Callaway E. https://www.nature.com/articles/d41586-020-00798-8
Nature. 2020 Mar;579(7799):321. doi: 10.1038/d41586-020-00751-9. Don’t rush to deploy COVID-19 vaccines and drugs without sufficient safety guarantees. Jiang S. https://www.nature.com/articles/d41586-020-00751-9
Nat Rev Immunol. 2020 Apr 21. doi: 10.1038/s41577-020-0321-6. The potential danger of suboptimal antibody responses in COVID-19. Iwasaki A1,2, Yang Y3. https://www.nature.com/articles/s41577-020-0321-6.pdf
96 – Mol Ther Methods Clin Dev. 2016 Apr 27;3:16030. doi: 10.1038/mtm.2016.30. Methods and clinical development of adenovirus-vectored vaccines against mucosal pathogens. Afkhami S1, Yao Y1, Xing Z1.
Hum Gene Ther. 2014 Apr;25(4):318-27. doi: 10.1089/hum.2014.007. Challenges in manufacturing adenoviral vectors for global vaccine product deployment. Vellinga J1, Smith JP, Lipiec A, Majhen D, Lemckert A, van Ooij M, Ives P, Yallop C, Custers J, Havenga M. https://www.bataviabiosciences.com/wp-content/uploads/2016/12/vellinga-2014.pdf
Biotechnol J. 2015 May;10(5):741-7. doi: 10.1002/biot.201400390. Large-scale adenovirus and poxvirus-vectored vaccine manufacturing to enable clinical trials. Kallel H1, Kamen AA.
Vaccine. 2006 Feb 13;24(7):849-62. Development of nonhuman adenoviruses as vaccine vectors. Bangari DS1, Mittal SK.
Hum Gene Ther. 2014 Apr;25(4):301-17. doi: 10.1089/hum.2013.235. Adenovirus-based vaccines for fighting infectious diseases and cancer: progress in the field. Majhen D1, Calderon H, Chandra N, Fajardo CA, Rajan A, Alemany R, Custers J.
Curr Opin Virol. 2016 Dec;21:1-8. doi: 10.1016/j.coviro.2016.06.001. Viral vectors as vaccine carriers. Ertl HC1
Curr Opin Immunol. 2016 Aug;41:47-54. doi: 10.1016/j.coi.2016.05.014. Viral vectors as vaccine platforms: from immunogenicity to impact. Ewer KJ1, Lambe T1, Rollier CS2, Spencer AJ1, Hill AV3, Dorrell L4.
Chapter 4 Adenoviral Vector-Based Vaccines and Gene Therapies : Current Status and Future Prospects Shakti Singh, Rakesh Kumar, Babita Agrawal Published 2019
https://www.semanticscholar.org/paper/Chapter-4-Adenoviral-Vector-Based-Vaccines-and-Gene-Singh-Kumar/f452e476b448ac6add9429a886cf2e9aab93f4db
Adenoviruses and Adenovirus Vectors: A Primer on their Biology http://www.hvtn.org/content/dam/hvtn/HVTNews/HVTNews%20March%202008.pdf
PLoS Comput Biol. 2019 Jul 19;15(7):e1006857. doi: 10.1371/journal.pcbi.1006857 Recombinant vector vaccine evolution. Bull JJ1, Nuismer SL2, Antia R3.
97 – PLoS Comput Biol. 2019 Jul 19;15(7):e1006857. doi: 10.1371/journal.pcbi.1006857 Recombinant vector vaccine evolution. Bull JJ1, Nuismer SL2, Antia R3.
98 – Simian adenovirus and hybrid adenoviral vectors https://patents.google.com/patent/US20150044766 https://clinicaltrials.gov/ct2/show/NCT03399578
99 – Curr Opin Immunol. 2016 Aug;41:47-54. doi: 10.1016/j.coi.2016.05.014. Epub 2016 Jun 7. Viral vectors as vaccine platforms: from immunogenicity to impact. Ewer KJ1, Lambe T1, Rollier CS2, Spencer AJ1, Hill AV3, Dorrell L4.
Swiss Med Wkly. 2017 Aug 8;147:w14465. doi: 10.4414/smw.2017.14465. eCollection 2017. Virally vectored vaccine delivery: medical needs, mechanisms, advantages and challenges. Pinschewer DD1.
100 – http://www.isrctn.com/ISRCTN15281137 https://www.covid19vaccinetrial.co.uk/files/cov001pisv3202apr2020pdf
101 – https://www.precisionvaccinations.com/vaccines/chadox1-mers-mers-cov-vaccine Numero partecipanti = 24 https://www.biorxiv.org/content/10.1101/2020.04.13.036293v1 studio preclinico su animali https://www.vaccitech.co.uk/pipeline/ vaccini che utizzano lo stesso vettore (Vaccitech)
102 – RIFLESSIONI SUL VIRUS SARS-CoV-2 E LA CORSA AL VACCINO https://www.nexusedizioni.it/it/CT/riflessioni-sul-virus-sars-cov-2-e-la-corsa-al-vaccino-6015 riassunto delle caratteristiche del prodotto: NIMENRIX https://ec.europa.eu/health/documents/community-register/2012/20120420120470/anx_120470_it.pdf
103 – Therapie. 2019 Sep;74(Nimenrix, Meningococcal group A, C, W135 and Y conjugate vaccine4):495-498. doi: 10.1016/j.therap.2018.12.008. [Guillain-Barré syndrome to meningococcal conjugate vaccine: Menveo®].[Article in French] Moukafih B1, Lachhab Z2, Moutaouakkil Y3, Fettah H2, Ahizoune A4, Tadlaoui Y2, Bennana A2, Lamsaouri J2, Bousliman Y3. 104 – https://en.wikipedia.org/wiki/Schering-Plough




