- 1. Los datos de seguridad para la licencia de hepatitis B son deficientes
- 2. Estudios de vacunados versus no vacunados
- 3. No hay razon científica para la aplicacion de esta vacuna
- 4. Riesgos de la hepatitis B en comparación con los de la vacuna contra hepatitis B
El calendario de vacunación infantil de los CDC en EE. UU. y varios países incluye la vacuna contra la hepatitis B desde la década de 1990. Recomienda que los médicos administren la primera dosis (de una serie de una a dos inyecciones) la primera dosis, el primer día de vida. 1 Dos de las vacunas contra la hepatitis B inyectadas en bebés sólo evaluaron las reacciones adversas durante cuatro y cinco días, respectivamente.
| Enfermedad objetivo | Nombre del producto (fabricante) | Duración de la revisión de seguridad después de la inyección | |
| Reacciones solicitadas | Reacciones no solicitadas | ||
| Hepatitis B | Recombivax HB (Merck) | 5 dias | 5 dias |
| Engerix-B (GSK) | 4 dias | 4 dias | |
Los datos de seguridad para la licencia de hepatitis B son deficientes
El Departamento de Salud y Servicios Humanos ( HHS ) de EE.UU. afirma que: “Los datos en los que se basa la autorización para el uso infantil de la vacuna contra la hepatitis B se resumen en el prospecto respectivo”. La seguridad de las vacunas contra la hepatitis B que se administran habitualmente a los recién nacidos no se ha probado en un solo ensayo clínico controlado aleatorio en el que un el grupo de control recibió un placebo inerte como se manifiesta en los propios prospectos.
Sin ensayos clínicos (con métodos rigurosos, muestras de gran tamaño, verdaderos controles de placebo y períodos prolongados de observación de los daños causados por la vacuna) que den resultados que demuestren que los beneficios de la vacunación superan claramente los daños, el programa de vacunación a gran escala no puede estar éticamente justificado y va en contra del principio de precaución.
El prospecto de Recombivax HB en la sección 6 de Efectos Adversos señala que se consideró seguro para los niños según un ensayo clínico en el que se monitorizó sólo 147 bebés y niños (de hasta 10 años de edad) durante cinco días después de la vacunación.
Este ensayo es inútil porque:
- el tamaño de la muestra es demasiado pequeño,
- el período de revisión de seguridad es demasiado corto y
- no se realizó un control con placebo.
La información de seguridad en el prospecto de Engerix-B es igualmente inadecuada ya que el ensayo clínico de esta vacuna tampoco tuvo control con placebo y solo monitoreó la seguridad durante cuatro días después de la vacunación.
Estos prospectos claramente no respaldan la seguridad de administrar estos productos a bebés. Por lo tanto, la afirmación del HHS de que “los datos en los que se basa la autorización para el uso infantil de la vacuna contra la hepatitis B se resumen en el prospecto respectivo” es alarmante.
Por otro lado es contraproducente vacunar a un bebe recien nacido dado que la vacuna contra hepatitis B tiene sobredosis de aluminio, varias veces mas lo niveles permisibles y los niños con problemas congenitos como por ejemplo mutación MTHFR pueden quedar gravemente dañados como los aclara Instituto de Medicina de la Academia de Ciencias de los EEUU., IOM. De acuerdo al IOM:
“Tanto las investigaciones epidemiológicas como las mecanicistas sugieren que la mayoría de los individuos que experimentan una reacción adversa a las vacunas tienen una susceptibilidad preexistente. Estas predisposiciones pueden existir por varias razones: variantes genéticas (en el ADN humano o microbioma), exposiciones ambientales, comportamientos, enfermedades intermedias o etapa de desarrollo, por nombrar solo algunas, todas las cuales pueden interactuar entre ellas. Algunas de estas reacciones adversas son específicas de la vacuna en particular, mientras que otras pueden no serlo”.
Este tipo de mutación MTHFR lo padece mas del 30 % de la poblacion. Es decir, estamos exponiendo al 30% de los bebes a riesgos de quedar gravemente dañados de por vida, cuando en realidad los riesgos no superan los beneficios.
Este compendio de estudios de expertos, contiene la suficiente evidencia para que los padres puedan presentar a sus médicos y abogados y prevenir que su hijos sean intoxicados con vacunas o inyecciones génicas que no tienen los suficientes estudios de seguridad como corresponde. Tambien sirve para educar a los médicos sin pensamiento crítico. Click aqui para descargar este compendio
Efectos Adversos
Es manifiesta la necesidad de evaluar la seguridad de cada vacuna contra la hepatitis B en ensayos clínicos sólidos. La siguiente es una lista de las reacciones adversas poscomercialización notificadas que se agregaron al prospecto de Engerix-B porque Merck tenía una “base para creer que existe una relación causal entre el medicamento y la aparición del evento adverso” :
- Pruebas de función hepática anormales; Reacción alérgica; Alopecia; Reacción Anafilactoide; Anafilaxia; angioedema; Apnea; Artralgia; Artritis; Síntomas similares al asma; parálisis de Bell; Broncoespasmo; Conjuntivitis; Reacciones Dermatológicas; Dispepsia; Dolor de oidos; Eczema; Equimosis; Encefalitis; Encefalopatía; Eritema Multiforme; Eritema nudoso; Síndorme de Guillain-Barré; Síndrome de hipersensibilidad (similar a la enfermedad del suero que aparece días o semanas después de la vacunación); hipoestesia; queratitis; Liquen plano; Meningitis; Migraña; Esclerosis múltiple; Mielitis; Neuritis; Neuropatía; Neuritis óptica; Palpitaciones; Parálisis; paresia; Parestesia; Púrpura; Convulsiones; Síndrome de Stevens-Johnson; Síncope; Taquicardia; Tinnitus; Debilidad Muscular Transversa; Trombocitopenia; Urticaria; vasculitis; Vértigo; Alteraciones visuales. Ver en el propio prospecto aqui
Y estas son las reacciones adversas poscomercialización reportadas para Recombivax HB agregadas al prospecto porque GSK tenía una base para concluir que cada una tiene una relación causal con esa vacuna:
- Agitación; Alopecia; Reacciones Anafilácticas/Anafilactoides; Artralgia; Artritis; Dolor De Artritis En Las Extremidades; Enfermedades autoinmunes; parálisis de Bell; Broncoespasmo; Constipación; Conjuntivitis; Reacciones Dermatológicas; Equimosis; Eczema; Elevación De Las Enzimas Hepáticas; Encefalitis; Eritema Multiforme; Eritema nudoso; Exacerbación De La Esclerosis Múltiple; Convulsión febril; Síndorme de Guillain-Barré; Infección de herpes; Reacciones hipersensibles; Síndrome de hipersensibilidad (similar a la enfermedad del suero que aparece días o semanas después de la vacunación); Hipestesia; Aumento de la tasa de sedimentación de eritrocitos; Irritabilidad; síndrome similar al lupus; Migraña; Esclerosis múltiple; Debilidad muscular; Mielitis, incluida la mielitis transversa; Neuritis óptica; Neuropatía periférica; Petequias; Poliarteritis nudosa; Radiculopatía; Convulsión; Síndrome de Stevens-Johnson; Somnolencia; Síncope; lupus eritematoso sistémico (LES); Taquicardia; Trombocitopenia; Tinnitus; Urticaria; Urticaria; uveítis; vasculitis; Alteraciones visuales. Ver en el propio prospecto aqui
Estas reacciones poscomercialización revelan un patrón constante de trastornos autoinmunes, neurológicos y otros trastornos crónicos que aparecerían o solo se diagnosticarían años después de vacunar a un bebé.
Sin embargo, en lugar de investigar estos eventos adversos en ensayos clínicos metodológicamente sólidos, el HHS responde a estos informes posteriores a la comercialización de lesiones crónicas de por vida diciendo que «no se ha demostrado la causalidad», sabiendo muy bien que es muy poco probable que se demuestre la causalidad, de una forma u otra, hasta que se realice un ensayo controlado con placebo de duración suficiente.
Sobredosis de Aluminio
El calendario escolar tiene sobredosis de aluminio. El aluminio que es tóxico al sistema nervioso central y a los huesos. Si tomamos en cuenta que la dosis maximas es de 5 microgramos por kilogramo, un bebe recién nacido no puede recibir mas de 20 mcg/dia y con solo la vacuna de hepatitis B, recibe 250 mcg , es decir 12 veces mas de los niveles permitidos, con un sistema inmunológico que aun se esta desarrollando. Ver niveles permisibles en : El Código de Regulaciones Federales, CFR, Título 21, Volumen 4, publicados en FDA.gov de la Federal Drug Administration (FDA),
https://www.accessdata.fda.gov/scripts/cdrh/cfdocs/cfcfr/CFRSearch.cfm?fr=201.66 https://www.accessdata.fda.gov/scripts/cdrh/cfdocs/cfcfr/CFRSearch.cfm?fr=201.323
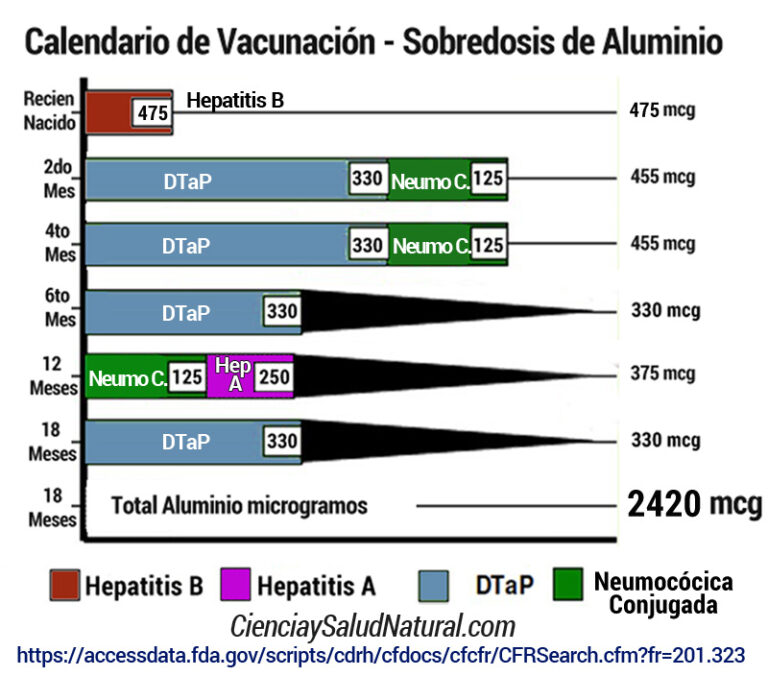
Si su hijo/a o nieto/a tiene mutacion MTHFR, que mucha gente la padece (30%) entonces si lo vacunan corre un gran peligro porque el aluminio es toxico para las mitocondrias
Dr. Stanley Plotkin asesor de laboratorios fabricantes de vacunas admite bajo declaración jurada que la Vacuna de Hepatitis B, solo tuvo 4 dias de estudios de seguridad https://www.bitchute.com/video/0ojBNV0Z19PA/ vea usted mismo los datos en el prospecto; https://gskpro.com/content/dam/global/hcpportal/en_US/Prescribing_Information/Engerix-B/pdf/ENGERIX-B.PDF
Falta de eficiencia de la vacuna
Alrededor del 50% de los niños vacunados contra Hepatitis B pierden su inmunidad a los 5 años, y la vacuna no ha tenido un impacto mensurable en la prevalencia de la infección crónica por hepatitis B
Este documento contiene la suficiente evidencia cientifica (más de 150 referencias) para que las madres puedan presentar a sus médicos y abogados y lograr exenciones para prevenir ser dañadas con vacunas o inyecciones génicas, que no tienen los suficientes estudios de seguridad como corresponde. Tambien sirve para educar a los médicos sin pensamiento crítico. descargar libro, click aqui
2. Varios estudios de vacunados versus no vacunados demuestran eventos adversos asociados con la vacuna contra la hepatitis B
Vacuna contra la hepatitis B y problemas hepáticos en niños estadounidenses menores de 6 años
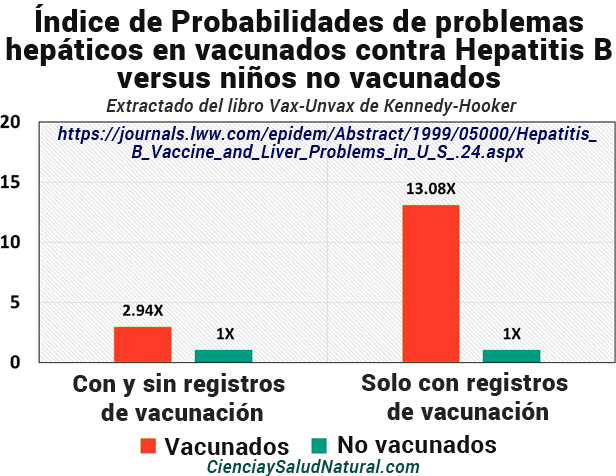
El Gráfico 1 muestra los resultados del artículo “La vacuna contra la hepatitis B y los problemas hepáticos en niños estadounidenses menores de 6 años”, publicado en la revista Epidemiology en 1999. 2
La autora principal es la Dra. Monica A. Fisher, afiliada a la Departamento de Epidemiología de la Universidad de Michigan en Ann Arbor. En este estudio de 5.505 niños que participaron en la Encuesta Nacional de Información de Salud de 1993, los niños menores de seis años que recibieron al menos una dosis de la vacuna contra la hepatitis B tenían 2,94 veces más probabilidades de ser diagnosticados con problemas hepáticos que los niños que no recibieron una. vacuna contra la hepatitis B (IC del 95% de 1,07 a 8,05). 3
Al considerar solo a los niños con registro de vacunación, el índice de probabilidades (odds ratio) en el grupo vacunado aumentó a 13,08 veces en comparación con el grupo que no había sido vacunado contra la hepatitis B (IC del 95% de 2,66 a 64,39). 4 Ambos resultados informados fueron estadísticamente significativos. 5 La diferencia entre el Los resultados “con y sin registros de vacunación” y “solo con registros de vacunación” pueden deberse a personas contadas en el grupo “no vacunados” que fueron vacunadas pero no poseían registros de vacunación.
Gráfico 1: Índice de probabilidades para problemas hepáticos en niños de 0 a 5 años que recibieron al menos una vacuna contra la hepatitis B versus niños no vacunados contra la hepatitis B (Fisher et al. 1999).
La inmunización con la vacuna contra la hepatitis B acelera la enfermedad similar al Lupus eritematoso sistémico (LES) en un modelo murino
El Gráfico 2 muestra los resultados del artículo “La inmunización con la vacuna contra la hepatitis B acelera la enfermedad similar al LES en un modelo murino”, publicado en el Journal of Autoimmunity en 2014.6 La autora principal es la Dra. Nancy Agmon-Levin, afiliada a la Centro Zabludowicz de enfermedades autoinmunes Enfermedades en el Centro Médico Sheba en Tel-Hashomer, Israel. El Dr. Yehuda Shoenfeld, titular de la cátedra Laura Schwarz-Kip de autoinmunidad en la Universidad de Tel Aviv en Israel, es el autor correspondiente y es considerado una de las principales autoridades mundiales en autoinmunidad.
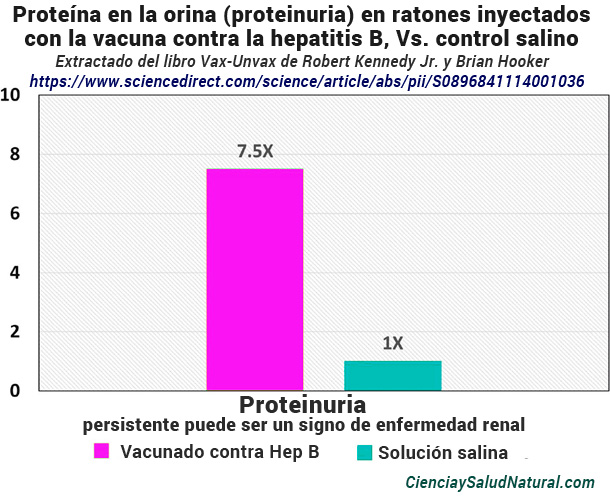
En este estudio, los investigadores inyectaron a ratones hembra 0,4 mililitros de la vacuna contra la hepatitis B Engerix® o de solución salina tamponada con fosfato a las edades de 8 y 12 semanas. La solución salina tamponada con fosfato es inerte y proporciona un control placebo adecuado. Los investigadores midieron la proteína en la orina (proteinuria) como indicador de enfermedad renal. En consecuencia, los niveles de proteína en la orina de los ratones hembra vacunados fueron 7,5 veces mayores que los de los ratones que recibieron solución salina tamponada con fosfato (valor de p <0,004).7 Además, los ratones inyectados con Engerix ® mostraron nefropatología (enfermedad renal) grave y avanzada en comparación con los ratones que recibieron solución salina tamponada con fosfato o solo adyuvante de aluminio .8
Gráfico 2
El Gráfico 2 trata sobre proteína en la orina (proteinuria) de ratones hembra inyectados con la vacuna contra la hepatitis B en comparación con ratones hembra inyectados con solución salina tamponada con fosfato (Agmon-Levin et al. 2014). Tener niveles elevados de proteína en la orina de forma persistente puede ser un signo de enfermedad renal.
El momento oportuno para la vacunación pediátrica y el riesgo de diabetes mellitus insulinodependiente
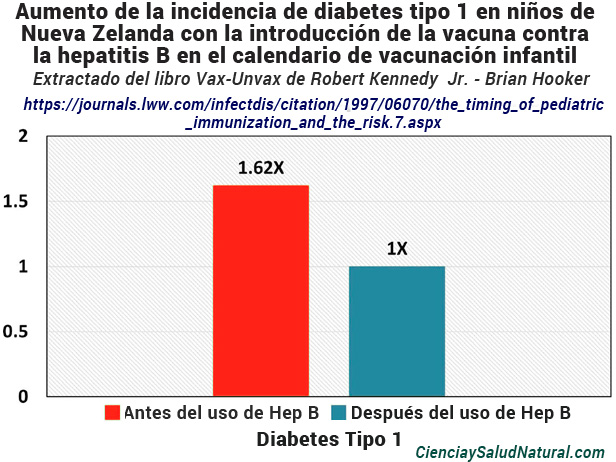
El Gráfico 3 muestra los resultados del artículo «El momento de la vacunación pediátrica y el riesgo de diabetes mellitus insulinodependiente» (“The Timing of Pediatric Immunization and the Risk of Insulin-Dependent Diabetes Mellitus”), publicado en Infectious Diseases in Clinical Practice en 1997.9 El autor principal es el Dr. John B. Classen, afiliado a Inmunoterapias Classen en Baltimore, Maryland. La incidencia de diabetes tipo 1 en niños que viven en Christchurch, Nueva Zelanda, aumentó de 11,2 por 100.000 (promedio entre 1982 y 1987) a 18,1 por 100.000 (promedio entre 1989 y 1991) después de la introducción de la vacuna contra la hepatitis B en 1988 (p -valor = 0,0008). 10 Más del 70% de los niños menores de 16 años fueron vacunados durante los primeros años del programa. 11
Gráfico 3: Aumento de la incidencia de diabetes tipo 1 en niños de Nueva Zelanda con la introducción de la vacuna contra la hepatitis B en el calendario de vacunación infantil (Classen et al. 1997).
Vacuna recombinante contra la hepatitis B y el riesgo de esclerosis múltiple: un estudio prospectivo
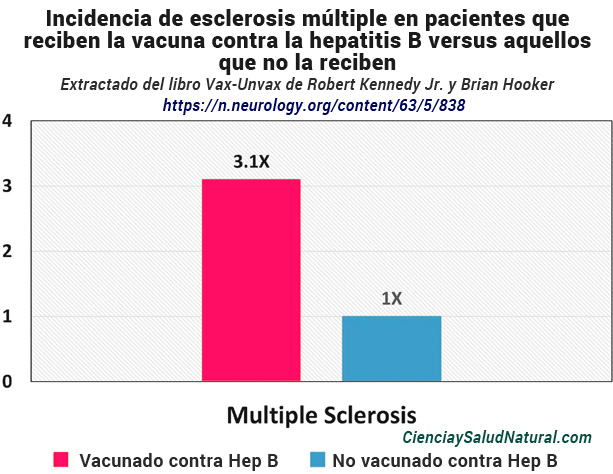
El Gráfico 4 muestra los resultados del artículo “La vacuna recombinante contra la hepatitis B y el riesgo de esclerosis múltiple: un estudio prospectivo”, publicado en Neurology en 2004.12 El autor principal es el Dr. Miguel A. Hernán, afiliado al Departamento de Epidemiología en la Escuela de Salud Pública de Harvard en Boston, Massachusetts. Dentro de la población de la Base de Datos de Investigación de Práctica General (GPRD) del Reino Unido, que incluía a más de 3 millones de pacientes, los pacientes que recibieron una vacuna contra la hepatitis B en los tres años anteriores tenían 3,1 veces más probabilidades de recibir un diagnóstico de esclerosis múltiple en comparación con pacientes que no habían recibido una vacuna contra la hepatitis B en los tres años anteriores. 13 La diferencia en la incidencia fue estadísticamente significativa, con un intervalo de confianza del 95% de 1,5 a 6,3. 14
Gráfico 4: Incidencia de esclerosis múltiple en pacientes que reciben la vacuna contra la hepatitis B versus aquellos que no la reciben (Hernán et al. 2004).
Inmunogenicidad de la hepatitis B después de un ciclo de vacunación primaria asociada con asma, rinitis alérgica y sensibilización a alérgenos
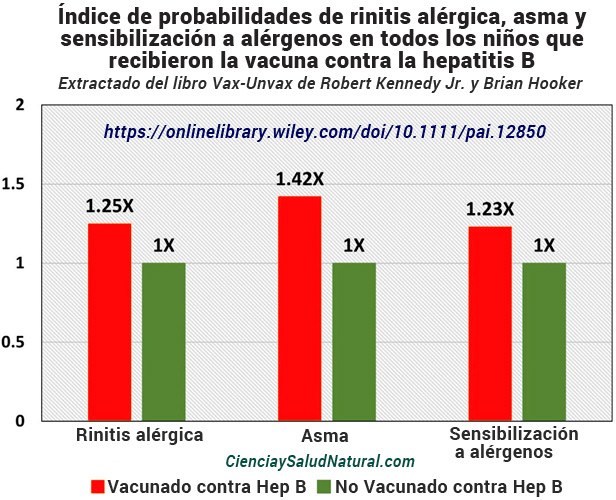
El Gráfico 5 muestra los resultados del artículo “Inmunogenicidad de la hepatitis B después de un ciclo de vacunación primaria asociado con asma, rinitis alérgica y sensibilización a alérgenos”, publicado en la revista Pediatric Allergy and Immunology en 2018. 15 Dr. Dong Keon Yon, afiliado a el Departamento de Pediatría del Centro Médico CHA Bundang en CHA
La Facultad de Medicina de la Universidad de Seongnam, Corea, es el autor principal del estudio. De 3.176 niños coreanos de 12 años que recibieron la serie de tres inyecciones de vacuna contra la hepatitis B cuando eran bebés, 976 niños estaban produciendo actualmente anticuerpos contra el antígeno de superficie de la hepatitis B, y 2.200 niños no. 16
Los niños que tenían anticuerpos positivos contra el antígeno de superficie de la hepatitis B mostraron una mayor incidencia de asma (9,7% a 7,0%, valor de p = 0,009), rinitis alérgica (33,3% frente a 28,8%, valor de p = 0,013) y sensibilización a alérgenos. (59,2 % frente a 54,5 %, valor de p = 0,014) en comparación con los niños vacunados que tenían anticuerpos negativos. 17
Este estudio también demuestra la disminución de la inmunidad asociada con la vacunación contra la hepatitis B en la infancia, ya que solo el 30,7% de los vacunados generaban anticuerpos específicos contra la hepatitis B a los 12 años.18
Gráfico 5 — Índice de probabilidades (Odds ratio) para rinitis alérgica, asma y sensibilización a alérgenos en todos los niños que reciben la vacuna contra la hepatitis B. Los niños que se seroconvirtieron para producir anticuerpos contra la hepatitis B se comparan con los niños que no lo hicieron (Yon et al. 2018).
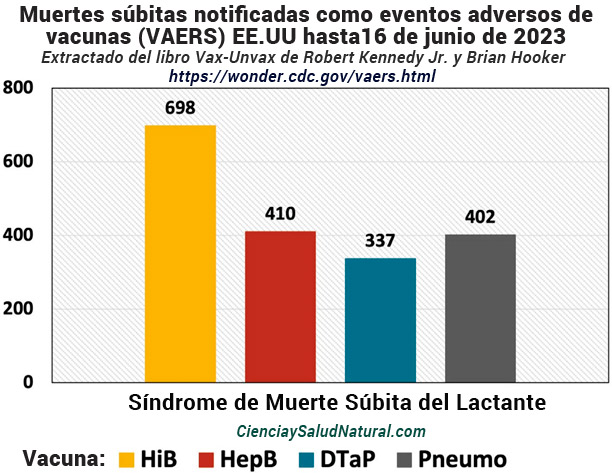
La figura 6 muestra nuestro análisis de los casos de SMSL notificados después de las vacunas contra la hepatitis B, Haemophilus influenzae B, difteria, tétanos, tos ferina acelular y neumonía. 19 VAERS ha implicado la vacunación contra la hepatitis B en 410 muertes por SMSL. 20 Muchas de estas vacunas se administran simultáneamente y algunos de los informes anteriores se asignaron a múltiples vacunas.
Informes VAERS de muertes por Síndrome de Muerte Súbita del Lactante SMSL
Gráfico 6: Número de muertes por Síndrome de Muerte Súbita del Lactante, SMSL notificadas a la base de datos del Sistema de notificación de eventos adversos a las vacunas (VAERS) de los CDC hasta el 16 de junio de 2023. https://vaers.hhs.gov/data.html.
Penina Haber (de la Oficina de Seguridad de las Inmunizaciones de los Centros para el Control de Enfermedades) y sus compañeros de trabajo completaron una breve encuesta de los informes del VAERS asociados con la vacuna contra la hepatitis B que incluían un tratamiento significativo de los bebés que recibieron la vacuna sola o dentro de una vacuna combinada (multivalente). 21
En general, los investigadores informaron 10.291 informes de eventos adversos en niños menores de dos años que recibieron la vacuna contra la hepatitis B durante un período de 11 años desde enero de 2005 hasta diciembre de 2015. 22 Esto incluyó 197 informes de síndrome de muerte súbita del lactante (SMSL ). 23
A partir de esto, los autores del estudio concluyeron: “Review [ sic] las vacunas contra la HepB actualmente autorizadas en EE. UU. administradas solas o en combinación con otras vacunas no revelaron problemas de seguridad nuevos o inesperados”. 24
Sin embargo, el estudio no proporcionó ninguna base para realizar comparaciones con respecto a las muertes por SMSL. En un estudio similar que involucra la vigilancia de eventos adversos de la vacuna en Corea del Sur, la mayor proporción de muerte súbita en lactantes después de la vacunación estuvo relacionada con la vacuna contra la hepatitis B. 25
Dr Peter McCullough: «Las vacunas contra la hepatitis B administradas a los bebés normales con madres normales son completamente innecesarias. No hay ningún beneficio porque a menos que la madre esté abusando activamente de las drogas o tenga hepatitis B, no hay riesgo». Además la vacuna tienen al menos 250 microgramos (sobredosis) de aluminio que es neurotóxico, lea los efectos adversos del prospecto y se dará cuenta que su pediatra, si se la recomienda, es porque solo sigue un protocolo elaborado por los laboratorios fabricantes de vacunas dictado por la OMS que esta controlada por estos laboratorios. Ver efectos adversos en el prospecto . Item 6.2 Postmarketing Experience
https://www.fda.gov/media/119403/download
Resumen
Análisis no publicado de las muertes por SMSL asociadas con la vacuna contra la hepatitis B del VAERS. 26 , 27 , 28 , 29 , 30 , 31 Hay otros informes de eventos adversos asociados con la vacuna contra la hepatitis B (por ejemplo, Agmon-Levin et al. sobre el síndrome de fatiga crónica y la fibromialgia). 32 Sin embargo, las publicaciones destacadas en este articulo comparan específicamente poblaciones vacunadas y no vacunadas.
Referencias sección 2 (Varios estudios de vacunados versus no vacunados)
- “Hepatitis B Vaccination of Infants, Children, and Adolescents,” U.S. Centers for Disease Control, accessed March 26, 2023, https://www.cdc.gov/hepatitis/hbv/vaccchildren.htm.
- Monica A. Fisher and Stephen A. Eklund, “Hepatitis B Vaccine and Liver Problems in U.S. Children Less than 6 Years Old, 1993 and 1994,” Epidemiology 10, no. 3 (1999): 337-339, http s://journals.lww.com/epidem/Abstract/1999/05000/Hepatitis_B_Vaccine_and_Liver_Problems_i n_U_S_.24.aspx.
- Ibid.
- Ibid.
- Ibid.
- Nancy Agmon-Levin et al., “Immunization with Hepatitis B Vaccine Accelerates SLE-Like Disease in a Murine Model,” Journal of Autoimmunity 54, (2014): 21-32, doi:10.1016/j.jaut.2014.06.006.
- Ibid.
- Ibid.
- David C. Classen and John Barthelow Classen, “The Timing of Pediatric Immunization and the Risk of Insulin-Dependent Diabetes Mellitus,” Infectious Diseases in Clinical Practice 6, no. 7 (1997): 449-454, https://journals.lww.com/infectdis/citation/1997/06070/the_timing_of_pediatri c_immunization_and_the_risk.7.aspx.
- Ibid.
- Ibid.
- Miguel A. Hernán et al., “Recombinant Hepatitis B Vaccine and the Risk of Multiple Sclerosis: A Prospective Study,” Neurology 63, no. 5 (2004): 838-842, doi:10.1212/01.wnl.0000138433.61870.82.
- Ibid.
- Ibid.
- Dong Keon Yon et al., “Hepatitis B Immunogenicity After a Primary Vaccination Course Associated with Childhood Asthma, Allergic Rhinitis, and Allergen Sensitization.” Pediatric Allergy and Immunology: Official Publication of the European Society of Pediatric Allergy and Immunology 29, no. 2 (2018): 221-224, doi:10.1111/pai.12850.
- Ibid.
- Ibid.
- Ibid.
- “VAERS Data,” VAERS, accessed September 23, 2022, https://vaers.hhs.gov/data.html.
- Ibid.
- Penina Haber et al., “Safety of Currently Licensed Hepatitis B Surface Antigen Vaccines in the United States, Vaccine Adverse Event Reporting System (VAERS), 2005-2015,” Vaccine 36, no. 4 (2018): 559-564, doi:10.1016/j.vaccine.2017.11.079.
- Ibid.
- Ibid.
- Ibid.
- Young June Choe et al., “Sudden Death in the First 2 Years of Life following Immunization in the Republic of Korea,” Pediatrics international: Official Journal of the Japan Pediatric Society 54, no.6 (2012): 905-910, doi:10.1111/j.1442-200X.2012.03697.x.
- Monica A. Fisher and Stephen A. Eklund, “Hepatitis B Vaccine and Liver Problems in U.S. Children Less than 6 Years Old, 1993 and 1994,” Epidemiology 10, no. 3 (1999): 337-339, http s://journals.lww.com/epidem/Abstract/1999/05000/Hepatitis_B_Vaccine_and_Liver_Problems_i n_U_S_.24.aspx
- Nancy Agmon-Levin et al., “Immunization with Hepatitis B Vaccine Accelerates SLE-Like Disease in a Murine Model,” Journal of Autoimmunity 54, (2014): 21-32, doi:10.1016/j.jaut.2014.06.006.
- David C. Classen and John Barthelow Classen, “The Timing of Pediatric Immunization and the Risk of Insulin-Dependent Diabetes Mellitus,” Infectious Diseases in Clinical Practice 6, no. 7 (1997): 449-454, https://journals.lww.com/infectdis/citation/1997/06070/the_timing_of_pediatri c_immunization_and_the_risk.7.aspx.
- Miguel A. Hernán et al., “Recombinant Hepatitis B Vaccine and the Risk of Multiple Sclerosis: A Prospective Study,” Neurology 63, no. 5 (2004): 838-842, doi:10.1212/01.wnl.0000138433.61870.82.
- Dong Keon Yon et al., “Hepatitis B Immunogenicity after a Primary Vaccination Course Associated with Childhood Asthma, Allergic Rhinitis, and Allergen Sensitization.” Pediatric Allergy and Immunology: Official Publication of the European Society of Pediatric Allergy and Immunology 29, no. 2 (2018): 221-224, doi:10.1111/pai.12850.
- VAERS Data,” VAERS, accessed September 23, 2022, https://vaers.hhs.gov/data.html.
- Nancy Agmon-Levin et al., “Immunization with Hepatitis B Vaccine Accelerates SLE-Like Disease in a Murine Model,” Journal of Autoimmunity 54, (2014): 21-32, doi:10.1016/j.jaut.2014.06.006.
La Dra Chinda Brandolino menciona los efectos adversos de la vacuna de hepatitis B, que tiene mas riesgos que beneficio. Vea prospecto Usted mismo y cuestione a su pediatra que tratará de minimizar estos riesgos graves, pero los estudios que presentamos, de expertos sin conflicto de intereses, demuestran su peligro. https://old.bitchute.com/video/ryaaOZQNPl2l/ – Ver prospecto en : https://www.fda.gov/media/119403/download
3. No hay razon científica para la aplicacion de esta vacuna
El CDC recomienda que todos los bebés se vacunen con tres dosis de la vacuna contra la hepatitis B a partir de las 12 horas de vida, con la última dosis administrada antes de los 18 meses de edad para prevenir la transmisión de una madre infectada a su recién nacido. 1
La razón principal por la que los CDC recomendaron la vacunación contra la hepatitis B para todos los recién nacidos en los Estados Unidos en 1991 es por que los funcionarios de salud pública y los médicos no pudieron persuadir a los adultos en grupos de alto riesgo (principalmente usuarios de drogas intravenosas y personas con múltiples parejas sexuales) que se apliquen esta vacuna . 2, 3, 4
La hepatitis B no es común en la infancia y no es contagiosa como las enfermedades infantiles comunes como la tos convulsa o ferina o la varicela. La hepatitis B es principalmente una enfermedad en adultos (entre 20 y 50 años), pero el virus también puede transmitirse de una madre infectada a su bebé recién nacido. La hepatitis B es una infección viral que infecta el hígado y requiere contacto directo con sangre infectada u otros fluidos corporales para la transmisión. Las personas con mayor riesgo de infección por hepatitis B son aquellas que se involucran en el uso ilegal de drogas intravenosas, la prostitución, o múltiples parejas sexuales y personas que han recibido transfusiones de sangre utilizando sangre infectada. 5
Hay seis vacunas recombinantes contra la hepatitis B aprobadas por la FDA para su uso.:
- Engerix-B;
- Recombivax HB;
- Twinrix (combinado con hepatitis A);
- Pediarix (combinado con toxoides diftérica y tetánica, pertussis acelular adsorbida y poliovirus inactivado).
- Comvax (combinado con Haemophilus Influenza Tipo B (HIB). (6)
- Heplisav-B, vacuna adyuvante recombinante, y se recomendó su uso en adultos por el CDC en 2018.
En 2014 habían sido vacunados contra la hepatitis B, hasta julio de 2018, de acuerdo a MedAlerts, se reportaron más de 88.629 (8) eventos adversos al Sistema federal de Reporte de Eventos Adversos a las Vacunas (VAERS) en relación con las vacunas de hepatitis B. Aproximadamente el 50% de esos eventos adversos graves relacionados con la vacuna contra la hepatitis B ocurrieron en niños menores de 3 años, con aproximadamente 1.620 muertes en niños menores de tres años.
De los eventos adversos relacionados con la vacuna informados a VAERS hubo 2.012 (9) muertes relacionadas, 12,460 hospitalizaciones y 3,271 discapacidades relacionadas. 20,326 de los eventos adversos se asociaron con la vacuna contra la hepatitis B sola (no combinada con otras vacunas). Se han informado efectos secundarios leves, como enrojecimiento, calor o hinchazón en el lugar de la inyección donde se aplicó la inyección en relación con la administración de la vacuna contra la hepatitis B.
Durante las últimas tres décadas, se han publicado muchos informes y estudios que relacionan la vacunación contra la hepatitis B con numerosas enfermedades inmunitarias y neurológicas crónicas en niños y adultos. Estos incluyen lupus, (7) artritis, incluyendo poliartritis y artritis reumatoidea (8, 9, 10), síndrome de Guillain Barre, (11) trastornos desmielinizantes como neuritis óptica, parálisis de Bell, mielitis transversa, neuropatía desmielinizante y esclerosis múltiple (12, 13, 14, 15, 16) junto con diabetes mellitus, (17) fatiga crónica, (18) trastornos vasculares y más. (19, 20) . En el informe completo que evalúa la evidencia científica, «Efectos adversos de las vacunas: evidencia y causalidad», publicado en 2012 por el Instituto de Medicina, IOM, 27 se informó sobre los eventos adversos de la vacuna después de la hepatitis B Las vacunas fueron evaluadas por un comité médico. 21
Este documento contiene la suficiente evidencia científica (más de 50) para que las madres puedan presentar a sus médicos y abogados y prevenir sus hijas e hijos sean dañados con vacunas que no tienen los suficientes estudios de seguridad como corresponde. Tambien sirve para educar a los médicos sin pensamiento crítico. No espere hasta último momento para estar protegida… descargar desde: https://cienciaysaludnatural.com/recursos

Estos eventos adversos incluyeron esclerosis múltiple, artritis, síndrome de Guillain Barre, diabetes mellitus, neuritis óptica, mielitis transversa y más. En 26 de los 27 eventos adversos relacionados con la vacuna contra la hepatitis B evaluados, el comité de la IOM concluyó que no había pruebas suficientes para respaldar o rechazar una relación causal entre la vacuna contra la hepatitis B y el evento adverso informado, principalmente porque hubo una ausencia metodológica estudios publicados sólidos o muy pocos estudios de calidad para hacer una determinación. 22 Sin embargo, el comité del IOM concluyó que la evidencia científica «apoya convincentemente» una relación causal entre la anafilaxia y la hepatitis B en individuos sensibles a la levadura. 23
Un estudio de 2010 publicado en Journal of Toxicology and Environmental Health encontró que los recién nacidos varones tenían una probabilidad 3 veces mayor de ser diagnosticados con autismo en comparación con los niños nunca vacunados o vacunados después del primer mes de vida. (24)
Un estudio de 2015, que revisó estudios de casos e investigaciones sobre numerosos trastornos autoinmunes posteriores La vacuna contra la hepatitis B, concluyó que existe un vínculo entre la vacuna contra la hepatitis B y desarrollo de vasculitis, artritis crónica, lupus, esclerosis múltiple, mielitis y trombocitopenia / pancitopenia. El estudio examinó una relación entre la vacuna contra la hepatitis B y otras afecciones, como la neuropatía, la miastenia grave, el síndrome de fatiga crónica, las afecciones cutáneas autoinmunes y más (25)
Desde el 1 de agosto de 2017, se han presentado 861 reclamaciones en el Programa federal de Compensación de Lesiones por Vacunas (VICP) por 89 muertes y 722 lesiones que se produjeron después de la vacunación contra la hepatitis B. De ese número, el Tribunal de Reclamaciones de los EE. UU. Que administra el VICP ha compensado a 324 niños y adultos que presentaron reclamaciones de lesiones por vacunación después de la vacunación con una vacuna combinada contra la hepatitis B o la hepatitis B. (26)
Referencias sección 3 (No hay razon científica para la aplicacion de esta vacuna)
- 1 https://www.cdc.gov/mmwr/preview/mmwrhtml/rr5416a1.htm
- (2) Kasper D, Fauci A, Longo D, et al. Disorders of the Gastrointestinal System: Prophylaxis: Hepatitis B. Harrison’s Principles of Internal Medicine 16th Edition. 2005. pp 1836-1837
- (3) http://www.vhpb.org/files/html/Meetings_and_publications/Viral_Hepatitis_Newsletters/vhv4n2.html
- (4) https://www.cdc.gov/mmwr/preview/mmwrhtml/00033405.htm CDC. Hepatitis B Virus: A Comprehensive Strategy for Eliminating Transmission in the United States through Universal Childhood Vaccination: Recommendations of the Immunization Practices Advisory Committee (ACIP). MMWR Nov. 22, 1991, 40(RR-13);1-19
- 5 https://www.cdc.gov/hepatitis/hbv/hbvfaq.htm#b4
- (6) https://www.cdc.gov/vaccines/hcp/clinical-resources/shortages.html#note1
- (7) https://journals.sagepub.com/doi/abs/10.1177/0961203309345732
- (8)https://academic.oup.com/rheumatology/article/38/10/978/1783598
- (9)https://www.ncbi.nlm.nih.gov/pubmed/2290175
- (10)https://www.ncbi.nlm.nih.gov/pmc/articles/PMC1754158/pdf/v061p00575.pdf
- 11)https://www.nvic.org/vaccines-and-diseases/hepatitis-b/vaccine-injury.aspx
- (12)https://www.ncbi.nlm.nih.gov/pubmed/2962488
- (13)http://www.sciencedirect.com/science/article/pii/014067369192034Y
- (14)https://academic.oup.com/cid/article-abstract/17/5/928/320651?redirectedFrom=fulltext
- (15) https://www.ncbi.nlm.nih.gov/pmc/articles/PMC1073567/
- (16)https://www.ncbi.nlm.nih.gov/pmc/articles/PMC2928079/
- (17)https://www.researchgate.net/publication/228662325_of_Cases_of_IDDM_2_to_4_Years_after_Hepatitis_B_Immunization_is_Consistent_with_Clustering_after_Infections_and_Progression_to_IDDM_in_Autoantibody_Positive
- (18)https://www.ncbi.nlm.nih.gov/pubmed/25427994
- (19)https://www.nejm.org/doi/full/10.1056/NEJM198910263211717
- (20)https://www.ncbi.nlm.nih.gov/pmc/articles/PMC1664388/
- (21) https://www.nap.edu/read/13164/chapter/1 Chap. 8 (453-503)
- (22) (23) https://www.nap.edu/read/13164/chapter/1 Chap. 8 (453-503)
- 24 https://www.ncbi.nlm.nih.gov/pubmed/21058170
- 25 https://www.researchgate.net/publication/278667214_Hepatitis_B_Vaccination_and_Autoimmunity
- 26 https://www.hrsa.gov/sites/default/files/vaccinecompensation/data/vicpmonthlyreporttemplate8_1_17.pdf
4. Riesgos de la hepatitis B comparado con los riesgos de la vacuna contra la hepatitis B
A partir de datos compilados por los Centros para el Control y la Prevención de Enfermedades (CDC) y el Centro Nacional de Estadísticas de Salud, los siguientes documentos ayudan a evaluar los riesgos de la hepatitis B en comparación con los riesgos de la vacuna contra la hepatitis B, para que los padres puedan participar en la elaboración de una decisión informada sobre esta vacuna. Vea efectos adversos en el propio prospecto, que ahora lo han puesto aqui: https://www.fda.gov/media/119403/download
Los padres deben saber que la probabilidad que contraigan hepatitis B mortal es del 0,00001 % o uno en siete millones. También deben saber que todas las vacunas contra la hepatitis B incluyen la neurotoxina aluminio, lo que significa que hay una garantía del 100 % de que su bebé estará expuesto al aluminio si se le inyecta una vacuna contra la hepatitis B. Y finalmente, necesitan saber que los recién nacidos, debido a su bajo peso corporal, la cantidad de aluminio en las vacunas contra la hepatitis B excede los niveles máximos de seguridad establecidos por la Agencia para Sustancias Tóxicas y Registro de Enfermedades, una división de la Departamento de Salud y Servicios Humanos de los Estados Unidos”.
El aluminio en las vacunas es neurotóxico y el calendario de vacunación infantil tiene sobredosis de aluminio. Los estudios de seguridad del aluminio tienen graves errores y este tema esta postergado desde hace décadas. Más de 100 referencias científicas de expertos para que Usted presente a su abogado o médico, para eximir a sus hijos de las vacunas. Descargar libro click aqui
El Departamento de Salud y Servicios Humanos de EE.UU. (HHS) afirma que el aluminio es una neurotoxina y la exposición a este elemento pueden provocar importantes «alteraciones en la función motora, sensorial función y función cognitiva.» https://www.atsdr.cdc.gov/toxprofiles/tp22.pdf pag. 34 Ver sección que dice:
- «Significant alterations in motor function, sensory function, and cognitive function have been detected following exposure to adult or weanling rats and mice or following gestation and/or lactation exposure of rats and mice to aluminum lactate, aluminum nitrate, and aluminum chloride»
- TRADUCCION: «Se han detectado alteraciones significativas en la función motora, la función sensorial y la función cognitiva después de la exposición a ratas y ratones adultos o destetados o después de la exposición durante la gestación y/o la lactancia de ratas y ratones a lactato de aluminio, nitrato de aluminio y cloruro de aluminio»
Un estudio publicado en el Journal of Trace Elements in Medicine and Biology concluyó que el calendario de vacunación de los Centros para el Control y la Prevención de Enfermedades (CDC) de los EE. UU. que muchos otros paises imitan, supera en 15.9 veces el nivel seguro recomendado de aluminio una vez que los investigadores ajustaron el peso corporal.
La exposición crónica se ha relacionado con la patogénesis de múltiples trastornos neuropsiquiátricos y neurodegenerativos. Mientras que la toxicidad del aluminio fue una vez descartada como irrelevante debido a la supuesta poca absorción y rápida eliminación, un creciente cuerpo de investigación muestra que el aluminio se bioacumula en tejidos vulnerables (Tomljenovic et al., 2013) , particularmente el cerebro, y puede ser un importante factor de riesgo evitable en el desarrollo de la enfermedad de:
- Alzheimer (AD; Armstrong et al., 2019),
- el trastorno del espectro autista (TEA; Boretti, 2021; Roe, 2022),
- la encefalopatía por diálisis (Alfrey et al., 1978; Mach et al. 1988) y
- otros trastornos cognitivos y conductuales como la intoxicación aguda por aluminio, que requiere terapia de quelación.
Ver mas sobre alumino aqui: https://cienciaysaludnatural.com/aluminio/
Puntos a tener en cuenta
- Efectos secundarios de la vacuna contra la hepatitis B
- Seguridad de la vacuna contra la hepatitis B Vs riesgos de la hepatitis B
Los documentos presentan hechos y cifras clave que son esenciales para la toma de decisiones informada. Por ejemplo:
- Un niño de riesgo normal no vacunado tiene una probabilidad de 1 en 7.000.000 (o 0,00001 %) de contraer hepatitis B fatal anualmente.
- Alrededor del 50% de los niños vacunados contra la hepatitis B pierden la inmunidad a los 5 años y la vacuna no ha tenido un impacto medible en la prevalencia de la infección crónica por hepatitis B.
- Las convulsiones pueden ocurrir en aproximadamente 1 de cada 1.300 niños vacunados con la vacuna contra la hepatitis B.
- La vacuna contra la hepatitis B contiene una cantidad de aluminio que es 12 veces mayor que el nivel máximo seguro de aluminio en el torrente sanguíneo por día para un bebé de 3.300 Kg..
- El Instituto de Medicina (IOM) encontró que la evidencia es inadecuada para descartar la posibilidad de que la vacunación contra la hepatitis B provoque más de dos docenas de trastornos neurológicos y autoinmunitarios .
Hay que luchar para abolir esta vacuna del calendario de vacunación escolar obligatoria.
Los efectos secundarios de la vacuna contra el Sarampión, Rubeola y Paperas, SRP (MMR en EE.UU.) incluyen convulsiones, que ocurren en aproximadamente 1 de cada 640 niños vacunados, aproximadamente 5 veces más frecuentemente que las convulsiones por infección de sarampión, sepa como eximir a sus hijos de esta vacuna. Este compendio de estudios de expertos, contiene la suficiente evidencia para que los padres puedan presentar a sus médicos y abogados y prevenir que su hijos sean intoxicados con vacunas que no tienen los suficientes estudios de seguridad como corresponde. Tambien sirve para educar a los médicos sin pensamiento crítico. Descargar libro click aqui
Efectos secundarios de la vacuna contra la hepatitis b
Los efectos secundarios comunes de la vacuna contra la hepatitis B incluyen fiebre, diarrea y fatiga/debilidad. 1 Un posible efecto secundario más grave son las convulsiones, que pueden ocurrir en aproximadamente 1 de cada 1.300 niños vacunados con la vacuna contra la hepatitis B. 2-5 Aunque se han observado efectos secundarios graves después de la vacunación contra la hepatitis B, incluidos trastornos neurológicos :
- encefalitis, mielitis transversa,
- neuritis óptica, esclerosis múltiple y
- síndrome de Guillain-Barré y
- enfermedades autoinmunes (p. ej., lupus eritematoso sistémico, artritis reumatoide , y diabetes tipo 1)
El Instituto de Medicina (IOM) afirma que “la evidencia es inadecuada para aceptar o rechazar una relación causal entre la vacuna contra la hepatitis B” y esas condiciones. 6
Para los niños, la vacuna contra la hepatitis B contiene 250 mcg de aluminio. Esta cantidad es 12 veces mayor que el nivel máximo seguro de aluminio en el torrente sanguíneo por día para un bebé de 3,3 kilogramos, según la Agencia para Sustancias Tóxicas y Registro de Enfermedades (ATSDR), una división del Departamento de Estado de EE. UU. de Salud y Servicios Humanos (HHS) . 7 Además, el prospecto del fabricante indica que la vacuna contra la hepatitis B no ha sido evaluada por su “potencial cancerígeno o mutagénico” o su potencial para afectar la fertilidad. 1,8
Como medir los riesgos de los efectos secundarios de las vacunas
Los métodos para medir los riesgos de las vacunas incluyen
- sistemas de vigilancia,
- ensayos clínicos y
- estudios epidemiológicos pero estan llenos de irregularidades.
Control y vigilancia de los efectos secundarios de la vacuna contra la hepatitis b
El gobierno realiza un seguimiento de los casos notificados de efectos secundarios de las vacunas a través del Sistema de notificación de eventos adversos de las vacunas (VAERS). Aproximadamente 114 casos de lesiones permanentes y muerte por la vacuna contra la hepatitis B se informan anualmente a VAERS. 9
Sin embargo, VAERS es un sistema de notificación pasivo: las autoridades no buscan casos activamente y no recuerdan activamente a los médicos y al público que informen los casos. Estas limitaciones han demostrado una significativa subnotificación. 10
Los Centros para el Control y la Prevención de Enfermedades (CDC, por sus siglas en inglés) afirman que “VAERS recibe informes de solo una pequeña fracción de los eventos adversos reales”. 11 De hecho, tan solo el 1 % de los efectos secundarios graves de los productos médicos se notifican a los sistemas de vigilancia pasiva. 12
Además, los informes de VAERS no son prueba de que haya ocurrido un efecto secundario, ya que el sistema no está diseñado para investigar a fondo todos los casos. 13 Como resultado, VAERS no proporciona un recuento exacto de los efectos secundarios de la vacuna contra la hepatitis B.
Sobre los ensayos clínicos de la vacuna contra la hepatitis b
El CDC afirma: “Los ensayos previos a la licencia son relativamente pequeños, generalmente limitados a unos pocos miles de sujetos, y generalmente no duran más de unos pocos años. Los ensayos previos a la autorización generalmente no tienen la capacidad de detectar eventos adversos raros o eventos adversos con aparición tardía”. 10
Los ensayos clínicos de la vacuna contra la hepatitis B en particular generalmente involucraron solo unos pocos cientos de sujetos por estudio. 14 En la era anterior a la vacuna, la hepatitis B mortal anual ocurría en menos de 1 de cada 7.000.000 de niños menores de 10 años con riesgo normal de exposición (es decir, que no nacieron de una madre infectada, no vivían con una persona infectada y no vivir en una comunidad con un gran número de personas infectadas). 15
Unos pocos cientos de sujetos en ensayos clínicos no son suficientes para probar que la vacuna contra la hepatitis B causa lesiones menos permanentes o la muerte que la hepatitis B en niños con riesgo normal de exposición

Alberto Castro, Sobredosis de aluminio en el calendario de vacunación infantil Niveles «permisibles» para un bebe que nunca tendrían que haberse permitido
Sobre los estudios epidemiológicos de la vacuna contra la hepatitis b
Los estudios epidemiológicos se ven obstaculizados por los efectos del azar. Por ejemplo, Instituto de Medicina de EE:UU., IOM citó un estudio de 1999 que involucró a unos 135.000 sujetos que buscaba una asociación entre la vacuna contra la hepatitis B y ciertos eventos adversos. 16,17
Aunque el estudio no encontró asociación entre la vacuna contra la hepatitis B y los eventos adversos, no descartó la posibilidad de que la vacuna contra la hepatitis B aumente el riesgo de un evento adverso que provoque una lesión permanente hasta en un 110 %.
En consecuencia, el estudio no descartó la posibilidad de que tales eventos adversos pudieran ocurrir hasta 180 veces más a menudo que la muerte por hepatitis B en niños con riesgo normal de exposición: 1 en 3.900 en comparación con 1 en 700.000.
El abanico de posibilidades encontrado en el estudio hace que el resultado no sea concluyente; incluso los grandes estudios epidemiológicos no son lo suficientemente precisos para demostrar que la vacuna contra la hepatitis B causa lesiones menos permanentes o la muerte que la hepatitis B en niños con un riesgo normal de exposición.
Seguridad de la vacuna Vs. riesgos de la hepatitis b
No se ha probado que la vacuna contra la hepatitis B sea más segura que la hepatitis B para niños con riesgo normal de exposición. El prospecto de la vacuna plantea preguntas sobre las pruebas de seguridad para el cáncer, las mutaciones genéticas y la fertilidad alterada.
Aunque VAERS rastrea algunos eventos adversos, es demasiado inexacto para medir el riesgo de hepatitis B. Los ensayos clínicos que incluyen unos pocos cientos de sujetos no tienen la capacidad de detectar reacciones adversas graves menos comunes, y los estudios epidemiológicos están limitados por los efectos de oportunidad.
Los estudios de seguridad de la vacuna contra la hepatitis B carecen de poder estadístico. Una revisión de los estudios de seguridad de la vacuna contra la hepatitis B realizada por el IOM encontró que la evidencia era inadecuada para descartar la posibilidad de que la vacunación contra la hepatitis B provoque más de dos docenas de trastornos neurológicos y autoinmunitarios.6
Debido a que contraer un caso de hepatitis B con secuelas permanentes (efectos secundarios) es tan raro en niños con riesgo normal de exposición, el nivel de precisión de los estudios de investigación disponibles es insuficiente para descartar la posibilidad de que la vacuna contra la hepatitis B cause una lesión permanente mayor. o muerte que la hepatitis B en niños de riesgo normal.
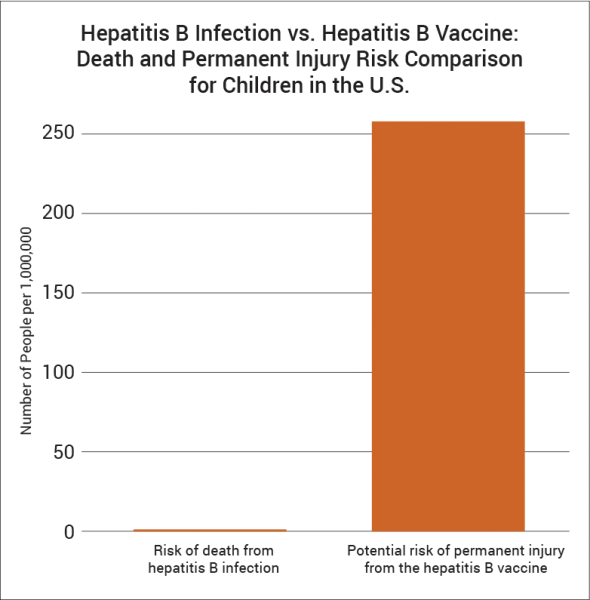
Figura arriba : Un estudio de 1999 citado por IOM no descartó la posibilidad de que la vacuna contra la hepatitis B pueda causar un evento adverso que provoque lesiones permanentes 180 veces más a menudo que la hepatitis B puede ser fatal para los niños estadounidenses con un riesgo normal de exposición.
¿cómo se transmite la hepatitis b?
La hepatitis B se transmite a través de la mezcla de fluidos corporales con los de una persona infectada, generalmente con sangre infectada. Las rutas de transmisión más comunes son el contacto sexual entre heterosexuales con múltiples parejas u hombres que tienen sexo con hombres y el uso de drogas inyectables. 2
El virus también se puede transmitir al nacer de una madre infectada. 22 El contacto casual con la saliva, las lágrimas, el sudor y la orina de una persona infectada son formas poco probables de transmisión. 22 La hepatitis B no se transmite al amamantar, besar, abrazar, tomarse de la mano, toser, estornudar o compartir platos, utensilios para comer o vasos para beber. 26
A pesar del uso generalizado de la vacuna contra la hepatitis B durante más de 25 años, la prevalencia de la infección crónica por hepatitis B en los EE. UU. se ha mantenido casi igual desde 1976, cuando la tasa era del 0,3 % de la población. 9 Se estima que entre 1 de cada 60 000 (0,0017 %) y 1 de cada 80 000 (0,0013 %) personas mueren anualmente de cirrosis hepática o cáncer de hígado relacionados con la hepatitis B. 30
La gran mayoría de las infecciones por hepatitis B ocurren en personas que:
- Participar en conductas sexuales de alto riesgo o uso de drogas intravenosas.
- El 79% de las infecciones por hepatitis B en adultos y adolescentes ocurren entre heterosexuales con múltiples parejas, hombres que tienen sexo con hombres o usuarios de drogas inyectables. 22
- Vive con una persona infectada.
- Antes del uso generalizado de la vacuna contra la hepatitis B, el 50 % de las infecciones por hepatitis B en niños ocurrían en bebés nacidos de madres infectadas. 22
- El 67% de los niños infectados con hepatitis B después del nacimiento viven con una persona infectada. 31
- Vive en comunidades donde la infección por hepatitis B es inusualmente frecuente.
- La mayoría de los adultos y adolescentes infectados sin fuente conocida de exposición viven en comunidades donde la prevalencia de la hepatitis B es de tres a cinco veces mayor que en la población general. 32
- La prevalencia de hepatitis B en comunidades que emigraron a los EE. UU. desde países con alta endemicidad de hepatitis B es de 14 a 28 veces mayor que en la población general. 33
Antes del uso generalizado de la vacuna contra la hepatitis B, anualmente menos de 1 de cada 7.000.000 o el 0,00001 % de los niños con riesgo normal de exposición (es decir, que no nacieron de una madre infectada, no vivían con una persona infectada y no vivían en un comunidad con un gran número de personas infectadas) contrajeron hepatitis B crónica que condujo a una cirrosis hepática fatal o cáncer más adelante en la vida . 34
Tratamientos disponibles
Debido a que la hepatitis B se resuelve por sí sola en la mayoría de los casos, generalmente solo se necesita un tratamiento de apoyo. Como tal, las opciones de tratamiento incluyen lo siguiente:
- descanso e hidratacion
- Medicamentos antivirales, disponibles para tratar a personas crónicamente infectadas con niveles altos tanto del virus de la hepatitis B como de enzimas hepáticas en la sangre durante al menos seis meses; las opciones incluyen interferones o adefovir, entecavir, lamivudina, telbivudina y tenofovir 35
- Inmunoglobulina, disponible para personas que están expuestas a infecciones, incluidos los bebés de madres con infección crónica y pacientes inmunocomprometidos, como los que reciben quimioterapia 22
Embarazadas pueden hacerce un análisis de sangre para detectar hepatitis B
Las mujeres embarazadas pueden hacerce un análisis de sangre para detectar hepatitis B cuando acuden al médico. Si una mujer no ha visto a un médico durante el embarazo, se le hará una prueba en el hospital cuando dé a luz. 26 Alrededor del 99,7 % de las mujeres en los EE. UU. son negativas para la hepatitis B. 40
Alrededor del 50% de los niños vacunados pierden su inmunidad a los 5, 18 años y la vacuna no ha tenido un impacto medible en la prevalencia de la infección crónica por hepatitis B . 41

La mayoría de los casos fatales de hepatitis B ocurren más tarde en la vida, después de los 55 años. Este gráfico muestra la tasa de mortalidad de niños menores de 10 años con riesgo normal de exposición (es decir, no nacieron de una madre infectada, no vivieron con una persona infectada , y no vivían en una comunidad con una gran cantidad de personas infectadas) que contrajeron hepatitis B y morirían de cirrosis o cáncer más adelante en la vida. La tasa era de 0,014 por 100.000 antes del uso generalizado de la vacuna y se compara con las principales causas de muerte en niños menores de 10 años en 2015, cuando la tasa de muerte por 100.000 por homicidio era de 1,3, seguida por cáncer (2,0), SMSL ( 3.9), lesión no intencional (8.2) y anomalías congénitas (13.6). La tasa de muerte o lesión permanente de la vacuna contra la hepatitis B (Engerix-B)
Descargar libros desde https://cienciaysaludnatural.com/recursos
Referencias Sección 4 (Riesgos de la hepatitis B comparado con los riesgos de la vacuna contra la hepatitis B)
- Merck Sharp & Dohme Corp. Whitehouse Station (NJ): Merck and Co., Inc. Recombivax HB Hepatitis B Vaccine (Recombinant); revised 2018 Dec [cited 2022 May 28]. https://www.fda.gov/downloads/BiologicsBloodVaccines/Vaccines/ApprovedProducts/UCM110114.pdf.
- Between 1993 and 1997, the government’s Vaccine Adverse Event Reporting System (VAERS) received 437 reports of seizure-related adverse events involving hepatitis B vaccine in children <1 year of age.3 In the same time period, VAERS received 940 reports of seizure-related adverse events involving measles vaccine in children 1-2 years of age.4 This suggests that seizures from hepatitis B vaccine may occur half as often as seizures from MMR vaccine, half of 1 in 6405 or about 1 in 1,300.
- Centers for Disease Control and Prevention. Washington, D.C.: U.S. Department of Health and Human Services. CDC wonder: about the Vaccine Adverse Event Reporting System (VAERS); [cited 2022 May 11]. https://wonder.cdc.gov/vaers.html. Query for seizure-related events involving hepatitis B vaccine, 1993-1997.
- Centers for Disease Control and Prevention. Washington, D.C.: U.S. Department of Health and Human Services. CDC wonder: about the Vaccine Adverse Event Reporting System (VAERS); [cited 2022 May 11]. https://wonder.cdc.gov/vaers.html. Query for seizure-related events involving all measles-containing vaccines, 1993-1997.
- Vestergaard M, Hviid A, Madsen KM, Wohlfahrt J, Thorsen P, Schendel D, Melbye M, Olsen J. MMR vaccination and febrile seizures: evaluation of susceptible subgroups and long-term prognosis. JAMA. 2004 Jul 21;292(3):356. https://jamanetwork.com/journals/jama/fullarticle/199117.
- Institute of Medicine (IOM). Adverse effects of vaccines: evidence and causality. Washington, D.C.: National Academies Press; 2012. 438,443,446,450,455,466,473,485,490-3. https://www.ncbi.nlm.nih.gov/books/NBK190024/pdf/Bookshelf_NBK190024.pdf.
- Physicians for Informed Consent. Newport Beach (CA): Physicians for Informed Consent. Aluminum – vaccine risk statement (VRS). Aluminum in vaccines: what parents need to know; 2020 Aug [cited 2022 May 28]. https://physiciansforinformedconsent.org/aluminum-in-vaccines.
- GlaxoSmithKline Biologicals. Rixensart (Belgium): GlaxoSmithKline Biologicals. Engerix-B [Hepatitis B Vaccine (Recombinant)] injectable suspension; revised 2021 Jun [cited 2022 Jul 14]. https://gskpro.com/content/dam/global/hcpportal/en_US/Prescribing_Information/Engerix-B/pdf/ENGERIX-B.PDF.
- Centers for Disease Control and Prevention. Washington, D.C.: U.S. Department of Health and Human Services. CDC wonder: about the Vaccine Adverse Event Reporting System (VAERS); [cited 2022 May 13]. https://wonder.cdc.gov/vaers.html. Query for death and permanent disability involving hepatitis B vaccine, 1993-1997.
- Centers for Disease Control and Prevention. Manual for the surveillance of vaccine-preventable diseases. 5th ed. Miller ER, Haber P, Hibbs B, Broder K. Chapter 21: surveillance for adverse events following immunization using the Vaccine Adverse Event Reporting System (VAERS). Atlanta: Centers for Disease Control and Prevention; 2011. 1,2,8. https://www.cdc.gov/vaccines/pubs/surv-manual/chpt21-surv-adverse-events.pdf.
- Centers for Disease Control and Prevention, Food and Drug Administration. Washington D.C.: U.S. Department of Health and Human Services. Guide to interpreting VAERS data; [cited 2022 May 28]. https://vaers.hhs.gov/data/dataguide.html.
- Kessler DA. Introducing MEDWatch. A new approach to reporting medication and device adverse effects and product problems. JAMA. 1993 Jun 2;269(21):2765-8. https://www.sciencedirect.com/science/article/abs/pii/0163834394900515?via%3Dihub.
- Centers for Disease Control and Prevention. Washington D.C.: U.S. Department of Health and Human Services. CDC wonder: about the Vaccine Adverse Event Reporting System (VAERS); [cited 2022 May 28]. https://wonder.cdc.gov/vaers.html.
- Institute of Medicine (IOM) Vaccine Safety Committee. Adverse events associated with childhood vaccines: evidence bearing on causality. Stratton KR, Howe CJ, Johnston RB Jr, editors. Washington, D.C.: National Academies Press; 1994. 215. https://pubmed.ncbi.nlm.nih.gov/25144097/.
- Magno H, Golomb B. Measuring the benefits of mass vaccination programs in the United States. Vaccines. 2020 Sep 29;8(4):561. https://pubmed.ncbi.nlm.nih.gov/33003480/.
- Institute of Medicine (IOM) Immunization Safety Review Committee. Immunization safety review: hepatitis B vaccine and demyelinating neurological disorders. Stratton K, Almario D, McCormick MC, editors. Washington, D.C.: National Academies Press; 2002. 53. https://pubmed.ncbi.nlm.nih.gov/25057609/.
- Zipp F, Weil JG, Einhaupl KM. No increase in demyelinating diseases after hepatitis B vaccination. Nat Med. 1999 Sep;5(9):964-5. https://pubmed.ncbi.nlm.nih.gov/10470051/.
22. Centros de Control y Prevención de Enfermedades. Epidemiología y prevención de enfermedades inmunoprevenibles. 13ª ed. Hamborsky J, Kroger A, Wolfe S, editores. Washington, DC: Fundación de Salud Pública; 2015. 151-7, 169. https://physiciansforinformedconsent.org/cdc-pink-book-13th-edition-2015/ .
26. Centros de Control y Prevención de Enfermedades. Washington, DC: Departamento de Salud y Servicios Humanos de EE. UU. Hepatitis B: ¿estás en riesgo? 2013 junio https://www.cdc.gov/knowhepatitisb/PDFs/FactSheet-HepBAreYouAtRisk.pdf .
30. Se estima que entre 3000 y 4000 personas mueren de cirrosis relacionada con la hepatitis B cada año en los EE. UU. Se estima que entre 1000 y 1500 personas mueren cada año de cáncer de hígado relacionado con la hepatitis B en los EE. UU. Esto da como resultado entre 4000 y 5500 muertes relacionadas con la hepatitis B de una población de 320 millones (1 en 60.000 a 1 en 80.000). 22
31. Armstrong GL, Mástil EE, Wojczynski M, Margolis HS. Infecciones infantiles por el virus de la hepatitis B en los Estados Unidos antes de la inmunización contra la hepatitis B. Pediatría. noviembre de 2001; 108(5):1126. https://pubmed.ncbi.nlm.nih.gov/11694691/ .
32. Alter MJ, Hadler SC, Margolis HS, Alexander WJ, Hu PY, Judson FN, Mares A, Miller JK, Moyer LA. La epidemiología cambiante de la hepatitis B en los Estados Unidos. Necesidad de estrategias alternativas de vacunación. JAMA. 2 de marzo de 1990; 263(9):1222. https://pubmed.ncbi.nlm.nih.gov/2304237/ .
33. Centros de Control y Prevención de Enfermedades. Epidemiología y prevención de enfermedades inmunoprevenibles. 10ª ed. Atkinson W, Hamborsky J, McIntyre L, Wolfe C, editores. Washington, DC: Fundación de Salud Pública; 2007. 218. https://physiciansforinformedconsent.org/cdc-pink-book-10th-edition-hepatitis-b-2007 .
34. Magno H, Golomb B. Midiendo los beneficios de los programas de vacunación masiva en los Estados Unidos. Vacunas. 2020 29 de septiembre; 8 (4): 561. https://pubmed.ncbi.nlm.nih.gov/33003480/ .
35. Cigna. Bloomfield (CT): Cigna. Hepatitis B: ¿debo tomar medicamentos antivirales para la hepatitis B crónica? [citado el 7 de mayo de 2022]. https://www.cigna.com/knowledge-center/hw/medical-topics/hepatitis-b-uf1166 .
36. Centros de Control y Prevención de Enfermedades. Washington, DC: Departamento de Salud y Servicios Humanos de EE. UU. hepatitis B y un bebé sano; 31 de mayo de 2015 [citado el 22 de mayo de 2022]: 4. https://www.cdc.gov/hepatitis/common/PeriEducation/HepBHealthyBaby-eng.pdf .
37. En 2012 en los EE. UU., alrededor de 850 000 personas (0,3 %) de una población de 314 millones estaban crónicamente infectadas con hepatitis B. En consecuencia, alrededor del 99,7 % (313/314) de la población era hepatitis B negativa. 3
38. Puliyel J, Naik P, Puliyel A, Agarwal K, Lal V, Kansal N, Nandan D, Tripathi V, Tyagi P, Singh SK, Srivastava R, Sharma U, Sreenivas V. Evaluación de la protección proporcionada por la vacunación contra la hepatitis B en India . Indio J Pediatr. 2018 julio; 85 (7): 514. https://pubmed.ncbi.nlm.nih.gov/29318526/ .
39. Lim JK, Nguyen MH, Kim WR, Gish R, Perumalswami P, Jacobson IM. Prevalencia de la infección crónica por el virus de la hepatitis B en los Estados Unidos. Soy J Gastroenterol. 2020 de septiembre; 115 (9): 1432. https://pubmed.ncbi.nlm.nih.gov/32483003/ .
40. Merck Sharp & Dohme Corp. Whitehouse Station (NJ): Merck and Co., Inc. Recombivax HB Hepatitis B Vaccine (Recombinant); revisado en diciembre de 2018 [citado el 2 de mayo de 2022]. https://www.fda.gov/media/74274/download .
41. Médicos para el Consentimiento Informado. Newport Beach (CA): Médicos para el consentimiento informado. Hepatitis B: declaración de riesgo de la vacuna (VRS). Vacuna contra la hepatitis B: ¿es más segura que la hepatitis B? 2022 agosto https://physiciansforinformedconsent.org/hepatitis-b-vrs .
42. Centros de Control y Prevención de Enfermedades. Washington, DC: Departamento de Salud y Servicios Humanos de EE. UU. 10 causas principales de muerte por grupo de edad, Estados Unidos—2015; [citado el 21 de junio de 2017]. https://www.cdc.gov/injury/images/lc-charts/leading_causes_of_death_age_group_2015_1050w740h.gif .
Ver más y acualizaciones en:
- https://cienciaysaludnatural.com/category/hepatitis-b/
- https://cienciaysaludnatural.com/tema/hepatitis-b/
- Vacuna contra la hepatitis B riesgo de desmielinización inflamatoria del SNC en la infancia
- https://cienciaysaludnatural.com/estudio/vacuna-contra-la-hepatitis-b-riesgo-de-desmielinizacion-inflamatoria-del-snc-en-la-infancia/
- Relación causal entre la vacuna de la Hepatitis B y la esclerosis múltiple en Francia https://cienciaysaludnatural.com/relacion-causal-entre-la-vacuna-hepatitis-b-y-la-esclerosis-multiple-en-francia/
- Vacuna contra la hepatitis B y riesgo de esclerosis múltiple
- https://cienciaysaludnatural.com/estudio/vacuna-contra-la-hepatitis-b-y-riesgo-de-esclerosis-multiple/
- Vacuna contra la hepatitis B y discapacidad del desarrollo en niños https://cienciaysaludnatural.com/estudio/vacuna-contra-la-hepatitis-b-y-discapacidad-del-desarrollo-en-ninos/
- Enfermedad de Vogt-Koyanagi-Harada asociada con la vacunación contra la hepatitis B https://cienciaysaludnatural.com/estudio/enfermedad-de-vogt-koyanagi-harada-asociada-con-la-vacunacion-contra-la-hepatitis-b/
- Lista de mas de 100 estudios sobre efectos adversos de la vacuna contra la hepatitis B https://cienciaysaludnatural.com/category/hepatitis-b/
 CienciaySaludNatural.com
CienciaySaludNatural.com