En la actualidad, los Centros para el Control y la Prevención de Enfermedades (CDC) de EE.UU recomiendan más de 200 dosis a lo largo de la vida de una persona. En 1983, los CDC recomendaban solo 11 dosis de siete vacunas para los niños . No existían recomendaciones de vacunas para adultos, incluidas las mujeres embarazadas, antes de 1986, cuando la Ley Nacional de Lesiones por Vacunas Infantiles de 1986 otorgó a los fabricantes de vacunas protección contra la responsabilidad por lesiones causadas por vacunas.
Los CDC, que influencian a varios paises, otra vez han hecho cambios en el calendario de vacunación actualizado para 2025 para niños, adultos y mujeres embarazadas. Fue publicado el mes pasado, hay marcas recientemente aprobadas de vacunas existentes y una nueva vacuna contra la hepatitis B para mujeres embarazadas tambien inyecciones adicionales recomendadas para personas inmunodeprimidas.
El año pasado, la agencia agregó las vacunas contra el COVID-19 y las vacunas contra el VSR para niños, las vacunas contra el VSR para adultos mayores y las vacunas MPOX para adultos de alto riesgo.
Hasta 2012, a las mujeres embarazadas se les aconsejaba no recibir la mayoría de las vacunas debido a la preocupación de que pudieran dañar al feto.
Ahora los CDC recomiendan cinco o más vacunas de rutina (siete o más vacunas) durante el embarazo, incluidas las de la:
- gripe,
- COVID-19,
- la Tdap (tétano, difteria, tos ferina),
- el VSR o virus respiratorio sincitial,
- la hepatitis B,
- la hepatitis A (si hay riesgo de infección) y
- posiblemente una dosis de refuerzo contra la gripe.
Los CDC dicen que vacunarse durante el embarazo es esencial porque ayuda a las madres a evitar enfermedades y también crea anticuerpos que protegerán a sus bebés durante los primeros meses de vida antes de que puedan vacunarse ellos mismos.
Sin embargo, los expertos dicen que el creciente número de vacunas recomendadas para mujeres embarazadas es preocupante, en particular debido a la falta de ensayos controlados aleatorios lo suficientemente grandes como para identificar problemas de seguridad y porque faltan datos de seguridad a largo plazo.
“Los datos sobre la seguridad de las vacunas son escasos”, afirmó Karl Jablonowski, científico investigador. “Durante el embarazo, son aún más escasos. Y son casi inexistentes en situaciones en las que se administran múltiples vacunas durante el embarazo, que es la realidad clínica”.
Cuando existen datos, los tamaños de muestra suelen ser tan pequeños que el estudio es prácticamente inutilizable, dijo Jablonowski.
Los CDC añaden una nueva marca contra la hepatitis B a pesar de la falta de datos de seguridad en mujeres embarazadas
Este año, los CDC agregaron una nueva marca de vacuna contra la hepatitis B, Heplisav-B , a la lista de vacunas que se pueden administrar a mujeres embarazadas, después de eliminar el texto que decía que Heplisav-B no se recomendaba en el embarazo “debido a la falta de datos de seguridad en personas embarazadas”.
En la reunión de octubre del Comité Asesor sobre Prácticas de Inmunización de los CDC , los CDC dijeron que su división de hepatitis viral estaba trabajando para actualizar la guía para el uso de la vacuna contra la hepatitis B durante el embarazo basándose en los cambios realizados en el prospecto de la Administración de Alimentos y Medicamentos de los EE. UU. (FDA) , pero la eliminación propuesta no se había discutido con el grupo de trabajo.
La etiqueta de Heplisav-B indica que “no existen estudios adecuados y bien controlados de HEPLISAV-B en mujeres embarazadas”. En cambio, las afirmaciones sobre la seguridad para las mujeres embarazadas se basan en un estudio de toxicidad en ratas y un estudio posterior a la autorización de 81 mujeres que estuvieron expuestas a la vacuna durante los 28 días anteriores al embarazo o durante el mismo.
La vacuna apareció por primera vez en el calendario para mujeres embarazadas en 2022, cuando la agencia recomendó la vacuna contra la hepatitis B a todos los adultos de entre 19 y 59 años, incluidas las mujeres embarazadas que no habían sido vacunadas previamente.
La información sobre si las mujeres embarazadas deben recibir la vacuna contra la hepatitis B es contradictoria en el sitio web de los CDC. Una página web de los CDC sobre el embarazo, actualizada en junio, recomienda que las mujeres con alto riesgo reciban la vacuna contra la hepatitis B, una recomendación que coincide con la de la mayoría de los demás países.
Sin embargo, la página web principal de los CDC sobre embarazo y vacunas, actualizada en julio y que enumera todas las vacunas de rutina y no de rutina para mujeres embarazadas, indica que la vacuna contra la hepatitis B se recomienda como vacunación de rutina para las mujeres embarazadas que aún no están vacunadas.
El Colegio Estadounidense de Obstetras y Ginecólogos (ACOG), que representa a más de 60.000 miembros obstetras y ginecólogos y es una de las organizaciones clave que establece las normas para esa industria, también recomienda la vacuna contra la hepatitis B para todas las mujeres embarazadas no vacunadas.
La ACOG cambió sus pautas y comenzó a recomendar la vacuna contra la hepatitis B en 2022, después de que los CDC agregaran la vacuna al calendario de vacunación para adultos , incluidas las mujeres embarazadas, de 19 a 59 años.
La hepatitis B es una infección del hígado que puede volverse crónica y transmitirse a través de fluidos corporales, generalmente por medio de conductas adultas de alto riesgo, como relaciones sexuales sin protección o el uso de drogas por vía intravenosa.
En 1991 , la vacuna contra la hepatitis B se añadió al calendario de vacunación infantil con una investigación de seguridad limitada , aunque sólo corren riesgo los bebés cuyas madres padecen la enfermedad.
Especulan que la incorporación de la vacuna al calendario infantil hara crecer el mercado de 8.380 millones de dólares en 2023 a 8.850 millones de dólares en 2024 y 13.310 millones de dólares en 2032, informó Fortune Business Insights .
Vacunas consideradas inseguras para embarazadas hasta 2009
La vacunación materna es un fenómeno reciente. Las vacunas no se administraban durante el embarazo por temor a que el virus debilitado de la vacuna pudiera dañar al feto en desarrollo, según el Hospital Pediátrico de Filadelfia (CHOP).
Pero según el CHOP, ese riesgo es sólo “teórico”. El sitio web del hospital afirma que las agencias de salud pública desarrollaron sus justificaciones para vacunar a las mujeres embarazadas después de la reciente serie de pandemias.
La vacuna Tdap se agregó al calendario en 2012
En 2012, el comité asesor de los CDC votó para recomendar que las mujeres embarazadas reciban una dosis de Tdap entre las 27 y 36 semanas de gestación para proteger a los bebés de la tos ferina, que puede ser grave.
Sin embargo, es probable que la bacteria que causa la tos ferina (pertussis) contenida en la vacuna Tdap ya no brinde protección, ya que está desactualizada. Los CDC han estado haciendo un seguimiento de los cambios en la prevalencia de las bacterias que causan la tos ferina durante años. Los datos más recientes de los CDC sugieren que la tos ferina causada por Bordetella parapertussis ha superado significativamente a la B. pertussis , el tipo que se trata con las vacunas.
Una investigación publicada en Vaccines en marzo muestra que las vacunas existentes “ apenas brindan protección ” contra esta cepa.
Las vacunas Tdap también contienen vacunas contra el tétano y la difteria, lo que expone tanto a la madre como al bebé a más medicamentos.
El obstetra Dr. James Thorp dijo que la recomendación de la vacuna Tdap para mujeres embarazadas es preocupante. “He ejercido la profesión durante más de 45 años y nunca he visto un caso de tétano o difteria. ¿Por qué estamos administrando esta vacuna?”
La vacuna contra la gripe tiene índices de eficacia bajos y datos de seguridad preocupantes
Los CDC recomiendan la vacuna contra la gripe para las mujeres embarazadas desde al menos 2013, aunque hay evidencia de que la recomendación puede haber comenzado antes. Los CDC afirman que las vacunas contra la gripe se han administrado a las mujeres embarazadas durante más de 50 años .
Incluso los defensores de la vacuna contra la gripe afirman que su eficacia es de tan solo entre el 22% y el 56% en un año determinado (la vacuna contra la gripe de 2014-2015 tuvo una eficacia de tan solo el 13%-23%). Las investigaciones muestran que la vacuna no tiene un efecto importante en la hospitalización , la mortalidad , las infecciones en niños pequeños o el riesgo de contraer la gripe en mujeres embarazadas y sus bebés .
También existen serias preocupaciones con respecto a la vacuna, en particular para las mujeres embarazadas y los niños, porque las inyecciones a menudo contienen timerosal , un conservante a base de mercurio. Según los CDC, las vacunas contra la gripe en viales multidosis contienen esta sustancia química.
Los CDC citan varios estudios de su base de datos Vaccine Safety Datalink que no muestran un mayor riesgo de aborto espontáneo u otros eventos adversos para la salud entre las mujeres que recibieron la vacuna. Sin embargo, los estudios citados eran estudios de eficacia.
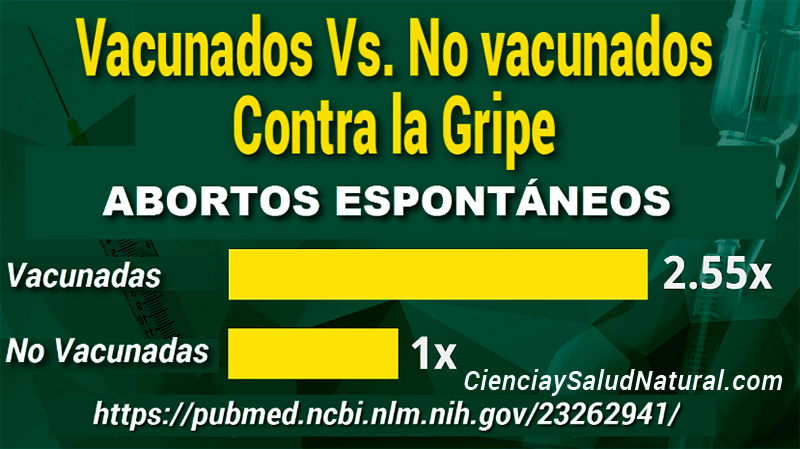
Un análisis de los datos de Vaccine Safety Datalink publicados en la revista Vaccine en 2017 concluyó que las mujeres que recibieron la vacuna contra la gripe tenían el doble de probabilidades, o más, de sufrir un aborto espontáneo que las mujeres que no la recibieron. Los CDC afirman en su sitio web que este estudio tenía “ varias limitaciones ” y señalan otros estudios que muestran que no existe ningún riesgo.
Relación de probabilidades de aborto espontáneo cuando reciben la vacuna contra la gripe antes de la concepción versus mujeres no vacunadas (Irving et al. 2013). https://pubmed.ncbi.nlm.nih.gov/23262941/ https://www.bitchute.com/video/UN5GiGHJ0fVS/
Vacuna contra COVID para embarazadas en EE. UU. y en otros países
En abril de 2021, los CDC emitieron una recomendación urgente para que las mujeres embarazadas y las nuevas madres recibieran la vacuna contra la COVID-19, a pesar de que las mujeres embarazadas fueron excluidas de los estudios originales de seguridad y eficacia y aún no se había realizado ningún ensayo controlado aleatorio.
La entonces directora de los CDC, Rochelle Walensky, emitió la recomendación apenas dos días después de que Pfizer presentara a la FDA su informe sobre el embarazo y la lactancia que detallaba los efectos de la vacuna en las mujeres y los bebés a partir de datos posteriores a su comercialización.
El informe indicó altas tasas de eventos adversos, desde leves a graves, incluidos abortos espontáneos y partos prematuros que la compañía atribuyó a la vacuna.
Los resultados del ensayo controlado aleatorio muy pequeño en mujeres embarazadas que Pfizer finalmente realizó, a partir de 2021, incluyeron solo 391 madres y 335 bebés prematuros y recién nacidos en todo el mundo.
Los resultados del ensayo mostraron que las madres del grupo de la vacuna tenían tasas más altas de preeclampsia e hipertensión gestacional y los bebés expuestos a la vacuna en el útero tenían una puntuación de Apgar marcadamente más baja , tasas más altas de malformaciones congénitas y otros problemas.
En un reciente reanálisis del Sistema de Notificación de Eventos Adversos de Vacunas (VAERS), los investigadores encontraron señales de seguridad (lease inseguridad) para 37 eventos adversos después de la vacuna contra la COVID-19 en mujeres embarazadas.
El Reino Unido y otros países dejaron de recomendar las vacunas para mujeres embarazadas a partir de 2025, citando el bajo riesgo de enfermedad grave por COVID-19 en mujeres embarazadas y bebés según datos epidemiológicos del mundo real.
Sin embargo, los CDC continúan diciendo a las mujeres embarazadas que tienen más probabilidades de enfermarse, necesitar hospitalización y tener un bebé prematuro o muerto si contraen COVID-19, por lo que deben vacunarse.
Las vacunas contra el VSR aumentaron la tasa de partos prematuros en ensayos clínicos
Una vez que el pánico inicial por el COVID-19 comenzó a disminuir a fines de 2022, los medios comenzaron a advertir sobre una posible “ tripledemia ”, ya que el COVID-19, la influenza estacional y el VSR estaban circulando.
Meses después, se dieron a conocer vacunas contra el VSR dirigidas a mujeres embarazadas y personas mayores, y nuevas inyecciones de anticuerpos monoclonales para recién nacidos, que se presentaron para su aprobación a las agencias reguladoras.
Inicialmente, tanto Pfizer como GSK estaban desarrollando vacunas contra el VSR casi idénticas dirigidas a mujeres embarazadas .
GSK suspendió los ensayos de su vacuna materna contra el VRS cuando detectó una señal de seguridad en relación con los nacimientos prematuros entre las mujeres vacunadas. En ese estudio, por cada 54 bebés nacidos de mujeres que recibieron la vacuna, se produjo un nacimiento prematuro adicional.
Los propios datos de los ensayos clínicos de Pfizer para su vacuna contra el VSR, Abrysvo, también mostraron tasas elevadas de parto prematuro entre las mujeres vacunadas, pero Pfizer dijo que las tasas más altas no eran «estadísticamente significativas».
Pfizer también observó más trastornos hipertensivos del embarazo entre las receptoras de la vacuna en comparación con las receptoras de placebo en sus ensayos con Abrysvo. La farmacéutica determinó que la tasa de trastornos no era estadísticamente significativa.
Aun así, la FDA limitó la aprobación de la vacuna para mujeres en las semanas 32 a 36 de su embarazo para reducir el riesgo y ordenó estudios de seguimiento posteriores a la comercialización tanto para el parto prematuro como para la eclampsia . La agencia también etiquetó el parto prematuro como un riesgo potencial asociado con la vacuna.
Algunos miembros del comité asesor de vacunas de la FDA dijeron que tenían serias preocupaciones de seguridad basadas en los datos de los ensayos clínicos, y cuatro miembros votaron en contra de aprobar el medicamento.
Colabore por favor con nosotros para que podamos incluir mas información y llegar a más personas: contribución en mercado pago o paypal por única vez, Muchas Gracias!
Via PAYPAL: Euros o dólares click aqui
ARGENTINA 10.000$ar https://mpago.la/1srgnEY
5.000$ar https://mpago.la/1qzSyt9
1.000$ar https://mpago.la/1Q1NEKM
Solicite nuestro CBU contactenos